 ��������
��������
�������ƣ�
1.���ʪ�ؽ��������Ƶ���ʶ���� ���ʪ�ؽ��������Ƶ��о���һ�������Ĺ��̣�����Ҳû�еõ���ȷ�Ķ��ۡ��ع���һ��ʶ���̣����Ը��������ʶ���ʪ�ؽ��ס�
����20����20����������������Ⱦ���Ե���RA�����ҽ�RA��Ϊ��Ⱦ�Լ����������ƣ�������һ������Ч������һֱû���ҵ���Ⱦ���²������20����40�����Waaler��Rose����ͬ�·��������ʪ���ӣ���������RA�ij�����ϵ��һ���Ժ�½��������Bϸ�������߸�����������RA�����е����á���Һ���ߵ��쳣,����Ϊ��RA��������ؼ����õ����ء�����˼��ͳ���˽�40�ꡣֱ��20����80��������Ŷ�ϸ�����ӵ���ʶ�����룬���RA����Tϸ���鵼�����������Լ������ڴ˻����Ϸ�չ���������Tϸ�������Ʒ�������ȡ����һ������Ч���������ͬʱ���ַ�����һЩ��֧��Tϸ����RA��������Ҫ���õ�֤�ݡ�20���ͺ��ڣ����Ŷ�RA��Ĥϸ������ʶ�����룬���ֳ���ά����Ĥϸ������ת�������ԣ��ɴ����������ߵ������ᵽ����Ҫ��λ�á�
��RA�������Ƶ���ʶ���̣�ʵ����Ҳ�Ƕ�RA������������ʶ���̡��������\������ߣ��о��ֶεIJ��Ϸḻ����21���ͣ�RA�ķ������Ʊؽ�ȡ��ͻ���Եijɹ���
2.��Ĥ��֯���쳣����
(1)��Ĥ��֯�Ľṹ����Ĥ��λ�ڹؽ��ҵ��ڲ㣬��Ϊ��Ĥ�ڲ�ͻ�Ĥ�²㡣��Ĥ�ڲ㣬�ֳƻ�Ĥ����㣬�����������е�ϸ����ɣ������ڻ�Ĥ�뻬Һ֮�䡣�ò���������Ҫ��ϸ�����ͣ�������ϸ��(�ֳ�A�ͻ�Ĥϸ��)�ͳ���ά��ϸ��(�ֳ�B�ͻ�Ĥϸ��)(��7)��
ǰ�����ɹ���ֻ��������������ϸ������������߶ȱ���HLA-DR��������ȱ�������HLA-DR���ӱ�ǡ�����������������������ϸ����������ǰ��ռ20%��30%������ռ70%��80%����Ĥ�ڲ��ϸ��֮��ȱ���������ӣ������뻬Ĥ�²��ϸ����û�л���Ĥ�������ҲΪRA��Ĥϸ���Ĵ��������ṩ�˽ṹ��������Ĥ�²㣬�ֳƻ�Ĥ�����²㣬��Ҫ�ɳ���άϸ����֬��ϸ��������ϸ�����ʴ�ϸ������ԭ��ά�͵�������ɣ��ò㺬�зḻ��Ѫ�ܺ��ܰܣ���Ҫ�Ի�Ĥϸ����Ӫ�����á�
(2)���ʪ�ؽ���Ĥ��֯�ı仯�������˵Ĺؽڻ�Ĥ�ڲ��1��2��ϸ����ɣ���RA���ߵĻ�Ĥ�ڲ�ͨ����4��10��ϸ��(��ʱ��������20��)����Щϸ���������������쳣���࣬�����ڹ����ϴ����쳣��Ծ��״̬�����ǿ��Է��ڴ�����ϸ�����ӡ��źŷ��Ӻ͵���ø�����ٹؽ��ƻ��Ľ��̡����⣬RA��Ĥ�л��д���������ϸ��������Tϸ����Bϸ���͵���ϸ�����Լ�Ѫ���������������ӡ�
�ٻ�Ĥ��ϸ���ı仯������ϸ�����������Ĥϸ����RA��Ĥ�н����Ŵ����ĵ���ϸ������Щ����ϸ�����Թ��裬Ǩ�����ؽں������Ϊ��Ĥ����ϸ����������Ǩ������Ĥ�Ĺ����У�����ϸ��������Դ�Կ�ԭ����������ת�����ؽ�ǻ�ڡ��鳲����(homing receptors)��𤸽���ӱ����ڵ���ϸ������Ƥϸ�����棬��������ϸ������Ƥϸ��ת�ơ��ڹؽ��У�����ϸ�����Խ����������Ŀ�ԭ�ݳʸ�������Tϸ��������Tϸ���Ļ��������Ϊ�����Թؽ��ͷŵ�ϸ�����Ӵ�Դ�Ծ���ϸ��������������������a��IL-1��IL-6�ȣ�������ԶԶ����Tϸ���������ڵ�ϸ�����ӡ�
RA���ߵ����ֻ�Ĥϸ�����������Ե����ӣ������Ծ�����ϸ��(A�ͻ�Ĥϸ��)����Ϊ�������ӵľ�����ϸ��Ҳ���Թ���ĵ���/����ϸ�������Ǿֲ�ϸ����ֳ�Ľ�������о��߹۲쵽��RA�Ļ�Ĥϸ�����������Ե�𤸽������E-ѡ���ء�Ѫ��ϸ��𤸽����(vascular cell adhesion molecule��VCAM-1)��ϸ����𤸽����(intercellular adhesion molecule��ICAM-1)�����Ʋ���Щ𤸽����ͨ������Ƥϸ���������ʹ����/����ϸ�����Ͻ�����뻬Ĥ��֯�����ֻ�Ĥϸ����Ҫ�����ڻ�Ĥ�ڲ�ı��棬�뻬Һ��Ӵ����������ɹؽ�ǻ����м�Ĺ��ܣ�������Щϸ���������MHC���ԭ��Fc���壬�ʿ���Ϊ��Tϸ������õĿ�ԭ�ݳ�ϸ����ͬʱ���������ϸ��һ��Ҳ�ɷ��ڴ�����ϸ�����ӣ�����IL-1��IL-8��������������-����TGF-�µȣ��Դٽ��ؽڵ���֢������Ҫ�����á�
�ڳ���ά����Ĥϸ��������ά����Ĥϸ��(�ֳ�B�ͻ�Ĥϸ��)��Ҫ���Լ���ʣ����ڻ�Ĥ�²㣬�������ǡ����ı��漸�������������Ե�MHC���ԭ��ȱ������ϸ���ı�����������ijЩ��ֳ���ӵ����������ɳ��־ֲ���ֳ�����о���Ϊ������������ϸ��������ϸ�����Ӱ���ѪС����������(platelet-derived growth factor��PDGF)��������������-����IL-1���뻨����ϩ��IJ��ﹲͬ���ôٽ�����ά��Ĥϸ������ֳ�����Ƕ����������һ�����ʣ����ڶ����ⶨRA��Ĥ�ϸ���ķֻ������У�������Щϸ������û�г�����˿�����࣬����ֻ������ϸ����ȡ����������ड��������о���ʾ������ά����Ĥϸ����ֳ����Ҫԭ��������һЩ������أ�
A.����������������Ӧ����-1(early growth response gene-1��egr-1)��c-myc��ras����ֳ��ص�ԭ������ļ����йء�
B.RA��Ĥ�������������ά����Ĥϸ��������ֳϸ���˿�ԭ(proliferating-cell nuclear antigen��PCNA)���о������������ά����Ĥϸ�������ԭ������c-myc�йأ���������ϸ����ֳ������Ҫ�����á�
C.��RA�쳣��ϸ��������ء��ݹ۲죬RA����ά����Ĥϸ����ϸ���������������������洦��ʧ��״̬�����ֵ���ϸ��������Fas��������c-myc��bcl-2��bcl-xl�ȣ�������Ҫ�ĵ���ϸ���������̵�ԭ�������Լ��������ƻ���p53���ʹ��ȱ����������Ч��ϸ������������RA��Ĥϸ������ֳ��
D.��Ĥϸ������ֳ���г���ά����Ĥϸ������ת�����������ر������ܵ���ʴ�Ĺ������ǽ��紦��Ŀǰ��Ϊ��RA�г���ά����Ĥϸ���Ĺ�����������ɻ�Ĥ�������Ҫԭ����ά����Ĥϸ�����Բ���ϸ�����ӡ����ֵ���ø���Թ���������֯�����ʴ������Ϊ�ǽ鵼RA�ؽ��ƻ�����Ҫϸ����
��Tϸ������RA�Ļ�Ĥ��Tϸ��ռ30%��50%�����ǿ��Ծۼ���Ѫ����Χ�γɵ��ܰ��������ṹ�У�Ҳ���Է�ɢ��Ѫ����Χ�Ļ�Ĥ��֯�С�������RA��Ĥ��֯��Tϸ����ҪΪCD4 ������Tϸ��(CD45RO )���ɸ߶ȱ���IL-2�����MHC���ԭ�Լ�𤸽���ӡ���������о�����RA��Ĥ��֯�е�Tϸ��ΪTh1ϸ������RA��Ĥ�н����Tϸ��ֻ������ΪCD8 Tϸ����
Tϸ������ν��뻬Ĥ��֯��?�о���������Tϸ��𤸽��������й����У�𤸽���ӡ�ϸ�����Ӻ���������������Ҫ���á�Tϸ�������L-ѡ��������Ƥϸ�����ǻ���-������ϸ��𤸽����-1(GlyCAM-1)��ϣ������ߵ������ϵ͡�����T�ܰ�ϸ����Ѫ���ڻ����ƶ����ɾ���ϸ��������������������-����IL-1��ϸ�������յ�Tϸ�����������ڼ������ÿ�ԭ(very late activation antigen��VLA)���ܰ�ϸ��������ؿ�ԭ(lymphocytic function-associated antigen��L
FA)��𤸽���ӣ���Tϸ��������ͬ�̶ȵ��������á��˺�ͨ����Ƥϸ����Ѫ��ϸ��𤸽����-1(VCAM-1)��Tϸ������VLA-4�������ʹTϸ������Ƥϸ������𤸽������Ƥϸ����ϸ����𤸽����(ICAM-1)��ͨ����Tϸ�������L
FA-1��ϴ�ʹTϸ���Ƴ�Ѫ���⡣��Ƥϸ����𤸽����������ѭ����Tϸ��������Ӧ��𤸽�����ԡ�����-���塱�ķ�ʽ��ϣ�ʹ֮𤸽����Ƥϸ����������Ѫ���⡣����֢��Ӧ��Ļ�Ĥϸ��ͬʱҲ����IL-8��RANTES���������ӣ������ǵ�������Tϸ����Ĥ��֢��Ӧ��λ���С��ɴ˿��Կ�����Tϸ�������ڻ�Ĥ��֯��һ�����Ƿǿ�ԭ�����Եģ����ڷǿ�ԭ�����Եľֲ���ֳ������ϸ��𤸽�����ڻ���Ĥ��֯�ı�������������ϸ���ƶ����������ڻ�Ĥ��֯���������أ�����ʹ�û�Ĥ��֯��������֢��Ӧ����������
��Bϸ����RA�Ļ�Ĥ��֯��Bϸ�����������٣�ռ��Ĥ����ϸ���IJ���5%����Ҫ�������������ṹ�У���������Χ���Կ�����ϸ���;���ϸ���������е��������ṹ�γ���������(germinal centre)��˵���ؽ��д����ܰ���֯���ṹ�����������ǿ�ԭ�����Bϸ����չ��Ϊ������Bϸ���ͽ�ϸ����������Ҳ����Һ���߷�Ӧ�������Գ���(affinity maturation)�IJ�λ��ͨ�������ʴ�RA���߱����Ļ�Ĥ��֯�п���ֱ�ӷ���õ���ֳ��Bϸ�����о����������������Ļ��Bϸ����������Tϸ��(dependent-T cell)����ʽ�շ���¡��ֳ�ġ����������Ļ���һ������״��ͻ״ϸ��(follicular dendritic cells��FDC)������һ�ָ߶������ԵĿ�ԭ�ݳ�ϸ�����������Ա��ﲹ�������Fc���壬��RA��Ĥ��Bϸ����Ӧ�����Գ�������Ҫ�����á���Щ����״��ͻ״ϸ��������Bϸ����¡����ֳ���γɡ�
����ͻ״ϸ����������Ĥ��֯����ͻ״ϸ��(dendritic cell��DC)����RA��Ĥ�ͻ�Һ�к��зḻ����ͻ״ϸ������Щ��ͻ״ϸ����������ѭ���в������ǰ�塣���о��Ʋ⣬��Ĥ��֯�г������������ˡ���Ⱦ��������ֲ����߸������γɵȷ���������֢��Ӧ����Щ�̼����»�Ĥ�����ľ���ϸ���ͷ�ϸ�����ӡ���GM-CSF�������������Ӧ���IL-1��ϸ�����ӵ������£�DC�ڻ�Ĥ��֯�е��Էֻ��ͳ��졣�ڳ���Ĺ����У�DC����MHC������Ӻʹ̼�Tϸ���ĸ�������(coreceptors)���о���ʾ������ͻ״ϸ�����ڵ�����£��������ij���ԭ������Ч�ش̼�Tϸ���������߷�Ӧ��
������ϸ�������ܻ�ĤҺ����������ϸ���dz��ḻ���������ڻ�Ĥ��֯�е������dz����ޡ���Ȼɱ��ϸ��(natural killer��NK)Ҳ���ڻ�Ĥ���ҵ��������Դ̼�Bϸ������RF��
(3)��Ĥ��֯�е�ϸ�����ӣ�
��ϸ��������RA��Ĥ���������ź������á�ϸ������ϵͳͨ�������ڶ���ϸ����������γ�һ�����ӵ����硣��RA�Ļ�Ĥ�У�����T�ܰ�ϸ�����Է��ڶ���ϸ�����ӣ���IL-2��IFN-�á�IL-4�ȣ����Ҿ�������Ĥϸ���ͳ���ά����Ĥϸ��Ҳ�ɷ��ڶ���ϸ�����ӣ�����������������-����IL-1��IL-12��IL-6��IL-15�ȡ���֮����Щϸ�����ӻ�̼�����������ϸ����һ������ϸ�����ӡ�
Ŀǰ��RAϸ�����ӵ��о����֣�RA��Ĥϸ��������ϸ�����ӳ��ȶ��������ı����������������������ʿɴ̼���Ĥϸ������ϸ�����ӣ����ң�ϸ�����ӱ���Ҳ�Dz���ϸ������ǿ�����Ĵ̼����ӡ���Tϸ��������Ӧ���µ���Ĥ�еľ���ϸ���ͻ�Ĥ����άϸ�����Է��ڻ��Է��ڷ�ʽ������ϸ������ʹ��֢��Ӧ�������������⣬�ڻ�Ĥ��Һ�пɼ�����ϸ�����ӣ����Dz����ܹ����ͻ�Ĥ�����ϸ��������ԭ�����ܹ��յ�HLA-DR��𤸽���ӵı���Լ���ĤѪ�ܵ��γɡ�
RA��Ĥ����֢��Ӧ�漰��ϸ����������dz��ࡣ�о�����������������-����IL-1��RA�ķ��������ż���ؼ������á�������ϸ�����Ӵ̼���Ĥ����άϸ������������IL-6��GM-GSF�����������Լ����ʵ���ø��ǰ�����ص�ЧӦ���ӡ����У�GM-CSF���ɻ�Ĥ������ϸ���ͳ���άϸ����ͬ���ڵģ������������յ�IL-1�ķ��ڲ��γ�һ���������������һ�����������������-����ͬ�����ھ���ϸ������HLA-DR�ı�����⣬�ɾ���ϸ���ͳ���άϸ�����ڵ�ϸ�����ӻ����Լ�������ھֲ�Tϸ����Bϸ���Ļ�����а���RF�IJ�����
������������-����Ҫ�ɻ�Ĥ�����Ļ�Ĥ����ϸ����������֤ʵ������������-�����õİ�Ŀ����ijЩ��������������-���ɷ�(�������������������-�������)��Ӱ��������������-�����������ذ������߸��������Ļ��ϸ������ʳɷֺ;ֲ�ϸ�����ӵı�������ر�Ҫ�ᵽ�ֲ�ϸ�����ӵı���������о��������ɻ�Ĥϸ�����ڵ�IL-15�������Դ�ʹTϸ������λ����Լ��������ӵIJ�������������������������-���IJ������о���ʾ��������RA��Ĥ�ڼ���IL-15��mRNA�͵��ף����ң�������ʵ��۲쵽������IL-15�������ֱ�Ӽ��ٻ�Ĥ����ϸ������������������-��������ͨ����IL-1��IL-6�Լ�������������-����ͬ�ٽ�Tϸ��/����ϸ���������á�
���о�������������������-������Ϊ�ǻ�Ĥ��֢��Ӧ�Ĺؼ���ϸ�����ӣ����ܵ�֤���ǣ�
A.������������-�����������ֱ�ӻ��Ӳ���RA���ֲ������̣���������ϸ���ľۼ��ͼ����Ĥϸ������ֳ���յ�����ά��Ĥϸ�������Ǻ������ƻ���ϸ�����Ӻ͵���ø���̼�����ϸ����������ϸ�����ӵ�(ͼ3)��
B.��RA��Ĥ��֯��������������-����������������-�������������ߡ�
C.�����⣬��������������-�������IL-1��������ǰ����ϸ�����ӵIJ������������á�
D.���ֱ���������������-����ת����С�������ʴ�Թؽ��ף�����֯ѧ�ص���RA���ơ�
E.�ؽ��Ķ���ģ��֤ʵ����������������-�����ʿ��Լ��Ს��̶ȡ�
F.��RA�迹������������-�����ƿ��Բ����Ϻõ��ٴ�Ч����������о���ʾ����Ȼ���迹������������-�����ƿ�����Ч�ؿ��Ʋ��飬��һ��ͣҩ���������������ҿ�������������-�����Ʋ����Ƕ����еĻ��߶���Ч����ˣ����о��߹۲쵽��RA�������ڵĻ�Ĥ��֢�������ɲ���������������-�����Է��ڷ���������ɵģ�����������Ҫ���صIJ��롣��ˣ������о���Ҫ��һ��̽��������������-������֢ϸ���������Ƿ���ж��صĵ�λ�����⡣
IL-1Ҳ�ǻ�Ĥ��֢��Ӧ�Ĺؼ���ϸ�����ӡ���RA��Ĥ�У���Ҳ���ɻ�Ĥ����ϸ�������ġ��������ؿ����յ�IL-1�IJ��������磬������Fc�Ρ����߸������ԭƬ���Լ�Tϸ�����źŷ��ӵȡ��ڻ�Ĥ�У�IL-1�����յ�����άϸ�����������̼���Ĥϸ���ϳ�IL-6��GM-CSF���������ӳ���άϸ��������ԭø�����⣬�������Դ̼���Ĥϸ��������ϸ�������Ļ�ϸ���������øԭ������Ļ��ԡ�����֤����IL-1����һ�ִ̼��������յ��ƹ�ϸ���Ļ���ӡ�IL-1���ɴ̼���Ƥϸ������𤸽���ӣ�����VCAM-1��ICAM-1��RA�Ķ���ģ����ʾIL-1�ǵ��ڹ��������ƻ�����Ҫ��ϸ�����ӡ�
��T�ܰ�ϸ����ΪRA��Ĥ����������һ������ϸ�������ڻ�Һ�У������ܼ�T�ܰ�ϸ�����ڵ�ϸ�����ӣ����Ҽ����ķ����ͷ�չ���������Tϸ�����ڵ�ϸ�����ӷ����仯�����磬������RA���ڻ��ǻ��IFN-���ڹؽ��ڱ���������������䡣ΪʲôRA��Ĥ��T�ܰ�ϸ�����ڵ�ϸ�������������֮����?����������һЩԭ��
A.ϸ�������ܵ��ֲ����������Tϸ������Ӧ�������½���ԭ��֮һ�����磬��RA��Һ�пɼ�IL-1��������(IL-1Ra)��TGF-��������Tϸ�������Ƽ������⣬��Һ��ijЩ�������Գɷ���hualuronate��Ҳ���Լ������Tϸ���Ļ��ԡ���RA����Ĥ��֯�������У��ɾ���ϸ�����ڵ�������������-�����ɻ�Ĥ��֯ϸ�����ڵ�IL-10�����µ�T�ܰ�ϸ���Ĺ��ܡ�
B.��Tϸ������(TCR)�ź��쳣��ء��ر��Ǿ�p38��˿����ԭ��ĵ���ø(MAPK)�ź�ת��;���Ĵ̼�����Һ��Tϸ�����Լ����Ұ�������ữ�����ң�TCR�������Ұ������ữҲ�����쳣���о�����TCR������ˮƽ�½��������RA����TCRװ���쳣��
C.��Tϸ�����ܵ����Ƽ�����ȱ���йء�����ʵ��۲쵽��RA��IFN-�õIJ��������ܵ����ƣ����ǣ�������������������������ɱ����������о���ʾ��Tϸ������IFN-�õļ�������ΪRAϸ����PGE��Ӧ�����������ӡ�����ʵ��֤��������RA��������Ѫ��Tϸ������IL-2���٣����������������������������Ҳ�ɵõ����ָı䣬��Ҳ��һ��˵��RA���˶�PGE�и��ߵ������ԡ�
D.��������Щϸ�������ڻ�Ĥ����������ʽ������ά�ּ��������仯�ij������С�������RA��Һ��Tϸ�����ڵ�IFN-�����ú���Ҫ������MHC���ԭ����Ч���յ��������Լ���˾���ϸ���������յ�VCAM-1��ICAM-1��𤸽��������Ƥϸ���ı�������ܹ�Э����ļ����ϸ�������˲�λ�ۼ�������һ����Ҫ�����þ���IFN-�ÿ��Ըı�ϸ������ʵĺϳ��뽵��֮���ƽ�⡣��֮��Ŀǰ��Tϸ�����ڵ�ϸ��������ȷ�Ĺ��ܻ�֪֮���١�
����RA��Ĥ��֢��Ӧ�Ĺ����У���Ĥ�ڵ�ϸ�����ͷŸ��־��п���֢��ϸ�����ӣ�����IL-1�����������������������������-�� p75��p55���塢������IL-1���塢IL-16��IL-11��IL-13��IL-10�ȡ���RA��֢��Ӧ�ĵ��ڹ����У���Щ����֢ϸ�����ӵı���Ҳ�������ӣ����Բ��������ƹؽڻ�Ĥ��֢�ķ������о����֣�ϸ����������Ŀ���������������������p55��p75���ڹؽڻ�ĤҺ�пɼ����������壬����Ũ�Ȳ������кؽڻ�ĤҺ�в�������Դ�������������ӣ�������ƣ�IL-1����������IL-1����Ȼ���Ƽ���������RA����ĤҺ�б����ˮƽҲ�ϸߣ�ͬ��Ҳ����������IL-1������������á�Ŀǰ���о���Ϊ������֢��ϸ�����ӺͿ�����ϸ������֮�����õ�ʧ��ʹϸ�����ӵ����ȶ���ƻ�������RA��������Ҫ������������Щϸ���������ɶ�RA�����ƺ��м�ֵ�������������û������鼼�������Ƴ�����ϸ�����ӵ���������ȡ��������������ٴ���Ч��
(4)��Ĥ���źŷ��ӵ����ã�ͨ�����ִ̼���ϸ�����ź�ת��ϵͳ��ϸ��������������ϸ�����ź�ת����ڣ����ڴ�����ת¼���ӵ�ˮƽ��ת¼���ӽ�������DNAλ�㣬����ijЩ�ʵ�����ı��RA��Ĥ��֯���쳣��������֢��Ӧ��أ�Խ��Խ���֤�ݱ����ж���ת¼���Ӳ�������һ���̡������Ӧ�B(nuclear factor-��B��NF-��B)���������ӵ���-1(activator protein-1��AP-1)�ͷ����ؼ���ĵ���ø(mitogen-activated protein kinase��MAPK)����Ϊ��RA������Ҫ�����á�
�ٺ�����-��B��NF-��B��һ���ձ���ڵ�ת¼���ӣ���RA����ת¼������ʮ�ֹ㷺����Ҫ�����ã������ڵ������絥��ϸ����IL-1�£���Ƥϸ����E-ѡ���ء�VCAM-1��JCAM-1���Լ���Ĥϸ����������������-����IL-6��MMP-1����֢������Ҳ��������Ҫ�����á����͵�NF-��B����p50(NF-��Bl)��p65(RelA)��ɵĶ����壬��������p52(NF-��B2)��Re1B��c-Rel�ȳɷ֡�
���ֲ�ͬ���źſ��Լ���NF-��B�����磬������������-����IL-1�����ӻ����ߡ�֬���Ǻ������⡣�ڰ�����NF-��B�뱻����NF-��B���Ƽ�(I��B)�������Ե�������������״̬����I��B�����л���I��Ba��I��B�º�I��B�ţ�����ͨ���ڸǰ��˶�λ�ź��Ե���DNA�Ľ�Ϻ���ϸ��NF-��B���Ķ�λ������Ĵ̼��������źż�����Ӧ������������I��B��ø(IKKs������IKK-1��IKK-2)�Ļ�������ּ�ø������I��B�����˵�˿����л����ữ����һ����ʹNF-��B��λ��ϸ���ˣ��ڴ������Խ�ϰл�������ת¼��
NF-��B��RA��Ĥ�еĺ���ʮ�ַḻ�������黯����֤�����ڻ�Ĥ������Ѫ����Ƥ��ϸ�����д���p50��p65 NF-��B���ס�ʵ���ϣ�NF-��B�鵼�������Ծ���ϸ������֢���ʵı������������������-�������⣬�ڹǹؽ��Ļ�Ĥ��Ҳ��NF-��B�ı��������������û�С��������ݵ�ӾǨ�Ʒ���(electromobility shift assays)��NF-��B��RA��Ĥ�еĻ��Ա���OA��Ĥ�е�ǿ��
��IKK�����������������-����IL-1��ϸ�����ӵĴ̼�����������RA����ά����Ĥϸ���кܿ췢��NF-��B�������λ������I��B��ø(IKKs)�ڻ�Ĥϸ���гʽṹ�Ա�����ǵĹ�����������������-����IL-1�յ�������IKK-2�ǻ�Ĥϸ����ϸ�����Ӵ̼���NF-��B�����Ҫ;����
����
�ٲ�����Ⱦ�ķ���ʹ������RA��Ĥ����I��B�����ȱ���������������������� ����IL-1��IL-6�IJ�����������ͨ���յ��Ѻ������ø���Ƽ�������NF-��B�Ļ��ԣ����Լ�����������Թؽ�����֢����Щ����˵�������NF-��B��ά��RA��Ĥ����������������-������Ҫ���أ����������ڽ�NF-��B����Ϊ��Ŀ�����������ÿ�����Ч��������֢��
�ڹؽ��Ķ���ģ����Ҳ���Թ۲쵽NF-��B��������ӡ����統���ߴ�����������Թؽ���3���NF-��B�������们Ĥϸ���ڳ��ֻ�����ữI��B�����Ƽ��������ƹؽ����ٴ����֡���С��ԭ�Թؽ����У��������1�����ߺ�10���ڷ�����ĤNF-��B�Ļ������ٴ����ֹؽ���ʱ������ܶࡣ���⣬�������ϸ���ڳɷ��յ��Ĺؽ��ף���Ĥ��֯�е�NF-��BҲ�ɱ���������������NF-��B�Ļ��ԣ��������������������Ӧ���Fas�鵼�Ļ�Ĥϸ���ĵ���(��һС�ڻ���ϸ����)���ؽ���NF-��B�Ļ���Ա���ϸ���������������Ӷ����»�Ĥ��֯�Ĺ�����ֳ��
��AP-1����NF-��Bһ����AP-1Ҳ�����ڵ��ڶ���������RA�Ļ����������������Ӧ��ͽ�������ø��ϸ�����ӡ��������ӡ�������������Rasԭ�����ȣ�ϸ�����źſ����յ�AP-1���AP-1����Jun��Fos����ת¼���Ӽ��壬���Ǿ߱�����������DNA��Ͻṹ��AP-1������Junͬ�Ͷ������Jun-Fos�Ӷ��������ʽ��DNA��ϣ�������ת¼���ڲ�ͬ���͵�ϸ���б������Jun��Fos�����Ա����c-Jun��JunB��JunD��c-Fos��FosB��Fra-1��Fra-2�ȡ����ǽ鵼���غ��ص������ת¼��
�����黯���о�֤������RA��Ĥ����AP-1���߷�Ӧ�Գɷֵı���ر����ڻ�Ĥ�����ij���ά����Ĥϸ���С��ڻ�Ĥ�²���������ϸ��Ҳ����c-Jun��c-Fos��ֻ���������١���������Ĥ��֯�У���δ��AP-1������OA���˵Ļ�Ĥ��Ҳ��AP-1����������NF-��Bһ�������ݵ�ӾǨ�Ʒ���(electromobility shift assays)��AP-1��RA��Ĥ�еĻ��Ա���OA��Ĥ�е�ǿ����RA��Ĥ�У�AP-1�Ļ����п�����RA��Ĥϸ����¶��IL-l��������������-���ȶ������Խ����йء�
������ʾ��������RA��Ĥ����άϸ����������ϸ���������ھ�ֹ�ڣ�AP-1�Ļ���ˮƽ�ܵͣ����ҽ��������������Jun��fos�����ǵ�����IL-1��������������-���̼���c-Jun��c-Fos mRNA�ĺϳ��ϵ���AP-1�Ļ����Լ���ԭø����ת¼ˮƽ�������ߡ�������ȷ���ڻ�Ĥϸ���й���AP-1�����Jun�������Ĺ��ܣ�����c-Jun��������֢���ʵIJ�������JunD�������ϸ�����Ӻͽ�������ø�IJ�����
����˿����ԭ��ĵ���ø����3����Ҫ����˿����ԭ��ĵ���ø(MAPK)��Ϊ�����ź�ת��ø������ϸ�����źŵ��ڼ�ø(extracellular signal-regulated kinase��ERK)��JunN�˼�ø(JunN-terminal kinase��JNK)��p38��������Ҫ����c-Jun�����ữ�Լ�ϸ�����ӵIJ�����ERK��Ҫ����Ras;��ͨ��������ʹϸ�����Ӻ��������ӵ��Ի��JNK��p38������IL-l�������������Ӧ���ϸ�����ӵĴ̼��²������ԣ���Ҫͨ�����ݵر�¶��IL-1֮�����ữ�������ԡ�JNK��AP-1�ĵ����зdz���Ҫ����Ϊ�������ữc-Jun����Ҫ��ø���塣JNK����JNKl��JNK2��JNK3 3��ͬ���͡�����JNK2��RA��Ĥϸ���гʽṹ�Ա��JNK2��c-Jun��ϲ���������������JNK1��25�������JNK2����Ϊ�������ά����Ĥϸ����AP-1��صļ�������ͨ��JNKs������c-Jun N�����ữ���ٿɽ�c-Junת¼��ˮƽ���30���������о�֤ʵ�����ó�JNK1��JNK2��С���У�JNK�Խ�������ø�ı����к���Ҫ�����á�
(5)��Ĥ��ϸ�����������ã������꣬��������ʶ��ϸ��������RA�����е����á�ϸ��������ϸ��������������һ�֡�ϸ������������������������£����ڸ��巢������ϸ���������ƽ��ͼ�������������Ҫ���õ�һ��ϸ��������ʽ����Ĥϸ���Ĵ�����ֳ����֢ϸ����������RA�ĵ���������Ŀǰ���о���Ϊ����ϸ������(��ֳ/����)��ʧ���йء�
���������ױ�����ʾ������DNA��Ӿ������������TUNEL(DNAnick-end labeling)��������Ĥ��֯�д��ڵ���ϸ�������������ֵ���ϸ���������٣�����Ҫ��������λ�ھ���ϸ����Χ��һ�����ֺܿ�ͱ�����ϸ���������Ŀǰʶ���3����ϸ��������ص����壬������Fas��ԭ(CD95)�Լ��������������������壬���߷ֱ���55kD��������������-R���75kD��������������-R������Fas��ԭ��һ��45kDϸ�����浰�ף��������͵�ϸ���������Ĥϸ���������塣���Ƕ�����������������/����������������壬�������ϸ���������������Fas����(Fas-ligand��Fas-L)��40kD����תĤ�����ʣ���Ҫ�����ڻ��Tϸ�����档�����յ�����B��T�ܰ�ϸ��������ϸ������������ϸ�����а�ϸ���ĵ�����
RA��Һ�л��Tϸ��������������Fas���ӡ�Fas��Fas-L������ã��ܹ�����ϸ����������IL-1�º�������������-��ռ�ݸ���ϸ�����������ʱ������Ҳ��ͨ�����ֻ�������ϸ�����������о����֣�RA��Ĥ��֯�Ⱥ���Fas �Ļ�Ĥϸ���͵���ϸ����Ҳ���б���Fas-L�Ļ���Tϸ������Ȼɱ��ϸ������ˣ���RA��Ĥ�У�ͨ��Fas/Fas-L������ü�������鵼�Ļ�Ĥϸ������������ϸ����������ؼ������á�����Fas-L��Tϸ������Ȼɱ��ϸ���뻬Ĥϸ���͵���ϸ�����������Fas����ã�Ҳ����RAϸ����ֳ����Ȼ��������һ�����á���֮����RAϸ����ֳ�Σ�Fas/Fas-L��������п����ܵ��������ص�Ӱ����ƻ���ϸ���ڵĵ���Bcl-2���������ƻ���ǿϸ�����������á�CD4 CD28-Tϸ��Bcl-2�ı������ӿ�ʹϸ�������ܵ����ƣ������ɻ�Ĥ��֯��������Ӧ��ϸ���Ŀ�¡��ֳ��
�������������RA�Ļ�Ĥϸ������Fas���ӣ����ҹǹؽ��Ļ�Ĥϸ������Ҳ����Fas�����ǣ���Fas��������յ�RA��Ĥϸ�����ֵ����������յ�OA���ֵ���������Fas�̼�ijЩϸ�����Գ�����ֳ�������ǵ�������˵��Fas������ͨ���������ص��ڻ�Ĥϸ������ֳ���������Щ���ذ���ϸ�����ź�ת��;���Ϳ��������ӡ��������о�������NF-��B��AP-1��MAP��ø���ź�ת��;����������һ���̡���������Ϊ������RA��Ĥϸ����Fas��������������-���鵼���ź�;���dz���Ҫ����Щ�����ܼ������źŷ�����ת¼����NF-��B���ɴ��յ��������ƻ���Bcl-xL��Survivin�ı���̼���Ĥϸ������ֳ�������Ƴ���άϸ���ĵ��������о�������Fas������NF-��B�������Խ鵼��JNK(����MAP��ø)/AP-1�յ��ĵ�������������������-�������NF-��B�ڻ�Ĥϸ����ֳ�ĵ�����������Ҫ�����á������Ϊ��NF-��B�ĵ��������ڻ�Ĥϸ������ֳ���յ�������ȷ��涼�к���Ҫ�����á�
����һ�����ض�ϸ����������Ӱ�죬���������ƻ���p53�����⣬������ϸ�����ڡ�DNA���ơ�ϸ���ֻ���DNA������Ҫ�ĵ��ڼ�����Ȼp53��������ԭ������������c-myc��ԭ�������ת¼�����£�Ϊ�յ�ϸ������ͣ�ͺ�ϸ�������ṩ����Ҫ���źš�������Ӧ���������£��������ͻ��Ե��IJ������ӣ����DNA�����ˣ�ʹp53ˮƽ���ߡ�������p53�����յ�ϸ������ͣ�͡�DNA����ϸ������������ͻ���p53�ɳ������DNA�����ˣ�����ϸ��ת����������ϸ���������о����֣���RA�Ļ�Ĥ�����ͳ����²㷢��ͻ���p53���������ı����������ߡ�����Ϊ��p53��RA��Ĥϸ������ֳҲ��һ�������á�
��֮����RA���ںܶ�����ϸ�����������أ���Ҳ��������Ĥϸ����ֳ����֢ϸ���������Ҫ���ء�
(6)������Ѫ�ܣ�Ŀǰ����ʶ��������Ѫ������֢��Ӧ���������ż�Ϊ���������á�������������Ϊ����ѡ��ϸ��������֢��֯��һ���ֶΣ����һ��Ǵٽ���֯�����Ͳ�����֯Ӫ���ľ������ء�
��RA��Ĥ��֯�п��Կ�������������Ѫ�ܣ�������������֯�ʹ���������֯���������ġ��ڶ�����ǰ�������о��߷�������һ����ָ��������Ѫ���ڻ�Ĥ��֢��չ�����е���Ҫ�ԡ��˺��ڽ�ԭ�Թؽ��Ķ���ģ����֤ʵ����һ���ۡ������о���������������֢������Ѫ�ܵ��γɣ���ô���Ի���RA�IJ��鷢չ����ˣ�RA��������Ѫ������֢�����ͷ�չ�����еĻ�����������Ϊ��ЩѪ�ܲ�������������ļ����ϸ��������Ϊ��ֳ�Ļ�Ĥ��֯�ṩӪ�����ʡ�
RA��Ĥ������Ѫ�������������ӣ���ҪΪëϸѪ�ܼ�����״��Ƥ��ëϸѪ�ܺ����������߳�λ���ܰ��������ġ�ϸ���������ɳںͻ���Ĥ�IJ�����״̬�������Ѫ�ܵ�ͨ�����ߣ�Ϊ������֢��Ӧ�ijɷֳ������벡����֯�ṩ�˽ṹ������������ά�ֲ��ٽ���֢��Ӧ�Ľ��С�
��Ĥ�ױ���Ϊ�����Ļ�Ĥ��֯��ֳ����Ȼ����������Ѫ���γɣ����ӻ�Ĥ��֯��λ����ķ����ϣ���������Ѫ�ܵ�����ԶԶ�������㻬Ĥ����Ҫ�����ң��о���ʾRA��Ĥ�ĺ�������������20�������־��Ʊ�Ȼ��ɾֲ���Ĥ��֯����ȱѪȱ�������⣬������֢�ķ�չ���ؽ�ǻ�ڻ�Һ�����࣬ǻ��ѹ��Ҳ��֮���ߣ��������Ѫ����������Ĥ��֯ȱ����
��Ĥ��֯�ĵ���״̬��Ѫ���γ���Ч�Ĵ̼����ء�����Ѫ���γɵĻ���֮һ���Dz�������Ѫ����Ƥ��������(vascular endothelial growth factor��VEGF)��Ѫ���γ����ӡ�VEGF����ǿ�ֲ�Ѫ�ܵ�ͨ�ԣ��̼���Ƥϸ��������˿���ѣ���һ�������ԵĴ���Ƥϸ���������ӣ�ͬʱ����ijЩ���������ԡ�������RA����ؽڵĻ�Һ�п��Լ���Ũ�ȵ�VEGF�������ڻ�Ĥ��֯��Ѫ���ڼ�����ΧҲ�ɼ������⣬VEGF������Ҳ����������ͬһ�����ڡ�VEGF�ڻ�Ĥ�����ʸ߱�������ij���ά����Ĥϸ����¶�ڵ�����������IL-1���ڵ������£�Ҳ���Բ���VEGF��
���˵���״̬�ܹ��̼�RA��Ĥ����Ѫ���γ��⣬����IL-8������άϸ����������(fibroblast growth factor��FGF)��������������-�������ڵ�����ϸ�����Ӿ���֤���ܴ̼��Ͳ���Ѫ���������̡�����һЩѪ���γ����Ӱ���������E-ѡ���غͿ�����VCAM��Ҳ�̼�����Ѫ�ܵ��γɡ�
3.�������ߵ��쳣
(1)Tϸ�������ʪ�ؽ����е����ã�
�й�Tϸ����RA�����������õļ�˵����ʮ������Χ��Tϸ����RA�������Ƶ�������������ּ�˵������������о�����ͬ�ģ�����ΪRA�����Ŵ��ͻ������ص���������T�ܰ�ϸ���鵼�����������Լ�������Ϊ�кܶ�֤�ݱ���Tϸ����RA������������Ҫ�����ã�
��RA��Ĥ��֯�н����ϸ���Ե���ϸ��Ϊ��������30%��50%��T�ܰ�ϸ����
����ЩTϸ���ľ��ֱ�����Ƿ��ӡ�
�����Tϸ�����������ƶ�RA��һ������Ч�������Ʒ���Ҫ�ܹ���������������Tϸ���Ļ��ԡ����磬��ȫ���ܰͷ��ƻ�����A���ƿ���ʹ����õ����⡣
���ڽ�ԭ�Թؽ��������Թؽ��ȶ���ؽ���ģ���У�������Ӧ��Tϸ������ʹ����������ּ�����ת�ơ�����������һЩ��Ҫ��������δ�����������
A.��ĤT�ܰ�ϸ���Ƿ��Dz��̽�չ���շ����ӡ�
B.Tϸ������Ĥ�Ƿ��ǹؽ�����֢��Ӧ�Ľ����
C.����Tϸ�����������ԭ��δ�ҵ���
�����������һ���µļ�˵�����ڼ�����չ�����У����������������ܻ��Ƶ��쳣���ܰ�ϸ�����쳣��ֳ��Tϸ���ڻ�����̬��ʧ�⡣�о�������ʾ����RA�У�Tϸ�����ߵ�ʧ����������������֢��Ӧ�IJ�λ����ȷ�е�˵����Tϸ���������ܳ���ȱ�ݵĻ����ϣ���Ĥ�γɾ��������ƻ��Ե��ܰ���֯���Զ���ģ�͵��о���ʾ����Щ������Ӧ��Tϸ������ֳԴ�Ե����ܰ�ϸ����ֳ��Tϸ���ڻ�����̬�Ļ��Ƴ����쳣��
(2)RA��Ĥ��Tϸ�����ص㣺RA��Ĥ�е�CD4 Tϸ��������һЩ��Ҫ���ص㣺
�ٱ���CD45RO��ͬ���ͣ�ʹ���Ǿ��м���ϸ�����ص㣬�������뿹ԭ�Ӵ�������Ĥ��naive Tϸ�������dz��١���������棬��Ĥ�������ܰͽ����Χ�ܰ���֯��ͬ��
�ڻ�ĤCD4 Tϸ������CD69��������һ�����ڻ�ı�־���ӡ�RA���ߵ�����ѪTϸ�����ٱ���������ӡ������ױ�������ĤTϸ�������CD69�뼲�������س̶���أ���Ҳ��ʾCD69 Tϸ���ڼ����е����á�
��������ȷ��ֻ���������źŵIJ����¿�ԭ�̼���Tϸ�����ܻ�����Ļ��ԣ��������źŷֱ���TCR-��-MHC������̼�����(co-stimulatory molecule)�����߰���Tϸ����������CD28��CTLA-4�Լ�APC��������B7-1(CD80)��B7-2(CD86)��RA��Ĥ�ڵ�Tϸ��Ҳ����CD28��CTLA-4�������ڹؽ��ڵ�APCҲ�ɼ�������B7��CD80��CD86��CD28��CT-LA-4��ϣ���Ҫ���븨���̼�Tϸ���Ļ������Tϸ������ֳ�Լ�IL-2�ķ��ڡ���������RAѪҺ�ؽ��ڼ�CD28-Tϸ������Щϸ������������ԭ����Ӧ�𣬶��ҿ����������ܵ��������ܡ��������о�������CTLA-4����Tϸ���Ļ�����ϵ������Դ��������źŶ��µ�Tϸ������ֳ��CD40����һ�ֹ��̼����ӣ������ڶ�������ϸ���ı��棬����Bϸ��������ϸ��/����ϸ������Ƥϸ���ͳ���ά����Ĥϸ����CD40�����屻��Ϊgp39��CD40L��CD154��λ���л��Ե�Tϸ�����档��RA��Ĥ�пɼ�CD40��������CD40L���ر�����IFN-�ô��ڵ�����£�CD40��������֮��ķ�Ӧ���Ը����̼�Tϸ���Ļ���ϵ�𤸽���ӡ�����ϸ�����Ӻ��������ӡ�ͬ��������ת���Լ�����һ��������CD40�����廹�����յ�����ϸ���Ļ����ͻ״ϸ���ķֻ���������Щ����Ӱ��RA�ķ�չ�����ȱ����Щ���̼����ӣ�Tϸ�������ᱻ�����ᵼ�¿�ԭʶ�����������(tolerance)��
�ܾۼ��ڻ�Ĥ�ļ�����Tϸ���ڹ�������һ����ȱ�ݡ���ĤTϸ������ı�����ʾϸ�����������쳣(�ʵ�Bcl-2��Bax��Fas����ı���)�����ң���ĤTϸ���������ʺܵ͡��෴���������Щ��Ĥ�е�Tϸ������������������ʲ����ߡ����˵����Ĥ����ͨ��ijЩ����Ĺ�������ϸ�������ʹٽ�ϸ�����(��8)��
(3)RA��Tϸ�������ã�Ŀǰ��Ϊ��Tϸ���ڼ������������ŷdz���Ҫ�����á��������һ������Խ���Tϸ���������RA�������õġ����ȣ�naive Tϸ���뿪���ٺ�������ѭ���б�������ǵı����������������ǿ����Ƥϸ��𤸽�������������벡��Ĺؽ��ڡ����û�г����Ŀ�ԭ��Ϊ�̼���Tϸ����������IL-2���彫���٣�һ����Tϸ��ת��Ϊ������Tϸ�������ؽ���һС���ֵļ�����Tϸ��ʶ��������ڿ�ԭ�ݳ�ϸ��(APC)������MHC���ӽ�ϵĿ�ԭ��֮��Tϸ����������л�Ĥϸ��������ϸ������ͻ״ϸ����Bϸ����APC���涼��Я��MHC������ӣ���MHC������ӿ�����ij�ֿ�ԭ�����ϣ���ͨ��APC�ݳʸ�Tϸ������Tϸ�������TCR��ϡ���Щ�����ڻ�Ĥ��֯��T�ܰ�ϸ����ͨ���뿹ԭ�ݳ�ϸ���ϵġ�δ֪��ԭ�����ϣ�����һϵ��������֢��Ӧ��������IFN-�á�IL-17��IL-2�ȶ���ϸ�����ӡ�
��ǰ���������ݹ�ѧ�����������黯���о���ʾ��������RA��Ĥ��֯��Tϸ����ҪΪCD4 ������Tϸ��(CD45RO )��CD4 T����ϸ���ֿɸ������Ƿ���ϸ�����ӵ������Ϊ�������ͣ���Th1��Th2��ǰ�߿ɲ�������IFN-�á�IL-2��IL-17�����ڵĴ���֢��ϸ�����ӣ���Ҫ�鵼�ٷ��ͳ�����Ӧ��������ɲ�������IL-4��IL-5��IL-10��TGF-�µ����ڵĿ�����ϸ�����ӣ���Ҫ�����̬��Ӧ�Լ�����Ļ��ת�͡��ڻ�Һ�У������ܼ�T�ܰ�ϸ�����ڵ�ϸ�����ӡ������꣬���о�������RT-PCR��ԭλ�ӽ��������֣�RA��Ĥ����Th1ϸ������Ϊ������Th2ϸ�����ӵ�ˮƽ���͡����в����Tϸ�����ڵ�ϸ��������RA�����е����á��������������о����֣���ĤT�ܰ�ϸ�����ڵ�IL-17��һ����Ҫ��ϸ�����ӣ��������ĺ����ܵ͡�����IL-1��������������-���������������ƣ�������ǿ����ά��Ĥϸ��������ԭø������ϸ�����ӡ�����Ҫ���ǣ�RA��Ĥ��֯�е�IL-17����ЭͬIL-1�������������Ӧ����Ĥϸ������ǿ�ֲ�����֢��Ӧ��
����ǰ������������Ĥ��Tϸ��������ϸ�������ڻ�Һ�еĺ����ܵͣ���ô��Tϸ����������������ϸ������?��Ĥ�ڵĸ���ϸ����Ҫͨ��ϸ�����ӵ����ò�������ã�Ҳ����ͨ��ϸ��ֱ�ӽӴ��ķ�ʽ�������á����µ��о������ʾ������Ĥ��֯�о���ϸ���Ļ��Ҫ����Դ���ھ���ϸ����T�ܰ�ϸ��֮���ֱ�ӽӴ���CD4 Tϸ������Ĥ��֯��ֱ�Ӻ;���ϸ���Ӵ����������ϸ���Ļ����ľ���ϸ�����ڲ���������������-����IL-1�ȴ���֢��ϸ�����ӣ�ͬʱҲ���ڲ���IL-15�����߿ɴٽ���Tϸ���;���ϸ��֮��Ӵ�����ľ���ϸ��������������ܴ̼�Tϸ������ʹ�����Tϸ�����Ի�����ž���ϸ���Ľ�һ�����������������������������-����IL-1���������о�������Tϸ�������ά����Ĥϸ��֮��Ҳ����ϸ����ֱ�ӽӴ����������ά����Ĥϸ���Ľ�һ���������ϸ�����Ӻ͵���ø��ֵ��ע����ǣ�Tϸ���뻬Ĥϸ����ֱ�ӽӴ�������Ҫ���T�ܰ�ϸ�����룬˵�����ַ�Ӧ����ͨ���ǿ�ԭ�����ķ�ʽ��ɡ�
�������о����֣�RA��Ĥ��֯�γɾ����ܰͽ�ijЩ��������λ�ܰ���֯��Tϸ������һ�γɹ��������ż�����Ҫ�����á��������ϱ������ܰ��������γɿ��Է��������绬Ĥ���ܰ�����֯�С������ڻ�Ĥ��֯���ܰ�ϸ���γɵ��������ṹ��Ҫ��CD4 Tϸ����Bϸ���Լ����ݼ��CD8 Tϸ����ɡ���һЩRA���ߵĻ�Ĥ�������ṹ�з��������������γɣ�˵���ؽ��д����ܰͽ����ṹ���������ĵ��γ���Ҫ��ԭ������Tϸ����Bϸ��֮�������ã��Լ�ͨ�����̼����ӱ���ģ�����Tϸ����Bϸ�����濹ԭ���������������ص��źš�����֤�������������ĵ��γ�(һ�ֽ鵼��ԭ���ռ��ͻ��������Ӧ��ĸ����ܰ��ͽṹ)����Tϸ���ģ���Ϊ��֤�ݱ�����λ�ڻ�Ĥ�������ṹ�е�Bϸ�������Ŀ������������Գ���ı��֡��Ʋ⻬Ĥ��֯�������ܰ������ٵ��γɿ���������Ӧ��Ľ��(��9)��
��֮����Ĥ�л��Tϸ������ͨ���������յ�ijЩ���ʣ����ھ���ϸ������Ĥϸ����Bϸ���Ĺ��ܣ�����RA��Ĥ����֢��
(4)RA��Ĥ��Tϸ���Ŀ�¡��ֳ������RA��ĤTϸ��������������Tϸ����¡��ֳ�����������ɶ��¡����Ľ����һ���⣬Ŀǰ�������ۡ�Tϸ�������ɳ��ֿ�¡��ֳ����Ϊ��Ĥ��Tϸ���Ļ����Tϸ������(TCR)�ɷֵĸı䣬���о�TCR�ɷֿ��Ը��õ�����Tϸ��������ʡ������йضԻ�Һ�ͻ�Ĥ��֯��TCR V����V�»���Ƭ�γ��ֵ�Ƶ�ʵ��о��õ�ì�ܵĽ��ۣ����������о�������ķ�����ͬ����ɵġ��еĽ�����Ϊ���������ԭ������Tϸ���Ļ������ij�ֿ�ԭ�����Է�Ӧ����һ����ص�Tϸ����ֳ����ô��ֳ��Tϸ���п��ܷ���ͬһ�����V�³ɷ֡����ǣ�Ҳ���˳ֲ�ͬ���������RA Tϸ��Դ�������صĿ�¡����Ϊ��������о�����TCR�ijɷ�ȷʵ�����ı䣬����Щ�ı䲢�����ԣ����Ҳ��������е��о��ж����������ָı䡣�����о���ʾTCR V����V�µijɷִ��ڶ����ԡ���Ĥ��֯Tϸ���ķ���������ijЩTϸ���ʿ�¡��ֳ�����ǣ�����TCR�Ľṹ����ЩTϸ���ijɷ����Dz�ͬ�ġ�����Щ�۲���Ϊ�����Ľ����ǣ���Ĥ��֯��ֻ��һС����Tϸ������ֳ��Դ�ԶԿ�ԭ������Ӧ����ֳ��Tϸ�����ֳ������ԣ���Ҳ˵�����䲿λʶ��Ŀ�ԭ�ܹ㡣
Ŀǰ����Tϸ����¡��ֳ��Ҫ�����ֽ��ۣ������ǣ���Tϸ���Ŀ�¡�����ڹؽ��ڣ�����Ϊ�Ծֲ���ԭ�ķ�Ӧ����Tϸ���Ŀ�¡���ʷ������Էֲ���ʽ��˵���ڱ���Tϸ�������Է�������ձ�ȱ�ݡ����˵��Tϸ����¡��ֳ�ķ�Ӧ�����Ƕ��ֶ����ģ������������һ��(��һЩ)����������Tϸ����¡����Ҳ��������ɼ��������Ե�ԭ��
(5)Bϸ�������ʪ�ؽ����е����ã�
��RA�е�Bϸ����RA��Tϸ����Bϸ����������δȫ�����˽⡣�ܶ��о��߽����������Լ������о��ص����Tϸ���������ϡ�����Ŀǰ����ȷ���֤����ʾRA�е���������ֱ�Ӳ�����֯�����Ӷ������˿�ԭһ���帴�����ڼ����е���Ҫ���á������RA���߶��ɼ��������壬������60%��80%�IJ��˴��ڸ��������������塣���磬���ʪ���Ӿ��Ƕ�����IgG�㶨���������������塣�Ӷ�RF���о����֣��ؽ����γɵ����߸������Լ������߸�����Բ���ϵͳ�ļ��������ɹؽڵ��ƻ���Bϸ�����˲��������⣬���Bϸ������ʶ��ԭ����������Tϸ���ݳʿ�ԭ���������ھ���ϸ��������Bϸ������һ����Ҫ�Ŀ�ԭ�ݳ�ϸ����
�������Ļ�Ĥ��֯����ϸ���ṹ�ģ���RA�Ļ�Ĥ�п��Կ�����������ϸ���Ľ����˾���ϸ����30%RA���ߵĻ�Ĥ��������Tϸ����Bϸ���γɵ��������ṹ�������е��γ���������(germinal centre)��˵���ؽ��д����ܰ���֯���ṹ��ϸ�����Ӷ�������λ�ܰ���֯���γ����Źؼ������á����������ǿ�ԭ�����Bϸ����չ��Ϊ������Bϸ���ͽ�ϸ����������Ҳ����Һ���߷�Ӧ�������Գ���IJ�λ������˱�������������������ϸ��һ������Ĥ��֯�������ĵ�Bϸ�������ˮƽ��CD38�����ܹ��µ����������塣���������Ļ��Bϸ������Tϸ������ʽ�շ���¡��ֳ���о���ʾ��ͨ�������ʴ�RA���߱����Ļ�Ĥ��֯�п���ֱ�ӷ���õ���ֳ��Bϸ����
�ۻ��Bϸ���ȿɴ���������Ѫ�У�Ҳ�ɳ����ڻ�Ĥ��֯�С�ϸ�������ڿ���IJ�����ת�������ŷdz���Ҫ�����á�IL-2���յ�����ͬ�������������������á���Ϊ��ȱ��IL-2������£�û������ϸ���ܹ�Ӱ���ܰ�ϸ���Ļ����ֳ��ֻ���IL-4��Bϸ���дٽ����������ã������յ�MHC���ԭ��Bϸ������ı��
��Ŀǰ����������й�IgG���Ծ�������ԭ�Եļ�˵��
A.��Ig���Ӿۼ��γɾۺ�����IgG�������Է�IgG��ԭ�γɸ�����п��ܱ�¶���µ�IgG��ԭ�����ء�
B.RA����IgG�ṹ���쳣��ʹIgG���������ԡ����磬IgG��������ȱ�ݿ���������Bϸ��Ĥ��Fc�����ϵ����������⣬Tϸ�����Ƽ���ȱʧ��ʹ��Bϸ��������IgG�Ŀ�ԭ�����ؿ��塣
C.IgG������ԭ�Ļ�����IgG�ǻ����ṹ�ĸı���ء����磬�����ǻ�ת��ø���Ե��쳣���ܻ�����RA������Σ���ԡ�
�������������ԭ����������Ӧ����RA������������ڵ�ԭ����һ����õ������о��ߵ�֧�֡���Ϊ��Һ���߷�Ӧ��ЧӦϸ����Bϸ����RA�ķ�����������Ҫ�����á�
���ٴ��۲쵽��һЩ�����뿹ԭ��ΪRA�IJ�����һ���������
A.һС����RA�����ھ����˼����µĻ�ں�����һ���൱�����ٴ������ڣ�����ʾ���߿��ܽӴ���ij�ֿ�ԭ�������ֿ�ԭ��������
B.���Ŷ�ؽڲ���Ľ�չ��Լ20%RA���߳���ijһ�ؽ�֢״�ķ�������ʾ�Ծֲ���ԭ���ڳ���������Ӧ��
C.��ȾϸС����B19��EB������B���ײ����������²�������������RA�������Թؽ��ס�
D.����θ������������ֳ���ĸ�Ⱦ��ɳ������Թؽ���(
��Ӧ�Թؽ���)��
��ȷ���֤�ݱ������ԭ������RA�ķ�������ͬʱҲ��һЩ�෴�Ľ��ۡ�������������ԭ��ܶ࣬�����о��������Ŵ�����������ַ���IJ��죬��ᾭ�õIJ��죬��������ʱ��ij��̣��Լ��������Ƶķ�����ͬ�ȣ����ң���⿹ԭ�ķ���Ҳ�Ƕ����ġ����潫��RA���ֵ���Ҫ����ֱ���н��ܡ�
(6)���ʪ���ӣ����IgG��Fc�β���������������������RAһ����Ҫ�������쳣���֡���RA��˵�����ʪ����(RF)�����߱������ԣ���Ϊ�ڽ����˺���������ϸ���Ը�Ⱦ��������ֲ��ijЩ�������Լ����Ȼ�����Ҳ�ɳ��֡����ң�RF���ֵ�Ƶ������������������ߡ���Լ80%RA���ߵ�Ѫ���п��Լ�RF����������������������Ŀǰ��Ȼ��RF��Ϊ���RA����Ҫʵ����ָ�ꡣ
������о�������������֤��֧��RF��RA�ķ�����������Ҫ�����ã������ǣ���RA�����س̶Ⱥͼ����Ļ����RF��ˮƽ��ء�Ѫ�����Ե�RA���߽�Ѫ�����Ե�RA���߳��ֹؽ���֢״��Ƶ�ʸ���(�����ʪ��ڡ�Ѫ����)������ǰ�ߵ�Ѫ�����죬����ˮƽ���ߣ��ַ��Ĺؽ���Ŀ���ࣻ�ڻ�Ĥ��RA��֢��Ӧ��Ҫ�����IJ�λ�������Ծֲ�����RF����RF��Ѫ�塢��Һ����Ĥ��֯��������֯�����߸��������Ҫ�ɷ֣��ܶ��¡IgM RF����ͨ������;���̶��ͼ���壻����RA���ߵĹؽ���ע��RF���Դٽ���֢��Ӧ����Ѫ��RF���Ե��ؽ�֢״�߳���RA��Σ�����������ӡ�
������֤�ݱ�����ԭ�鵼�ķ�Ӧ������ΪRF�ĵ��ڼ�����������RF�����Ļ����в����������֤����ʾ�����������յ�RF�������Ŵ�Σ�����ء�Դ��Bϸ�����������ɷ��ڴ���������V�ʻ���Ƭ�ε�RF���������γ����ʪ�ؽ���RF��������V����Ƭ�ε�������ɳɷֲ�����Ωһ�ģ���Ϊλ�������������������е����ͬƬ�ζ�����ΪRF������ɳɷֵĴ�������RF����һ������������ϵ����(germinal gene)�ɷ֡����ƺ�����RA��Ĥ������Ѫ�в���RF��Bϸ���ǿ�ԭ������Ӧ�Ľ���������Ƕ��¡Bϸ���̼��Ľ����Ŀǰ�в�����Ŵ����غ���Դ�������ڴٽ����¡Bϸ��������е����á�
�ڶ���ʵ���п��Կ�����lprС���fas��������ͻ�����Բ����ߵζȵ�RF�����������غͳ���ԭ���ڵĶ��¡�̼��������յ�RF�IJ����������Bϸ�����ڳ���ά����Ĥϸ����IL-10�������½���������RF�IJ����������ӡ�����ʵ����ʾ����Tϸ���������£�RF���Է���ͬ��ת�������Գ��졣���⣬RF���Ե�Bϸ����ֳ����ڻ�Ĥ��֯����Ϊ������RF�����IJ�λ��
RA���ߵ�Ѫ���г���RF��˵������ʧȥ���������ܡ������о��߶�RFת����С���Bϸ���������ܵĵ��ڽ������о�����֤ʵ����������
�ڼ����ķ�չ�����У�RF������һЩ���ã��ٺ���RF�����߸���������ڶ�����֯�У��п���ͨ�����뻬Ĥ��֯��RAѪ������֢��Ӧ������弶����Ӧ�������������ˣ���RF��RA�е�������������������ѧ����������أ�����RF�ܹ���IgG��ϣ�ʹ�ñ���RF��Bϸ�����Բ��������߸������õĿ�ԭ���뿹ԭ������Bϸ��һ����RA�в���RF��Bϸ��������ΪIgG-��ԭ������Ŀ�ԭ�ݳ�ϸ���������߸����ﺬ�еĿ�ԭ�ݳʸ���ԭ������Thϸ������ά�־ֲ�����Ӧ�𣬲��̼�ǰ��֢��ϸ�����ӵIJ�������IgG-RF���Խ�������ʶ����һ����Ũ���£������γɶ������С�Ķ���塣��ʵ��֧�֣���Щ��������CD16A(����ϸ���ϵ�������Fc������)�Ľ�Ͽ����������ʹٽ�������֢����Ҫ���ƣ����ڶ�RA���߽��е������У���ȡ�Ի��ߵ�RFע��һ���ؽڣ�����������IgGע����һ���ؽڣ����ǰ�߳��־��ҵ���֢��Ӧ��������δ���֡����Ҷ���ģ��Ҳ֤ʵ�˵���ע�����ijһ������ԭ�������������������ת�ơ��о���������ģ���²��Ե����������������-6-�����칹ø�������ԡ�������-6-�����칹ø���ǽͽ�;���е�һ��ø������ÿ��ϸ�����ɱ����ø�����в�����������������Ե���������������յ��ؽ���֢�ġ�ֵ��ע����ǣ���Щ�������ԶԶ���ؽ���ģ�͵Ĺ۲졣����ֱ��֤����ʾ����RA������RF�߱��������á�
(7)RA�������������壺
�ٿ����ݿ˵���dnaJ���壺E.coli�����ݿ˵���hsp65�ij�Ա֮һ��������DNA���ƹ�������һ�����á�ϸ���е����ݿ˵���ͨ������ģ����������ʪ�ؽ���Bϸ��������Ӧ������Ҫ���á��Ʋ���Ϊ�������Դ�Կ�ԭ����������Դ�Կ�ԭMHC��������ͬ����ô���������п����¹ؽ������ǡ���ĵݳʣ���������������֯������֢��Ӧ������ģ�����ƻ����������Լ�����Bϸ�����ܷ�����һ�����á������о�����������ת����С��ģ����֤ʵ��ģ��������ԭ����Դ�Կ�ԭ���Խ��Bϸ������������(peripheral tolerance)�����ж������֤ʵϸ��dnaJ�����ܲ�����RA��������
�ڿ����ǵ��������壺���кܶ�֤��֧�����ǵ��͵�������RA�����е����á���BALB-cС���У����ͽ�ԭ���ۺ��ء��������ӵ���������gp39�����յ��ؽ��ķ�����ͬʱҲ��֤�ݱ�����Щ��ԭ��RA�пɷ������߷�Ӧ��
A.���ͽ�ԭ��������С����鳤�ද��������Ȼ�Ģ��ͽ�ԭ��������RA���Ƶ����Թؽ��ס����������͵Ĺؽ�����ȣ���RA���ߵĻ�Ĥ�г��ɼ������ͽ�ԭ���塣�����RA�����ڷ��ָÿ��壬��Ԥʾ�п��ܳ��ֽ�Ϊ���ص�֢״����ʵ����ʾ�����������ȣ��ڷ����ͽ�ԭ��RA���߹ؽ���ʹ�����͵ı������Լ��ᡣĿǰ��Ϊ����ԭ������²����ƿ�����ͨ���γ����߸���������Ӷ�������֢��Ӧ����Ϊ��RA���˵�Ѫ�弰�ؽ�Һ�ж��ɼ�����н�ԭ�����߸����������Щ���߸�����������C1q������������ԭ���������RA����֮��������Ϊ���Ǽ̷��ڹؽ���֯���ƻ���ͬʱ�ֲ���ؽ���֯���ƻ����ٽ�RA���̵ķ�չ��
B.�������ǵ���39����RA���������ǵ���39(HCgp39)�ǽ��������о��߹�ע�ĺ�ѡ������ԭ�����ǿǶ���ø������ǵ��׳�Ա֮һ�����Ĺ���Ŀǰ��δ�������ʶ��HCgp39����Ǵ�RA���ߵĻ�Һ��ѪҺ�з���õ��ģ�����Ϊ�ǹؽ����˵�������־�����ڹؽڵ�����ϸ���ͻ�Ĥϸ�������HCgp39����BALB-cС������շ����Կɸ����Ĺؽ��ף�������RA��˵�������շ�Ѫ����IJ��������ǵĽ��⡣��HCgp39Ԥ������BALB-cС����ֳ������������ӳٺͼ�����ȵļ�������˵���ڶ���ģ����HCgp39�����յ��������ܡ������������Գɹ��ػ���ڻ��BALB-cС��IJ��顣��Щ������ʾ��HCgp39��Ϊά�ֻ�ĤBϸ����Ӧ��������ԭ��RA�е����á�
C.�ۺ��غ��������ӵ��ף��ۺ���(aggregation)�Ǻ��к��ĵ������ǵ�����(proteoglycan)�������ǰ����Dz���������������غ������������Լ���N-���Ӻ�O-���ӵĹ��ǡ��ۺ��صĽṹ��������������(G1��G2��G3)���������ӵ�����һ��С���ǵ��ף������ȶ��ۺ���������������á��÷��ǻ����ĺ��ĵ���G1�ṹ������BALB-cС��ɳ�����RA���ƵĽ����Զ�ؽ��ס���һ����RA���ߵ�Ѫ���п��Լ����ۺ���G1�ṹ���Ŀ��塣�ǻ����ĵ��������յ�С����ֹؽ�����Ҫ��ɳɷ֡����������ͷų��ĵ�����Ƭ����ά��RA��Ĥ�쳣����Ӧ��������Ҫ���á�
��Ӧ�����ٴ������������壺
A.���ǵ�����(antikeratin antibody��AKA)���ü������ӫ�ⷨȾɫ����ʳ���жεĽ��ʲ���Լ�AKA��AKA��ƽ���İ��״��������֯���ɳ�������Ⱦɫͼ�Σ���������������RA���ߵ�Ѫ���У���˱�������ų���AKA-IgM��RA�Ƿ������Եģ���AKA-IgG��RA�и߶ȵ������ԡ������������Ľǵ������RA�������Բ����ܸߣ������������RA�����Կ�ԭ�ǽ��ʲ��в�ͬ�ijɷ֡���50%���ҵ�RA���߿ɳ���AKA��������������0%��3%������AKA�������жȺܵͣ���������RA�������Դﵽ95%��100%������Ҫ���ǣ�Լ��34%�����ʪ�������ԵĻ��߿ɳ���AKA����������У�AKA����һ����������塣
B.����������(antiperinuclear factor��APF)����Ƥϸ��������������ʿ����п��Լ��������ӿ�ԭ�����ֿ�������Բ�Σ�ֱ��0.2��0.3��m��ÿ��ϸ������2��10����ֻ�кϳ����ǵ��ļ��Ĥ��ʳ���Ĥ����Ƥϸ���ű������ֿ�ԭ��Ŀǰ��֪���ֿ�ԭ��profillagrin�йء�APF�ļ���볣��Ŀ���ʵ���Ҽ�ⷽ����ͬ����Ϊ�������ֿ�ԭ��ϸ��ϵ���٣���̫�����ҵ����ʵĹ���(����10%��������Ĥ����APF)�������ߵ�APF�ζ�Ϊ1��5�����������߲����߸ÿ���ĵζ���1��800��APF������RA��SLE��ϵͳ��Ӳ���ʹ�Ⱦ�Ե���ϸ������֢�Ȼ��ߵ�Ѫ���г��֡���RA���ÿ�����������Ը���AKA���������Ե��ں��ߡ����ʪ�������Ե�RA���߳���APF�뼲�������س̶ȡ��ؽ�����֣��Լ�����ѧ�ı��ֽ�չ�йء�
C.��HnRNP�����壺Լ��47%��RA����Ѫ���д���IgG�Ϳ������Ժ�RNP(Hn-RNP)���ĵ���A1�Ŀ��塣HnRNP��������ǰ-mRNA�йأ�����СnRNPs��Sm��nPNP��ͬ��������Ҫ��SLE�������ڵĿ�����ʶ����Ȥ���ǣ�AKA�Ļ����뿹A1����ij�����أ������AKA��HnRNP A1��ԭ�н��淴Ӧ��
1/3��RA���߿��Լ�����RA33kD���塣�ÿ�����������Ѫ���в����ڣ���˸ÿ����Ϊ��һ��Ѫ��ѧ������õĿ��塣RA33kDҲ����HnRNP���ĵ��ף������б���A1��
D.���۽ǵ���˿������(anti-filaggrin antibody��A
FA)���۽ǵ���˿���ײ����ڲ��鶯����Ƥϸ���ֻ�����ĩ�Ρ�������ԭ�۽ǵ���˿����(profilaggrin)��ǰ����ʽ�ڽ�����Ƥ��֯�кϳɵġ�ԭ�۽ǵ���˿���׳�������Ƥϸ���Ŀ����ڣ���ϸ���ֻ��Ĺ����У�������ˮ�����ã��ͷų��ľ۽ǵ���˿���ס�������ε��������ᣬԼ��20%�ľ�����л������������ǰ���ø������ת��Ϊ�ϰ��ᡣ30%��40%�ľ۽ǵ���˿���İ�����л����ظ���λ�仯��������ˣ��۽ǵ���˿���İ��������д��ںܴ�������ԡ���Ҳ��A
FA���ٴ�Ӧ���������谭��
A
FA����RA��ص�IgG���������壬���а���AKA��APF��A
FA��������ӡ������ELISA���м�⣬�����ױ������ÿ���������ԺͿ��Խ�AKA��ARF�ļ������ӫ���������ߡ���ȥ��ΪA
FAʶ��������Ƥ��֯�ľ۽ǵ���˿�����Լ�������ԭ�۽ǵ���˿������صĵ��ס�20����90���ĩ��������ͨ�����������ǰ���ø�����˾۽ǵ���˿���õ�A
FA���Ŀ�ԭ�����أ�����2/3���Ծ۽ǵ���˿���ϳɶ��ĵ����IJ�λ�ǹϰ��ᡣ�����ֱ��봿����A
FA���塢RAѪ�巴Ӧ��ֻ�к��ϰ�����������ܱ�RAѪ���A
FA����������ʶ����Щ˵�����ϰ��ᣬ��RAѪ�忹�۽ǵ���.˿������ؿ���ʶ�����Ҫ����Կ�ԭ�����سɷ֡���ˣ��˹��ϳɵĿ����ϰ�����Ŀ���(anti-CCP antibody)�������ױ������������Է��棬��CCP������RF���ƣ��������ԽϺ������������ߡ�Kroot�����ٴ��۲���Ϊ����CCP�������Ե�RA���ˣ������ƻ��ij̶ȣ��ϸÿ������������ء��ɴ˿ɼ���CCP�������RA��������Ϻ�Ԥ��������һ�������塣
(8)�������������ʪ�ؽ����е����ã���������(innate immunity)ָ���ǶԸ�Ⱦ���صķǿ�ԭ����������Ӧ�𣬰����������ġ����弤��;������¶�ǽ��������(mannose binding lectin��MBL)ϵͳ����Ȼɱ��ϸ���Լ�ϸ�����ӵ��ͷŵ����ڵ�ЧӦ���ơ�����෴�����������(adaptive immunity)��ͨ��Tϸ����Bϸ��������ԭ�����Ե�����Ӧ�𣬾��зֱ����Һͷ��ҵĹ��ܡ���������Ӧ���дٽ���֢��Ӧ�����ã����һ��ɶԻ���������д̼����������á�
�о�����������RA�е����ã�ǰ����ij�ָ�Ⱦ����ֱ�Ӵ̼���������ϵͳ��������ͷſ���������Ĥ��֢�ķ�������ϸ�����ӣ�����Ŀǰ�в�֪���ָ�Ⱦ������ʲô��
���������RA�ķ����ƺ���ʼ�ڻ�Ĥ�����ϸ������Щϸ�������������ӣ�ʹ�õ���ϸ�����ܰ�ϸ������ؽ��ڡ��������ϸ�����ܰ�ϸ��ʶ����ؽ��ڵ�ijһ��(����)��ԭ����ô�ܰ�ϸ���ͻᱻ�������������ŷ�����֢��Ӧ������С����ԡ��Ļ������Ըı�Tϸ�����͡�������費��Ҫij�������Ե��²����أ��κ�һ�ֽ���ؽڵIJ�ԭ�嶼�ɼ�����������Ӧ��
���ݶԶ���������֢�Թؽ��������Ƶ��о���������Ϊ��RAҲ�ɳ������Ƶı��֡�����������Ϊԭʼ���ƶ����п�����RA���ڽ�������ԭ����������Ӧ�𣬲��п����ƶ���һ���̵Ľ��̡���֯ѧ���о���ʾ����������ϵͳ������RA��Ĥ��֢�е����ð�������Ĥ�з���������֢���Դ̼�����ϸ���ͷ�ϸ�����ӣ�������ͻ״ϸ���ֻ����γ���Ч�Ŀ�ԭ�ݳ�ϸ������Ĥ�г������ͻ״ϸ�����Խ���ԭ�ݳʸ�������Tϸ�����յ�����Th1��Th2��Ӧ������ϸ����������ϸ����Ƭ�Σ������ӻ����Ĥ�������ؽڵľ������ߴ̼��Ե�DNA��ϸ������̼�����ϸ�����ڵľֲ�ϸ�����Ӳ��ٴμ�����ͻ״ϸ����Bϸ������Ȼɱ��ϸ�����ؽ��ڻ�IJ���ϵͳ��ǿ�ֲ�����֢��Ӧ��Bϸ����Ӧ��
����ͻ״ϸ��(dendritic cell��DC)��RA���������е����ã��о����֣�RA�Ļ�Ĥ��֯�Լ���Һ�к��зḻ����ͻ״ϸ��������Щ��ͻ״ϸ������DZ�ڵĿ�ԭ�ݳ�ϸ��(APC)�Ĺ��ܡ�RA����ͻ״ϸ����������һЩ�ص㣺
A.�����RA��Һ�е�DC����ijЩ�ֻ���־���ӣ���߱���MHC-��HLA-DR��HLA-DQ���ӡ�������DC�Ŀ�ԭ�ݳʹ��ܹܺؼ���
B.DC�ۼ��ڸ���ϸ�����ӵĻ�Ĥ��֯�У�����ϸ�����ӵİ������������ͺ��ܵķֻ���
C.�ھֲ�ϸ�����ӵ������£�DC�ķֻ�Ҳ������Th1���ܣ����յ�Th2Ӧ�𣬻��յ�ϸ������������С�������ο�ԭ��Ӧ����ˣ��о���ΪDC���ܲ����˻�Ĥ��֢����ʼ�Σ������Ǵٽ�RA��Ĥ��֢��Ӧ��Tϸ������Ӧ�����Ҫ���ء�
�ھ���ϸ����RA���������е����ã���������ʶRA��������Ⱦ����һֱ����Ϊ�DZ������������أ���������δ�ҵ���Ⱦ��ֱ��֤�ݡ�����ϸ����ΪRA��������Ҫ��������Ҫ������һЩ���ݣ�
A.����ϸ����ijЩ���ԭ�������£����Ա������ģ��ʶ������(PRR)�����¶�����塢Toll���塢���������ȣ��ͷŶ���ǰ��֢��ϸ�����ӣ���GM-CSF��IL-1��������������-����IL-12��IL-15��IL-18�ȡ�
B.����ϸ��������Ϊ��ԭ�ݳ�ϸ��(APC)����Ĥ�еľ���ϸ�������λ�ڳ���㣬������뻬Ĥ��ϸ�����ӵIJ����Լ��ǡ����ǵ��ƻ���ء���������ͻ״ϸ����ȣ�����ϸ����������APC��
C.����ϸ���ͷŵľֲ�ϸ���������ٴμ�����ͻ״ϸ����Bϸ������Ȼɱ��ϸ������ʹ��ͻ״ϸ����һ���ֻ��γ���Ч��APC��
�۲�����MBLϵͳ��RA���������е����ã����嵰�ȿ�����ΪЧӦ����Ҳ����ϸ�����������ã����磬ǰ��ͨ��C5-9Ĥ���������������ֱ���ƻ�ϸ��Ĥ����IJ��嵰��������Ƭ�ξ���ϸ�����������ã�C5a��һ����������ϸ���������ӣ����ɽ�����һ����RA�ؽ�ǻ�ڵ����߸�����Ϊ����Ļ�ṩ�˷ḻ�ĵ�����������ಹ��ϳɵ���Ҫ��Դ��ͨ��Ѫ�嵰�ױ���ת�����ؽ�Һ�С��������ؽ�ҺҲ�ܲ����ֲ��IJ��嵰�ס�1970�꣬�״�֤ʵ�˻�Ĥ��֯���Ժϳɲ��嵰�ס�����ʵ���������ϸ�����Ӵ��ڵ�����£�����ϸ����(��)����άϸ��Ҳ�ɲ������ֲ��嵰�ס����磬IFN-�ÿ��յ�C2��C3�IJ�����IL-1��������������-�����յ�����C3��
������RA��֢��Ӧ������Ҫ���á���Ҫ������֤�ݣ�
A.��ԭ�յ��Ĺؽ���(collagen-induced arthritis��CIA)������������в������
B.��C5ȱ��С��CIA�ķ����Ͳ���ķ�չ�ܵ����ơ�
C.�ÿ�C5�����������Ƽ������Բ�������-1����С�ɷ�ֹCIA�ķ�����
����ϵͳ�е����;����Ҫ��3�֣��ֱ��Dz��徭��;����������·;����MBL;�������в�����·;���Ƿ�ֹ��֯���˵���Ȼ���ڼ���������״̬�²�����·;���ļ����ǵͶȵģ�����RA�ؽ��У���������·;������Ϊ�������⣬���廹������Ȼ�IJ�����ڵ����˵�Ĥ��ϲ���������ӡ���֤����ʾ��RA�ؽ��в�����ڵ��ױ��オ�ͣ���Щ���ڵ���ȱ��ʹϸ�����׳��ֲ��ʵ����ѽ⡣
��¶�ǽ��������(mannose-binding lectin��MBL)���ڼ����ڵ��ף����ɲ��������������ߵĸ�ϸ�����ڵġ�MBL���¶�ǻ�N-��������������ĩ�˵������ϣ��ڲ��������������¼���弶����Ӧ��MBL����ģ�������Ͳ���(C1q)�Ķ��ֹ������ԣ���ˣ�������Ϊ�����������˷���ϸ���ĵ�һ�����ߣ����һ��߱�����һϵ�л��ԣ����������ĵ��ڡ�MBLȱ�ݿɵ��·�����Ⱦ�����ҿɼ���RA����ķ�չ���о���ʾ��MBLȱ����RA�ķ��������磬��ؽڲ���Ҳ���ء�ͨ����һ��RA�����뽡���˵ĶԱ��о����֣�RA��MBL����ͻ�������MBL��Ѫ���еĺ����ܵͣ�����������ԭ���ɴ˿ɿ�����MBL��ȱ�ݿ���Ԥ��RA�ķ����Լ����������س̶ȡ�
��NKϸ����RA���������е����ã�NKϸ��������RA��Ĥ�ij����ͳ����²����RA���ڿ��Է��ִ�������øB(granzyme B)Ⱦɫ���Ե�NKϸ��������RA���ںǹؽ���������ټ�����ЩNKϸ����ˮƽ��Ѫ���м����ڵ�����ء����ң���RA���ߵĻ�Һ��Ѫ���пɼ���ˮƽ�Ŀ����Կ���øA��B����Щ˵��NKϸ���ر�����RA������һ�����ã������DZ����������ͷ�ϸ���ڿ������������ȻNKϸ���ڶԿ�������Ⱦ����������������Ҫ���ã����ǻ�ĤNKϸ����δ���κ������ԵIJ�����Ⱦ�������
�����ݿ˵�����RA���������е����ã����ݿ˵���(heat-shock proteins��HSP)��һ����ж��ֹ��ܵĵ��ס�HSP�Ƕ�ϸ������֦�˾��ͼ�����Ȳ�������Ӧ�������ʶ�����Ҫ��ԭ�����磬����С�����߽�˷�֦�˾������Բ�����HSPs70��60��18��12���塣��֦�˾��ĸ�Ⱦ�����߿��յ�����Bϸ����Tϸ����Ӧ���������ߡ������HSP60���֦�˾���HSP70�������Ƶ�����(Լ��60%����ͬԴ��)���������ϸ���ĸ�Ⱦ�����п��ܻ��յ��������߷�Ӧ�ķ������ڽ����߿ɼ��������HSP��T�ܰ�ϸ�������ʹ���ǵõ������Ľ��ۣ������ܴ��ڲ����������ߵ�Σ���ԣ����Ƕ�HSP������ʶ���ڿ�ϸ���������зdz���Ҫ�����á�
��RA����Ĥ����㡢����/Ѫ���轻�紦��Ƥ�½����ϸ����ϸ�����пɼ���ˮƽ��HSP60��ԭ�����أ�����������֯�����ⲻ����RA���ߵĻ�Ĥ�Լ���Һϸ����ϸ�����б���HSP60��HSP70��HSP90������HSP60��������IFN-�ô������ľ���ϸ���Լ�������Burkitt��s�ܰ���ϸ�����档��ˣ������Ʋ⣬��Ĥϸ�������HSP�����뻬Һ�еĿ����γ����߸����
��ϸ��������RA���������е����ã��ڹ�������ϵͳ�д�������ϸ�����ӣ��ֱ��ǣ�
A.�鵼���Է�Ӧ��ϸ�����ӣ�����IL-1��������������-����IL-6��IFN-����IFN-�¡�
B.��������õ�ϸ�����ӣ�����IFN-�á�TGF-�¡�IL-4��IL-5��IL-10��IL-12��IL-15��IL-18�������ж���ϸ�����Ӳ�����RA��Ĥ����֢��Ӧ����֯���ˡ������д����Ŷ��ֹ�������ϸ�����ӵ���Ȼ�������ʾ��Щϸ�����ӵ�ǰ��֢�����õ���Դ�Ե����ڷ�ֹ��������������Ҫ���á�
IL-1��������������-����DC�;���ϸ����������DC�����ڷֻ�������Ҫ���á�IL-1����Ȼ������IL-1Ra�ɾ���ϸ������������ϸ���͵���ϸ������������IL-1R��ϣ����������ϸ����������RA����ĤҺ��IL-1Ra�ı���ˮƽ�ϸߡ����ǣ�����ϸ������IL-1��������10��100����IL-1Ra��������IL-1���Ե�50%����ˣ�RA����ĤҺ�����ߵ�IL-1Ra������������IL-1������������á����⣬IL-1��������������-�����ԵĿ���������Ҳ����ֹ���ǵĻ��ԡ�
��ͻ״ϸ���;���ϸ����Th1ϸ������IL-12����Ҫ��Դ��������RA��Ĥ�ij�������IL-12��mRNA�͵����ʡ�ʵ���ϣ�RA����Ѫ����IL-12��ˮƽ�����͵Ĺؽ�������ʹ�Ĺؽ�����CRPˮƽ��أ���˵��IL-12�ڼ�����������һ�������á�IL-12����p35��p40��������ɵģ��������κ�һ��������û��������ԡ�����p40ͬ�Ͷ��������IL-12�����Ĺ��ܡ�
����һ����Ҫ��ϸ������IL-15����������ͻ״ϸ��������ϸ������Ƥϸ���ͳ���ά����Ĥϸ�����ڵġ���������Tϸ�����뻬Ĥ��֯�����ʹ֮����������ң������ɴ̼���ĤTϸ������������������-���������⣬IL-15����Ŀ����Ԧ���������ΪIL-15��������
IL-18���ɻ�Ĥ����ϸ�������ġ�������IL-12��IL-15��ͬ�յ�NKϸ����Tϸ������IFN-�ã����ɴ̼�����ϸ������IL-1��������������-����IL-18��ϵ�����IL-18��Դ�����Ƽ���
������������RA��Ĥ�п��Լ���������ϵͳ����Ҫϸ���ͷ��ӣ������п���ͨ���������Կ�ԭ���Ʋ�����֢�����������ǣ����粹�����Ƽ���MBLϵͳ���������ͻ״ϸ����NKϸ�������������塢������ϸ�������Լ�ϸ�����ӵ������ȹ�������ϵͳ����Ȼ���ڻ��Ʋ�������ֹRA��Ĥ�ķ�չ�����У���������ϵͳ���ڻ��ƴ��ڵ�ȱ���п������Ŵ����ؾ����ģ�Ҳ�����ܻ������ص�Ӱ�졣��Щ�쳣�ĵ��ڻ����ڲ����б���Ϊ������ʽ��������Ŀǰ�в������RA�й�����������������Եĸ������ã�������Ϊ�²�����Ҫ��ʽ���ڡ�
4.�������ǵ��ƻ� RA��������֢�Թؽڲ���֮ͬ�������们Ĥ�й��������������ɶ��뻬Ĥ�Ӵ��ľֲ�������ǣ�������ʴ���á����ֻ��Ʋ�������һ����(��10)��������Dz�������֯��ƻ���ΩһĿ�꣬����ϸ�����ƹ�ϸ��Ҳ��������֯ϸ������ʵĶ�ʧ���̣�����RA�ؽ��ƻ���Ŀ�껹�����ʹ��ͼ��졣
�����������£������������ǵĺϳɺͽ����һ�ֶ�̬��ƽ���У�������ƽ����RA�����������ƻ�����ɽ����֯�ij������⣬���³���������ǵĽ����ԺͲ��������ƻ������в�������ذ�����������IL-1��ϸ�����ӶԹؽ������Ե��ƻ�����Ҫ���ã���Ѫ���������Լ��ܹ��ٽ�Ѫ�����ɵ��������ӣ����Dz�������ǿ����ϸ����ʴ�ؽ���֯����������������֢��ϸ��������ϸ���ṩ��������ϣ����������ӿɽ���������ϸ������ؽ�ǻ�ڣ���Щ�������Ӱ���C5a������ϩB4��ѪС�����ӣ��ڹؽ�ǻ����������ϸ���ͷŵ���ø���������ӣ�������ø����������øԭ����������������ø���γɵģ�����ʹ����ø���ͷ��Ŵ�����ã��ݻ�Ĥ��֯���������Ե���ø������ԭø�ͼ������أ���Ҫ�����������ǵ���ʴ������ά�����ڻ�Ĥ�������ϣ���Ѫ�ļ�����Ӧ�ɽ�һ���ٽ���֯�����ˡ�����������ʴ�����Ȼ�����Ƽ��������Ƕ������Լ���RA����֢��Ӧ��
(1)�����ƻ��Ļ��ƣ��ؽ��������ɴ����ļ��ʺ�����������ϸ����ɵġ����У���ԭ��ά�������ǡ�ˮ��������Ǽ��ʡ�����ϸ���ɺϳɲ����ڽ�ԭ���ס��������Լ����������ڼ��ʵĵ��ס�RA���ǵ��ƻ���Ҫ��ָϸ�����ʵĽ��⣬��һ����ʵ�����Ǽ��ʱ�ˮ�⵰��ø�����Ĺ��̡�
RA���ǵ��ƻ���ø����ѧ���õĹ��̡���IL-1��������������-����ϸ�����ӵĴ̼��£���Ĥ��ϸ���ͷŸ��ֽ������Ǽ��ʵ�ø�����ǻ����������ʽ�����������ӽ�ϵ���ʽ��ɹؽڵ��ƻ����ڻ�Ĥ�����ڣ���IL-l�������£����ֵ���øʹ����ϸ���ĵ��������������������ǵ���ѧ���ü���������������ȫ����������ʧ�����Ǽ�ʧȥ����縺����ɱ��εĻָ����������Ž�ԭø�ͼ������ض����ǵ����ã�����ʹ��ʧȥ�˹��ܵ������ԡ����⣬��֤�ݱ���������ϸ��Ҳ�ɲ�����������ø���о���ʾ��RA���Ǽ������غͽ�ԭømRNAˮƽ�������ӡ���ˣ����ǵ��ƻ����ڶ����Ƶ���������ɵģ������и�������ø�Ļ�Һ�����ã���ʴ��Ѫ��������ã����һ�������ϸ���������ƻ����á�
�ټ��ʽ�������ø(MMPs)�����ʽ�������ø(matrix metalloproteinases��MMPs)��һ����ø���ڰ�����ʵĽ��������������Ҫ�����á���Ϊ����(������ԭ�͵����ǵ�)�Ľ�����RA�ؽڵķ�����ռ������Ҫ��λ�ã������˽����MMPs�Ļ���ʮ����Ҫ��������һ������ÿ��ø���ص㲻����ͬ�����������ڽṹ�Ͼ�����������֮�������˵�����������Թ�ͬ�Ļ���һ��MMPs�������Ե�øԭ��ʽ���ڣ�ֻ�о����ֽ��ž��ԡ������ֵ��ֽ�������Ҫ��п���ӵĴ��ڡ�п������MMPs�ϵİ��װ��������γ����Ե�ø����ʧȥ���ֽ��ʱ��MMPs�ž��е���ˮ��Ļ��ԡ�һ������£��ж����ϵİ��װ����ͷų����л��Ե�Ƭ�Σ�ͬʱ��п����Ҳ������ø�ķ�Ӧ����ijЩ�����£�������ø���������װ����Ա�����ø�Ľṹ�У����ǵ����㹻���ģ������кл��Ͳ���������������γɶԺϡ����⣬MMPs�ڽṹ�ϵĹ�֮ͬ���������������ƵĴ��ṹ��MMPs������������Ƕ��صġ����磬�����������ṹ�Ľ�ԭø���Խ���I������X�ͽ�ԭ����������ø��ɽ�����ԵĽ�ԭ����������(stromelysin)�������Ը��㷺���������ɼ��кͻ��ԭø�����ɽ��⵰���ǡ�
ϸ�����Ӳ��������յ���Ĥϸ���ϳɽ�������ø�����ҿɸı������ʵIJ����ͽ���֮���ƽ��״̬��PDGF����ֱ���յ�����ϸ����������ø��ͬ������������Ҳ�������Ƶ����á��ڳ���Ѫ���γ�(angiopoiesis)������ʱ��PDGF��ΪѪС�弤���ﱻ�����ͷ���RA����֯�С�IL-1�������������Ӧ�Ҳ��ֱ���յ�����ϸ�������������ø����������ά����Ĥϸ������������ϸ���������ϳ���ʱ�����ǵ������е���ЧӦ��ЭͬЧӦ��������Ķ���ʵ���������ȻRA��Ĥ�����������Դ̼����ǵĽ��⣬�����ɱ�IL-1�Ŀ��������ơ���Щ�о���ζ��RA��Ĥ��Ϊ��������ϸ����������ø��IL-1����Ҫ��Դ�����⣬IL-6�����յ���Ĥϸ��������������ø����������TIMP-1�IJ�����
MMPs�����ã���������ø�IJ����ٶȣ�����ø���������Ƽ���ء����ѿ�¡�������õ�����MMPs�����Ƽ�������Ϊ��������ø����֯���Ƽ�-1(tissue inhibitor of metalloproteinase��TIMP-1)��TIMP-2�����������Ƽ�������Լ��38%����ͬԴ�ԣ�����ͨ����ѧ�����ķ�ʽ(1��1)���������ø��ϣ��Ӷ���ϵ���ø�����á������Ƽ����������ø�Ľ���ǿ���ģ����кܸߵ�������
��MMPs���ر��Ǽ������غͽ�ԭø����������Ҫ��������֯���ʵ�ø������Ϊ��RA�ؽ����˵���Ҫ���ʡ�����ֱ����������MMP�Լ�TIMF��
A.��������(stromelysin)�����������ֳ�MMP-3��ֻ�е�pH��7��8���ž�������������ԡ��������ضԼ��ʽ�ԭ�Ľ������ú�С�������ɽ�����ͽ�ԭ����ά���ӵ���(fibronectin)����ճ������(laminin)�������Ǻ��ĵ��͢��ͽ�ԭ�����⣬�������ػ�����ԭ��ԭø�ļ��
B.�������ػ��������ǴӴ���ת���ij���άϸ���з��ֲ���¡�õ��ġ����ڶԸõ���ø���о����֣������Խ������Ǽ��ʡ���RA����ģ�͵Ļ�Ĥ��֯�пɷ���õ���������mR-NA���������黯Ⱦɫ�����ڻ�Ĥ�����ϸ��������ϸ�����ƹ�ϸ�����м������ص��ס������RA����Ĥ�ij����ͳ�����¼��������ص��ס���ǹؽ��Ļ�Ĥ��֯��ȣ�ǰ�ߺ��еļ������ص�����Խ϶ࡣ���˸���Ȥ���ǣ��ü���������̽��Ի�Ĥ��֯��ԭλ�ӽ������ּ��������ڻ�Ĥ��֯�еķֲ���ͬ���������mRNA�����ڻ�Ĥ����㣬�����dz����²㡣�������������ص������ɳ����ϸ�������ģ�����������²㱻����ϸ�������ա����˼������أ��Ѵ�RA��Ĥϸ����cDNA�Ŀ��п�¡�õ����������ø���и߶�ͬԴ�Եı���Ϊ��������-2�ĵ���ø��
�ڽ�ԭø����ԭø�ֱ���ΪMMP-1�����������һ����RA��Ĥϸ��Ҳ���Է��ڴ����Ľ�ԭø��1967�꣬�״���RA��Ĥ�����������з��ֽ�ԭø-1��RA��Ĥ��֯�еĽ�ԭø��pH 7��8�Ļ����¿��Է�������������ԡ���ԭø��Ҫ��I������X�ͽ�ԭ�ȼ��ʽ�ԭ�����������ã����Ԣ����������ͽ�ԭ�Լ������������ṹ�Ľ�ԭ�������Ƶ�ЧӦ���о���������RA��ԭø����ı��ﷶΧ�ܹ㡣��Ȼ�������غͽ�ԭø����������RA���ߵĻ�Ĥ�����ϸ�����������Ƕ������ڼ������ڵĶ�λ�в�������о����������ڵĽ�ԭ�Թؽ�����ģ�ͣ����ֻ�Ĥ������ϸ���ж��������߷�Ӧ�Եļ������ء���֮�෴���ڻ�Ĥ�пɼ���ԭø�������������ⲻ�������ҷ���������ø��Ѫ����-���ǽ��紦��Ⱦɫ���Լ��ء�������Щ�о������������Թؽ������ڼ��ɲ�����������ø����������ϸ��Ҳ������һ���̡����⣬���������뽺ԭø����������ͬʱ�����Ϊ��������RA��Ĥϸ���м��������뽺ԭøת¼�Ļ��Ʋ�ͬ��
������ЧӦ����һ������ԭø���ڵĵ���Ҳ����ϸ�����ӽ鵼�ġ�����IL-1��������������-��������Ч���յ��������ܵ�ϸ�����Ӵ̼�����Сʱ�ڣ���ԭømRNA���ɳ��־ۼ����������ӡ���������IL-1��������������-���̼��Ļ�Ĥϸ����IFN-�ÿɼ����佺ԭø�Ļ��ԡ����˸���Ȥ���ǣ�IL-1��������������-��֮�������ò�����ʹ��ԭø����ı����½�����������TIMP�IJ������о�������IFN-�ÿ�������������IL-1�鵼�ļ������صIJ��������ڼ��������ǽ�ԭø��Ч�ļ�����������Һ�м������������ļ��ٿ��ܻ�Ӱ�콺ԭø�Ļ��ԡ�ͬ����IFN-��Ҳ������������������-���鵼�Ľ�ԭø�IJ������������е����û����в������
�۽�������ø��֯���Ƽ�(TIMP)��Ŀǰ��TIMP��RA�еĵ������û���֪֮���١���һЩ�䶳�Ļ�Ĥ��֯��ԭλ�ӽ��о���ʾ��RA����Ĥ����㺬�д�����TIMP-1 mRNA���뽺ԭø�෴���й�TIMP����ı�����RA��OAʮ�����ơ�Ҳ����˵��TIMP�뽺ԭø�ı����ڷ����Թؽ��ױ�RA���ߡ�����Ҳ������RA�����ƻ����ܵ���ʴ��һ�ֻ��ƣ���RA�в��������Ľ�������ø�ڸ���TIMP�����ǵ����á�
�ý�ԭø��TIMP�����Կ���Ի�Ĥ��֯������ӫ��Ⱦɫ�������ʾ��Ĥ�������Ժϳ������ֵ��ס����⣬IL-1��������������-����Ȼ�����������Ӽ������صIJ��������Ƕ�TIMP-1��������Ӱ��������
�ܰ��װ��ᵰ��ø������֯����ø����֯����ø��һ����й㷺ˮ����Եİ��װ��ᵰ��ø�����������ڢ��͢��ͽ�ԭ�Լ������ǡ���MMPsһ������֯����øҲ�ܵ�ϸ�����Ӻ�ԭ������(ras)�ĵ��ء�IL-1��������������-�������յ�����ά����Ĥϸ��������������֯����øL��ԭλ�ӽ����о���ʾ��RA��Ĥ����֯����øB��L�ı���ر���������ʴ�IJ�λ����֯����øK���ǽ����·��ֵ�һ�ְ��װ��ᵰ��ø�������е���֯����ø�������ж��ص����ã����ɽ�����ͽ�ԭ��RA��Ĥ��֯�ľ���ϸ���ͳ���άϸ�����ɱ�����֯����øK����֤ʵ��֯����ø��Ϊ���ƻ��Ľ��ʣ���Ϊ�������Թؽ��Ķ���ģ���з��ְ��װ������Ƽ����Լ��١�
(2)�ֲ�����ʴ�Ļ��ƣ�RA�ķ���ѧ�ĸı�������ؽڴ����ֹ��ʼ��١������¹ǵľ����Թ���ʴ��Ѫ������Ϯ�ؽڱ�Ե�����ж����о��������йؾֲ��Ĺ���ʴ���ż����Ľ�չ�����أ�һ����˵�뼲�������س̶���ء�
��RA�ֲ�����ʴ��ϸ�����ƣ�����֤����ʾ������������״̬���ƹ�ϸ����Ҫ����������á��������ڵ���ϸ��/����ϸ����ǰ�壬ͨ��������ص������ء����ʽ�������ø����֯����øK�Ϳ���ʯ������ø��ɹ����յ����á���RA������ʯ������ø(TRAP)��һ���ƹ�ϸ���ı����������ƹ�ϸ�����档��˵���ƹ�ϸ��������RA����ʴ������һ�����á����⣬�ƹ�ϸ������ǰ������ͬ��ǰ�߱��オ�������壬�����������ļ��ؽ����ؽ�ϣ�ʹ���ƹ�ϸ�������յ������ܵ����ơ�
�Ĺ�ϸ������ʶԵ���ø�Ĺ����б������á��ֲ�����ʴ�ĵ�һ������ļ���ֻ������ƹ�ϸ�����͵�ϸ�����ڹ�������ʴ�IJ�λ���е��͵Ķ�˾�ϸ�������ɱ������г�����ƹ�ϸ��������Щ���������������ø����֯����øK�ͽ��������塣�ڽ�Ѫ���躬�д����ľ���ϸ�������Dz���IL-1��������������-����������Դ��Tϸ����ϸ������IL-17�ȵ����Խ��ʣ�����˾�ϸ���ֻ����ƹ�ϸ�������ݶԶ���ģ�͵��о����֣��������ƹ�ϸ���ֻ����ӵ������osteoprotegerin����ֹ���ܵ���ʴ�����á�
�����ԵĹ�������Ҫ�������յĹ������γɵĹ�����֮�����������һ�ֶ�̬ƽ�⣬��RA��������ƽ�ⱻ�ƻ���ȷ���Ƿ����ƹ�ϸ�����������͵�ϸ����ɾֲ������յ��³��ֹ���ʴ����������RA�ֲ��Ƕ�ʧ�����û�����һ���ؼ���
�ڵ����ƹ�ϸ���ֻ��ͻ�����ӣ�������Խ��Խ���֤�ݱ�����ϸ�����Ӳ�������ƹ�ϸ���ķֻ��ͻ����������ֱ���������ƹ�ϸ��ǰ���յ��������ͷֻ������ӣ�����M-CSF��IL-6��IL-11��IL-1����IL-1�º�������������-���ȡ������������Ӽ�ӵز������ƹ�ϸ����һ���̣�������״���ټ��ء����״���ټ�����صĶ��ġ�1��25(OH)2ά����D3��ǰ������E2��IL-11���Ƽ��غ���Ƥ�ʼ��صȡ����˸���Ȥ���ǣ�IL-1����IL-1�¿���ֱ���������ƹ�ϸ������������������ ��ͨ���������ƹ�ϸ����ǰ���ӵ�����ǿ�ƹ�ϸ�����Ե����á�
�������һ�ֱ�����Ϊ�ƹ�ϸ���ֻ�����(osteoclast differentiation factor��ODF)Ҳ�г�֮Ϊosteoprotegerin����(OPGL)������������������ص��յ�����ϸ�����ӣ����Ƿֻ��ƹ�ϸ����Ч�ĵ��ڼ������ɻ�Ĥ�г���ά��ϸ�����ڵġ�����������������������������Ĥ��ϳ�Ա��ODF��Ҫ���ƹ�ϸ���ij��������������á��ɹ�ϸ���ͻ��Tϸ��Ҳ���Բ���ODF������Tϸ�����ܶ�RA���ƹ�ϸ���ͳɹ�ϸ�����ܵ�ƽ����һ�����á��о���ʾ��������ǿ�ƹ�ϸ���γɻ�����Ե����Ӷ���Ҫͨ���µ�ODF(��OPGL)�ı�����ܲ����鵼���ƹ�ϸ��������ϸ�������á�
����һ�����ӽ�ODF��ΪNF-��B��������弤����(RANKL)����Ϊ�ٽ�Tϸ������������ͻ״ϸ�����ܵ����ӡ��������ֱ�����RANKL/ODF���о����֣�ODF���ź��������NF-��B�����弤����(RA2NK)�����ڶ���ϸ�������������ƹ�ϸ�����ƹ�ǰ��ϸ����ijЩBϸ����Tϸ���Լ���ͻ״ϸ����ODF��RANK������ÿ�ʹǰ��ϸ���ֻ�Ϊ�ƹ�ϸ������Щ���ӵĹ��ȱ������ɹǵ������ա�
���⣬����RANKL/ODF�Ŀ����ԡ�decoy�����壬����Ϊosteoprotegerin(OPG)��OPG�൱���ƹ�ϸ���γ��������ӡ��ڽṹ������RANK��ͬ���������ɽ���ƹ�ϸ���ֻ����ӣ���ֹ���߶��ƹ�ϸ���ķֻ�����
�۲���RA�ֲ�����ʴ�����ӣ�RA��Ĥ��֯�������������������������ص����ӣ����а���IL-1a��IL-1�¡�IL-6��IL-11��M-CSF��������������-������RA����ģ�͵��о���ʾ��IL-1��������������-�������Թؽ��ֲ�����ʴ�ķ������зdz���Ҫ�����á����磬�ڽ�ԭ�Թؽ��Ķ���ģ���У������ܹ��к�IL-1�Ŀ��弴����ֹ�Ǻ����ǵ��ƻ������⣬���˷�����Ȼ���������������-�����Լ���RA����֢������ֻ�����IL-1���ܷ�ֹ�������ǵĶ�ʧ������������RA�������ٴ���Ӧ��IL-1��������������-�����Ƽ��ɼ���ؽڵ���֢���֣������Ƴٹ���ʴ�Ľ�չ��
�����һ�о�С���RANKL/ODF��RA�������ջ����е����ý�����������Ӧ��ԭλ�ӽ���RT-PCR���������Ƿ���ȡ��RA��Ĥ��֯�����ij���άϸ���ͻ��CD4 �ܰ�ϸ�����Ա���ODF mRNA��ͬ����ȡ�շ���ģ�RA��Ĥ��֯��CD4 ��CD8 �ܰ�ϸ��Ҳ����ODF mRNA��Ӧ������ӫ���ֱ��֤��RA��Ĥ����RANKL/ODF���Ĵ��ڡ�Kong�����������Թؽ��Ķ���ģ���о�������ODF�����ƹ�ϸ���鵼�Ĺ�����������һ�����ã����磬����շ����Ķ���һ����OPG�����Կ�����Ƥ�ʺ�С���ĹǶ�ʧ����ȫ���ơ�
(3)�������͵�ϸ����RA�ؽ��ƻ��е����ã���RA���ڣ����ڻ�Ĥ�����ϸ�������������ϸ����̬�ķʴ���ɻ�Ĥ������֢��ϸ������IL-1��������������-���̼�𤸽��������Ƥϸ���ı����������ļ��������ϸ������ؽ�ǻ����������ϸ�����ͷŵ���ø����Ҫ�������DZ���ĵ����ǡ���������ȫ�����������߸��������뽺ԭ�ı��㣬����¶������ϸ������IL-1��������������-���Ĵ̼��£����ڴ��ڻ��CD4 Tϸ������£�����ϸ���ͻ�Ĥ����άϸ�����ͷ�MMPs�����Ų���Ľ�չ����Ĥ��֯��ת��Ϊ������֯������һ�������µ�Ѫ�����ɣ����γ�Ѫ���衣������֯������ʴ���ƻ��ڽ������ǺǵĹ��ܡ�
��Ѫ���裺�ؽ����dz��˾��е��Ժ���չ�ԣ����Ҷ������¹���һ�ֱ������ϣ����⻬Ĥ��֯�ͻ�Һ�е��������ʶԹǵ���ʴ��������λ�����DZ�Ե�Ĺǣ�û�����ǵı�����Ϊ�����������ڸô�����Ĥ����ֱ����ǽӴ��������ϸ�����������DZ��档�������¹Dz�ͬ������������û���κα������Ա���ø�ԹǵĽ��⣬Ҳ����ֹ�ֲ�ϸ������ʴ��
RA�����������Թؽ��ײ�֮ͬ�����ڻ�Ĥ��֯������������֮�Ӵ������Ǻ��оֲ���ʴ�ԡ����־����ƻ��Ե���֯����Ϊ��Ѫ���衱����RA����ؽڵķ���ѧ����п��Թ۲쵽Ѫ�����Ե��ʴ�����ԡ�
Ѫ�������֯ѧ�ص���������λ�Ļ�Ĥ��ͬ���ر���������Ҫ���ϸ���Գ����ϸ��Ϊ���������²�ϸ�����١����ֳ����ϸ�����������ص㣺A.������ֳ�Լ���ϸ�������Σ�B.ϸ���˳ʶ����ԣ�C.�߱���ԭ������D.���д��������������ø��mRNA����ȱ��T�ܰ�ϸ��������£�Ѫ�����Ծ�����ʴ���ص㣬����ζ��RA��Ĥϸ���ܹ�����ijЩת��ϸ�����������ڹؽ�������ǣ�����ʴ�Ĺ����У��ɻ�Ĥ��Ѫ����������������Ӻ�ϸ���������ŵ������á���Ѫ������ԣ���֯�ƻ�����������ʽ�������ø�Լ������ܹ����⽺ԭ�͵����ǵĵ���ø������ء�
����Ѫ��������ϸ����̬�IJ�ͬ���ɽ����Ϊ�������ͣ�һ��λ����ʴ��Ѫ����/���ǽ�ϴ�(��Ѫ����/�ǽ�ϴ�)���ɼ������ľ���ϸ���ͳ���άϸ��������Ѫ�ܣ��ּ�����ϸ�������ʣ�������ǵ��ƻ�����һ��Ѫ���賣���ڸ��صĹؽ����ǵı�Ե������̬ѧ�ص������Ե�Ѫ����������֮�䣬�ɼ��ɳ���άϸ������ά��֯���ɵ������������ǵ��ƻ������ԣ�������ά��֯���Ĺ��̡�
Ѫ�����ԭʼϸ���ܹ����ﻬĤϸ��������ϸ���ı��ͺ����ص㣬������Щϸ������Դ��֮ΪѪ����ϸ�������ǵ����γ����Σ����������пɳ������������⣬�뻬Ĥϸ��������ϸ����ȣ���ϸ���ı���߱���VCAM-1��������Tϸ����𤸽���о����֣�Ѫ����ϸ������ijЩ����ϸ�����ص㣬��Ϊ���ɱ����յ����ܰ�ϸ����ԭ��������һ�������ϳ�ø������ǰ������������������-���������Ӽ��塣������ά����Ĥϸ���������������������˸���Ȥ���ǣ�Ѫ����ϸ���뻬Ĥϸ�����ƣ�������NO��ø���������Ǻ���NO��ømRNA��������Ѫ����ϸ�����и������ά����Ĥϸ�����ص㣬��Ϊ���ǿɲ���I�ͽ�ԭ�������Ǣ��ͽ�ԭ�����ң���Ĥϸ��һ��������ϸ���ں��в��ε��ס����ǣ�Ҳ���о�������Ѫ������Դ��ϸ���ɱ�����ͽ�ԭ�������������ǡ��ܵ���˵��Ŀǰ�������в���˵��Ѫ����ϸ������Դ������ϸ���ֻ���ϸ�������dz���ά����Ĥϸ�����������Ǵ�����һ������ϸ��ϵ�����ǣ����ǿɷ��ڽ�ԭø������ֱ����ʴ���ǡ�
�ڳ���ά����Ĥϸ��������ά����Ĥϸ���Ǵ�RA��Ĥ�з���õ���������Ƴ���άϸ����һ����RA��Ĥ��ռ��Ҫλ�õĻ�Ĥϸ���������������ŶԳ���ά����Ĥϸ���о������룬����������һ����Ҫ�����ԣ���ת�����ԡ���Ϊ�Ӻܶ�濴����ϸ������Ϊ����̬�ص�����ǹؽ��ھ��оֲ���ʴ�Ե�������ʵ���ϣ����������ڻ������⣬RA��Ĥϸ�������ֳ�ϸ��ת���ĺܶ����ԣ�������A.����̬�Ͽ���ϸ���˴�����ҳʷĴ��Σ�B.�ʷ�����������������C.�ǽӴ������ƣ�������������п��Կ������ر�����PDGF������Ҫ�ij���ά����Ĥϸ���������Ӵ��ڵ�����£�D.����������Ļ��أ���egr-1��c-fos��c-iun��c-myc��c-sis��c-H-ras�ȣ�E.�Ե���¡��ѿ�¡��ʽ��ֳ��F.����ĩ��ת��ø(transferase)������ǿ��G.��ϸ��ͻ�䣬��p53��H-ras��hprt��
��RA�ķ����У�����ת�����Եij���ά����Ĥϸ������ԭ������Ĺ��ȱ���ܹ������������Ӳ������ɹ���ļ��ʽ���ø������ڹؽ��ƻ������з�������Ҫ���á�����Ҫ�����������RA�ؽڲ����ƻ����ã�A.������ֳ��B.�������ֶ����ǻ������ʴ���õ�ø����MMPs���ۺ���ø(aggrecanase)����֯����ø��
������ϸ��������ϸ�����Ժϳɲ����ڽ�ԭ�����뵰�����Լ�����������ʡ�ͬʱ�������ɷ��ڶ���ϸ�����ӣ���IL-1��������������-����IL-6��IL-8�ȣ���ɲ���MMPs��TIMP������������״̬�£���Щϸ�����ӡ�ø�����Ƽ�֮�䱣��ƽ�⣬�������Ǽ��ʵIJ������ƻ�����ά�������Ĵ�л���ܡ�����RA������MMP�ʹ�����ϸ�����Ӳ��������ӣ�������Ǽ��ʵ��ƻ���
��RA��IL-1��������������-����TGF-�µȶ���ϸ�����ӶԵ���ø�IJ������ŵ��ص����á���Щϸ�����Ӵ��������λ�ڻ�Ĥ�ľ���ϸ�����ڵġ�����ϸ������Щϸ�����ӵ�Ӧ��һ�������Ϊ��ԭ�͵����Ǻϳɵļ��٣���һ�������Ϊ�̼���ԭø�ͼ������غϳɵ����ӣ��������߿ɽ��������еĢ��ͽ�ԭ�͵����ǡ�
����֪RA��Ĥ��֯�е�ϸ�����������������ӡ����У�RA��֯�ƻ��Ļ���֮һ����ϸ��������������ϸ������
��Tϸ���;���ϸ������RA�У��ж������͵�ϸ�������˵�����֯�ƻ��ķ�������(�����ǵ������ǵ���ʴ)�����У�RA����Ĥ�е�Tϸ���;���ϸ������ֱ�ӻ���յ�ø�ϳɵġ�downstream��ЧӦ�����ƻ���֯�ĸ���ϸ�����ӡ�
��ȻT�ܰ�ϸ���ѱ�֤��������RA�ķ��������������ڷ��������е������в�ʮ����ȷ������ϸ����Ѫ��������һ����Ҫ��ϸ������Ϊ���ǿ��ͷŶ��֣�����֢��ϸ�����ӣ���������������-����IL-1�º�IL-17����Щϸ�����Ӳ����յ�����ά����Ĥϸ������MMP���ƹ�ϸ��OPGL�ı��MMPs��������ǵĽ��⣬��OPGL�յ��ƹ�ϸ���ij��죬����ǵ������ա�
��RA����Ĥ��ѪҺ�еľ���ϸ���ɼ�һ������(NO)��ˮƽ���ߡ����⣬����ϸ�������κ�ϸ�����ܰ�ϸ����NKϸ������Ƥϸ�����ɳ���������NO��ø����������NO��ø�����ã�NO�ɽ鵼����ϸ���ڵ�һЩ��ԭ�������ϸ�������ң�NO��������������ϸ���ĵ���������Ӱ��Th1��Th2ϸ���ı������ڹؽ���֯���ƻ���������һ�����á�
�о����֣�RA��Ĥ�е�Tϸ���ܲ���ODF�������߿ɼ����������Щ��RA�ֲ�����ʴ�ķ����������õ�ϸ�������ң�����Tϸ����ϸ������Ҳ�е����ƹ�ϸ���ֻ������á����磬IL-17����RA��Ĥ��֯��Th1��Th0ϸ�������ģ�������RA��Һ�С��ڶ���ģ���У�IL-17���ֳ��ܴ̼��ƹ�ϸ���ķֻ���IL-15����һ��RA��ĤTϸ��������ϸ�����ӣ��������������յ��ƹ�ϸ���Ļ������෴��IL-18�����ƹ�ϸ����ϸ���ͻ�ľ���ϸ�������ģ���ͨ���յ�Tϸ������GM-CSF�����������ƹ�ϸ���ķֻ���
����������ϸ������������ϸ����RA�б��ֳ����Ե����һ�(compartmentalization)������ֳ�Ļ�Ĥ��֯��ֻ�м���������������ϸ�������ڻ�Һ����������Ҫ����ɳɷ֡����ڳ����������һ���ԭ���в��������Ȼ��������ϸ���ڻ�Ĥ�в�������Ҫ�����ã��������Ƕ����ǵ��ƻ�����ռ��ͻ����λ�á���������ϸ��ͨ�������ɻ������ڲ�ԭ�塣��������ϸ���ڵ�ø������������һ�����ӣ����²�������������ţ�ͬʱ�����������绯ø�γɵĹ�����������������ſ���ת�Ƶ��ӡ�������Щ����л������и߶��ԡ���RA��Һ�з��ֻ�����ˮƽ���ߣ��������ǶԹؽ���֯���ƻ������в������
Ŀǰ��֪��������ϸ���ɱ���Һ������IL-8��GS-CSF�����߸������һЩ���Ӽ���������ɲ��������߸���������ͷ�ϸ���ں��еĸ����ܾ�ø��(�����������ø���ܾ�ø�����Ե���ø����ԭø�Ͱ�����ø)�������������������ǺͶԹǾ����ƻ��Ե������ɻ������У����߸�����������������ϲ㣬��������������ϸ��ֱ�����������ǣ����ұ��ھۼ��л��Եĵ���ø������л��������Dz�����ʴ���á�
5.���ʪ�ؽ��������Ƶ�ģʽ ����Խ��Խ���ϸ�����ӱ����֣��Լ���TCR�;���ϸ��/����άϸ�������о������룬ʹ���о�����������ͳ��RA�������Ƶ�ģʽ���������һ������ͼ�����ھ���ϸ��/����άϸ���߶Ȼ������£�RA��Ĥ��֯���ֵ�Tϸ��Ӧ��Ӧ��Ŀǰһ����Ϊ��RA����ʼ���п�������Tϸ���鵼��һ��ԭ�����ԵĹ��̡��¹ؽ���ԭ��δ���֣��п����Ƿ�ת¼������ij��ϸ���IJ�������������壬����ԭ�塢��֦�˾���������ȡ�����RA���߶��ԣ���������Tϸ����Ӧ�𣬵���ϸ�����ӵķ��ڣ������ļ������������ϸ��������ϸ����Bϸ���ͼ�����Tϸ�����ڵĶ�������ϸ�������Ǿ��й㷺�Ŀ�ԭ�����ԡ�������ȷ�����ֻ�Ϊ3��RA����ģʽ����������Ҫ���ǣ������������ʶ����3��ģʽֻ�������������Ի�Ĥ��չ�ij����Σ����Ǽ�������ʼ�Ρ�ͬʱ����Ӧ���˽���3��ģʽ�����Ǹ��Թ����ģ����ǿ�������õ�(ͼ4)��
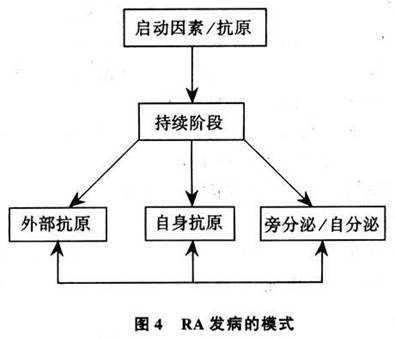
(1)Tϸ���鵼������Ӧ�������Ĥ��֯�г�������ij���¹ؽ���������Ӧ����������ʵ����֧����һ�۵㡣���磬��ķ���Ĺؽ�����RAʮ�����ƣ�����ķ�����²���ԭ���������忹ԭ��HLA-DR�ı����ܶ��ڻ�Ĥ�����ϸ���;���ϸ���ܸߣ���˵�����ڻ�Ծ�Ŀ�ԭ�ݳʻ�����⣬���Ի�Һ�ͳ��������֯��Tϸ��������ϸ�������ı�����MHC��ԭ��ת���������塣λ�ڡ�������(transitional areas)�����ܰ�ϸ���븻��HLA-DR�ĸ���ϸ��������ء���Щ�ϸ���IJ����п����յ�MHC��ԭ�ı����ʹ��Ĥ�����ϸ������������֧��Bϸ����������ֻ��������ص���������ȫ���ܰͷ��ƺͻ�����A�����Tϸ�������������ƶ�RA����ĸ�����һ�����ã���һ��ʵҲ֧��Tϸ���鵼������Ӧ����RA������Ҫ���á�
Tϸ���鵼������Ӧ�����RA��Ĥ����һ�۵�������Ͽ��Խ���RA��������������������T�ܰ�ϸ���ľۼ����ڻ�Ĥ�����ϸ��������������Bϸ�����Ȼ�Ծ���ֲ������������塣
������Ŀǰ��һЩ�����в�������һģʽ���ͣ��ٹؽ��ڲ����Ŀ����Խ�����Դ�ڷ�Tϸ�����������ֶμ�T�ܰ�ϸ��������ϸ�����ӵ������dz��٣�������Tϸ���鵼����������������Tϸ���鵼�ļ�����Ҳ�ɼ���������Ĥ��ˡ�Ƥ���ijٷ��ͳ�����Ӧ�����ԭ�շ��������ȡ���Щ����ij���ʹ���о��������RA��������������ģʽ��
(2)������Ӧ��Tϸ����RA�����Թؽ����˿����ǶԿ�ԭӦ��Ľ�������뼲������ʼ�β�ͬ�����������������Լ�����Ҳ����������Ƶķ������ƣ����磬
���������Լ�״�������Ƕ�ij���Ʋⲡ������Ϯ�����ʵ�������Ӧ�𣬵��¾ֲ�����IFN-�ã������յ���״��ϸ������HLA-DR��ʹ֮��Ϊ���߹����Ķ������Ϊ��ԭ�ݳ�ϸ����Я��HLA-DR�Ĵ̼�ϸ��������T�ܰ�ϸ��֮��ķ�Ӧ����������������ܰ�ϸ����Ӧ(autologous mixed leukocyte reaction��AMLR)��RA���ߵĻ�Ĥ�ɳ��־ֲ���AMLR����Ҫ���������ݣ��ٸ���ϸ�����ӵ�RA��Ĥ��AMLR�е�����dz����ƣ�������IL-2��IFN-�õ�����Tϸ����ϸ�����������dz��٣���RA�ؽ�Һ�м���ϸ������T�ܰ�ϸ����AMLR������NK��ϸ�����������ԣ��۹ؽ�ǻ�ؽڻ�Ĥ�к��ж���DZ�ڵĴ̼�ϸ����������Ӧ��ϸ����λ�÷dz��ӽ�������Ӧ��ϸ������A�ͻ�Ĥϸ������ͻ״ϸ����������AMLR����Ч�Ĵ̼��
����MHC��ԭ�⣬���Ի�Ĥ���еĻ�ĤTϸ������ֱ���������������ԭ����Ӧ�𣬲����ͷ�������Tϸ���Ļ����С���Ԣ��ͽ�ԭ������Ӧ��������е�һ�����ӡ����⣬Ҳ��ͨ������ģ��ķ�ʽʹ������Ӧ��Tϸ���ܵ��̼������磬���ݿ˵��ס������Ǻ�EB��������ͨ�����ַ�ʽ��������Ӧ��ġ�
(3)�Է���/�Է���ģʽ��ǰ���ἰ��RA�����ε����ַ������Ƶ�ģʽ��ҪΧ����T�ܰ�ϸ��������Щģʽ�У�Tϸ���IJ���ֲ���������֯�У�ֱ�Ӵ̼���Ĥ������µľ���ϸ���ͻ�Ĥϸ�����յ�𤸽���ӱ����ں�ëϸѪ�ܸ���Ƥϸ����������ͨ��Bϸ����������ֻ��̼��ֲ������IJ���������������ǰ�������о����ֹؽ�ǻ�ڻ��Tϸ���IJ��ﲻ�������٣��������������Ҳ����(��11)��
��֮�෴����Ĥ�ھ�����ϸ���ͳ���ά��ϸ�����ڵ�ϸ�����ӣ���IL-1��������������-����IL-6��GM-CSF��M-CSF��TGF�¡�ǰ�����ء����嵰�ס�TIMP����ԭø�ȣ��ڻ�Ĥ��֯�ͻ�Һ�еĺ���ʮ�ַḻ�����ݳ��ṹ������ϸ������HLA-DR�ı����ʾ��Щϸ�����л�ı��͡���Щ������RA�����Ի�Ĥ������Tϸ�������²�������һ��ͳ�۵�Ӧ�������ı䡣Ҳ����˵���ؽڳ�����ڽ��ľ���ϸ���ͻ�Ĥ����ά��ϸ�����Է��ڻ��Է��ڵ���ʽ����������ϸ�����ӣ�ά�ֲ��ٽ���Ĥ��֢�ķ����뷢չ���ڹؽ�ǻ����ʶ������ֲ�����һ���̵�ϸ�����ӣ����ܽ��ͻ�Ĥ�����ϸ����������HLA-DR���յ��ͻ�Ĥ����Ѫ�ܵ��γɡ�
ͼ5�Ǵ����ڻ�Ĥϸ���临�ӵ�ϸ����������ʾ��ͼ���漰����ϸ���ͳ���άϸ��������Tϸ�����ڵ�ϸ���������Լ�⣬����ϸ�������Ƿ���뼲���Ĺ����в������
IL-1��������������-�������ɻ�Ĥ������ϸ�����ڣ����ǿ��Դ̼�����ά��ϸ��������������IL-6��GM-CSF������������غͽ�ԭø��ЧӦ���ӵķ��ڡ�GM-CSF���ɻ�Ĥ������ϸ���Լ���IL-1�»�������������-���̼��µij���ά����Ĥϸ�������ģ�����IL-1��������������-����IL-8�������յ������ر�����������������-����Эͬ�£�GM-CSF���������Ӿ���ϸ���͵���ϸ������HLA-DR�ı������ά����Ĥϸ�������Է��ڷ�����������ͨ�����ڳ���άϸ����������(FGF)�����������ĵ��ڡ�����ϸ���ͳ���άϸ�������ľֲ�ϸ�����ӻ���������Tϸ���������ʶȵ���Tϸ���Ļ��ԡ�Bϸ���Ļ�Լ�RF�IJ����п����Ƿ�Tϸ�����û��ƵĽ������Ϊת������������FGF��PDGF��ϸ���������Է�����ʽ�Ĵ̼�������˵����ת�����ԵĻ�Ĥϸ��Ҳ�����Է���/�Է��ڵ��ص㡣���Ʋ⣬��һģʽ����һ���ص㣬��ϸ�������Էǿ�ԭ����ķ�ʽ����Tϸ������ؽڻ�Ĥ��
ϸ�����ӵ����Ƽ����Է���/�Է���ģʽ��Ҳ������һ�����ã���Ϊ��������������һ����Ҫ�ĵ��ػ�Ĥ��֢��Ӧ�������ڻ�����̬���ơ���������Щ���Ƽ���������Ч����ֹ������֢��ϸ�����ӵ����á����磬�������Ͻ���IL-1Ra�ܹ���RA�ķ�չ��һ�����谭���ã�����ʵ�ϣ����ܹؽ����д�����IL-1Ra����Ĥ��֢�Գ�����չ��
(4)Tϸ��-����ϸ��-����άϸ�������3���й�RA�ķ�������ģʽʵ���ϰ���һϵ�еĻ���ԭ�������ۡ�Ŀǰ��Ϊ��RA��Ĥ��֢�ij���������������ģʽ��ͬ��ɵģ�����Tϸ��������ϸ���ͳ���άϸ������õĽ����
�����о������������Ƶ�Ŀ����Ϊ���ܹ���ȡ��������������ȫ������ƴ�ʩ����ΪRA�漰����Щϸ���֮��Ĺ�ϵ���۸��ӣ�������������κ�һ��ģʽ�����ƶ�������ȡ��ʮ���������Ч���������ٴ���Ӧ�����Tϸ�������Ե�����ȡ����һЩ�ɼ���������Ȼ��һ���ֻ��߶����Ƶķ�Ӧ�ͼ����ĸ��Ƴ̶���Խϲ���磬������A��һ����Ҫ���Tϸ��������ҩ��ٴ���ֻ��һС���ֻ��߿��Դﵽ50%�ĸ��ơ�Ҳ����������RA�����ƻ���һ�������ã���Ϊ��RA�����ڿ��Գ���Tϸ���鵼�����ˣ���ʱʹ�����Tϸ�������ƻ��������յ����õ�Ч����
6.���ʪ�ؽ��Ķ���ģ�� ���ʪ�ؽ��Ķ���ģ��Ϊ�����о�RA�IJ��������ƺ����Ʒ����ṩ�������Ĺ��ߡ���1892��Lucet�״�������ʵ���յ���������ؽ�������������ģ����������Ϊ��֢�Թؽ��������Թؽ����о������ڿ��ƶ����Ӵ���ֳ�������£�ʹ�ڽ���ϵ���յ��������Ի�Ĥ�׳�Ϊ���ܡ���Ȼһ�ֶ���ģ��ֻ��ģ��һ���������߲���ȫò�����ǣ������ܹ��ṩ�й����������Լ�������֯ѧ����������ѧ���Ŵ�ѧ�ȷ������Ҫ���ϣ����ң�����ģ�Ͷ��о��µ����Ʒ���Ҳ������Ҫ�����á���Ϊ�����RA����ģ��Ӧ�þ߱�����һЩ���������ٴ��������ͷ���ѧ���ص�������RA���ƣ��ھ������ٵľ߱���RA���ص㣻�����ּ����еĶ���Ʒϵ���õ����Ҽ۸���ˣ������ֶ�����Ը�Ч�ط�ֳ���ݿ������̼�������Ȼ�������̣�������⼲�������߹��ܵı仯���߿���ģ��RA���߶����Ƶķ�Ӧ��
ĿǰRA�Ķ���ģ���������Թؽ���(adjuvant arthritis��AA)����ԭ�Թؽ���(collagen type��CIA)�������ϸ���ڳɷ�(streptococcal cell wall fragments��SCWF)�յ��Ĺؽ��ס��������յ��Ĺؽ��ס�������(pristane)�յ��Ĺؽ��ס���ת¼�����յ��Ĺؽ��ס�����˾����յ��Ĺؽ���֧ԭ��ؽ��ס���Ȼû�е�һ��ϵͳ���Է�ӳRA�������ܵ���˵������ģ�����о���֢�Ĺ��̺��ֿ������ӵ����������˼�Ϊ��Ҫ�����á�������ܼ�����Ҫ�Ķ���ģ��(��12)��

(1)��ԭ�Թؽ��ף��ڴ���С��ͷ������鳤�ද�����Ʒϵ������Ƥ��ע�������ȫ���������Ģ��ͽ�ԭ�����յ��ؽ��ij��֡�����Trentham������1977���ڳ���������ԭ�Ŀ�Ѫ�������ʱżȻ���ֵġ�CIA�ڹؽ��Ķ���ģ���бȽ϶��أ���Ϊ������ͨ�������������ǵ���������Դ�����忹ԭ�����������߷�Ӧ���յ������ķ��������ң�����������ע�䴿���Ŀ����ͽ�ԭ����ɲ�����ȵĹؽ��ס���10��14����ܢ��ͽ�ԭ���ߵ�С��90%��չΪ��ؽ��ס��ڹؽ��������2���ڣ�С�����Ѫ�����γɺ�Ѫ���γ�(angiopoiesis)�������¹ؽ����Ǽ�����֯����ʴ���ƻ������ͽ�ԭ��Ҫ�������������У���Ҳ�ɳ����ڶ����Ͷ�ǰͥ�ȹؽ��ⲿλ����Ҳ���Խ��͢��ͽ�ԭ�Ĺؽ���ЧӦ��CIA���ص��ǿ��Բ��������ͽ�ԭ���壬���ɷ�չΪ�ٷ��ͳ�����Ӧ���˹ؽ�������Tϸ����֤�ݰ�����������ȱ��Ķ��ﲻ���յ����ؽ��ף��ڸ��迹Tϸ����CD4����Tϸ������������ƹؽ��ף��۶Ԣ��ͽ�ԭ�����Tϸ����¡���Դ��ݼ�����
(2)�����ϸ���ڳɷ��յ��Ĺؽ��ף�Cromartie������1977���״������������ϸ���ڳɷ��յ��Ĺؽ�����ģ�͡����͵�SCW�ؽ�������һ�θ���Ƥ��ע�����ϸ�����Ķ���Ƭ�ε�ˮ����Һ�շ��ġ�һ�㶯�������ߺ�24h�ڣ�100%��Ʒϵ�ɳ������ܹؽڵļ�����֢���֣�����Ҫ������SCWƬ�γ����ڻ�Ĥ����ɵġ���������Ƿ���Tϸ���Եģ����벹��ļ�����ء�һ�����3��5�졣�����ߺ�2��3���ڹؽ���֢״���ٴζ����������¡����һ��һ���Ե���֢��ͬ���ڶ��ε����Ի�Ĥ������Tϸ���Եģ������а���Ѫ�����γɡ�Ѫ���γɡ�������ǵ���ʴ�ؽڵ��ƻ����ؽ���ı�����RA���ƣ�������Сϸ����ƶѪ��������IL-2�������٣�����SCW�ؽ�����ģ��ȱ���ߵζȵ����ʪ���ӣ�����û�����ʪ��ڵ��γɡ�SCW�ؽ���NSAID�������������װ����ʺ���Ƥ�ʼ����з�Ӧ�����ǶԽ��Ƽ�����ù���ķ�Ӧ�
(3)�����Թؽ��ף�Pearson��40��ǰ�״������������Թؽ��ס�һ�θ���Ƥ��ע��һ�ְ�����ɱ����˷�֦�˾���M.phlei��M.butyricum�������еĻ���Һͨ�����շ��ؽ��ס���SCW�ؽ���һ�������Ŵ�������صĶ����������Ʒϵʮ����Ҫ�������н�˸˾���65kDӦ�����������²���ԭ�����������еĵ�������������ԭ�ɷ����ơ��������˼�AA����Ĺؽ����Ǻͻ�Ĥ��ϴ������������Ƶ���Դ��Ӧ�����ס������Թؽ�����֢��������Tϸ���ġ���ò���ص��ٴ��ص�����ؽ��ܵ���ʴ���ؽ�ǿֱ�����ؼ��ᡢʳ�����ˡ�
Ƣ������ϸ�����ࡢ���ȡ������ڷ�Ӧ�����ߡ���
������Ƥ�
ǰ����Ĥ������Ĥ��״���ס���Ĥ�ס�
�������
���(��13)��
ȱ���Ƿ����졢���̵�һ�����о���Щ���������ڼ��������ش���һ�������ѡ����⣬CIA�Ķ���ģ���У����ֵĹؽ�ǿֱ���������������������ۺ����ı��֡�
�����Թؽ�����RA�е����ã������øö���ģ���о�RA�IJ�������ѧ����������������ؽڵ��ƻ���������ʶ��������������Լ����Ļ����Լ�Ѱ�ҿ��ɻ���
������Griffiths������ͬ������CIA����ģ�ͣ�������4����ؽ���֢���س̶���ص��µ�������״�����������������˸���Ȥ�ĺ�ѡ������ǰ�����غϳ�ø������C5��PDGF��VEGF�������������Ӽ����Ա�ȡ����ң�������һ���µ�������״������(Ciaa3)�������뿹��ԭ����IJ�����
7.���� ���ʪ�ؽ��IJ�����Ҫ�����ڹؽ�ǻ����Щ���˰��йؽ������(ͼ6)���䲡���ص��ǣ�����֢ϸ�����������ܰ������γɣ���Ѫ���ף������ʪ����ѿ���γɡ�
(1)�����ؽ���֯����Ĥ�dz��ڹؽ��������һ����֯�����������ǹؽ����ǣ�����汻Aϸ����Bϸ����һ�������ǣ�����ΪAϸ�����ɸ��巢�����ڹ̶��ڸô��ľ���ϸ���ܱ��������������һ���ɳ���άϸ���ܱ�����Bϸ����Bϸ�������зḻ��ëϸѪ�ܺ�ϸ���������ǵ�ͨ�Ժܸߡ�����������֬��Ϊ���Ľ����֯��Aϸ���к�С��ϸ��ͻ�𣬺��зḻ����ø�壬���������ú�ǿ���ܹ����ǻ��˥����֯��Bϸ�������зḻ��Բ�λ���Բ��С���壬�ܲ�����ԭ����άճ�����ס���ճ������������Ȼ��ʣ����ͻ������á�ͬʱҲ���д������ʺϳ�ø�ͻ��ʷֽ�ø��Ѫ�ܹ������������й���ˮ���ܡ�
�ؽ����Ǹ����������¹ǵı��档����������ϸ�������ǻ��ʹ��ɣ�����ϸ���ϳɼ����ڻ��ʡ�������Ҫ�ɢ��ͽ�ԭ�������Ǻ�ˮ��ɡ��ؽ�������Ѫ�ܺ��ܰͣ�������ͨ����ĤҺ��ȡӪ���ġ�
(2)��Ĥ��֢��Ӧ��
�ٳ���ϸ�����������ʪ�ؽ��Ļ�Ĥ����ϸ����������1��2������8��10�㡣����ϸ�����������ӣ�����A��ϸ������Ϊ����������A��Bϸ����������߶ȱ��D�ԭ��
������Ѫ�ܺ�����ϸ���������ʪ�ؽ���Ĥ��Ѫ�������������ӣ�������Ѫ����ҪΪëϸѪ�ܼ����и���״��Ƥϸ����ëϸѪ�ܺ������������ڻ�Ĥ�����Щ����״��Ƥϸ���߶ȱ������ϸ��𤸽���Ӻ�ϸ�����ӡ������ܰ�ϸ���ۼ���Ѫ����Χ��������CD4 Tϸ��Ϊ��������CD8 Tϸ�����γ��������ṹ���ɼ�����Bϸ�����������ģ���������ϸ��ɢ�����ܰ������ܱ�֮�䡣����ϸ���ֲ���������Ĥ��������ͻ״ϸ��ɢ�����ܰ������кͳ���ϸ���㡣���ʪ�ؽ���Ĥ�ڸ���ϸ��������MHC������ӣ�������ˮƽ�������������˵Ļ�Ĥ��
��Ѫ������γɣ����ڻ�Ĥ����ϸ����������Ѫ�ܡ�������֢ϸ�������ܰ������γɣ�ʹ��Ĥ������ë�������������Ļ�Ĥ�γ�Ѫ����ͻ��ؽ�ǻ�ڡ�
(3)���Ǻǵ��ƻ������ʪ�ؽ��ؽ����ǵ��ƻ���ʼ�ڻ�Ĥ�����ǵĽ��Ӵ����˴���Ĥ����Ѫ�ܡ�ϸ���ɷ��������࣬�γ�Ѫ���貢�Թؽ����DZ�Ե���������������ӣ�����Ѫ����/���ǽ�ϡ�Ѫ������������A��B��ϸ�����������֢ϸ�����ڵ���ø(��Ҫ�ǻ��ʽ�������ø)��ϸ������(IL-1��������������-����)���������Խ��ʣ��ƻ����ڵ����ǣ�ʹ����ϸ�����ڻ��ʼ��٣���ԭ�͵����DZ����ʽ�������ø�ƻ����ƹ�ϸ����������յ��¹ؽ����Ǻǵ��ƻ���
(4)�ؽ�ǻ��Һ(ͼ7)�������ؽ�ǻ����������ĤҺ��ϥ�ؽڻ�Һ������3.5ml���ʲݻ�ɫ��������������������ϸ�������ؽ����á����ʪ�ؽ��ײ��˹ؽ�ǻ�ɳ��ִ�����Һ�������ڼ����ڡ���Һ�к��д�����֢ϸ������ҪΪ������ϸ�������ɼ�������Tϸ���������ĵ���/����ϸ������ͻ״ϸ����Bϸ�����ɲ����ϸ�����Ӽ����������塣
 ����
����
���ƣ�
1.���Ƹ��� ������������Ч�Ʒ���������Ҫ�ǻ�����ʹ�����ƹؽڹ��ܣ����ٸ����������ܿ��Ƽ����ķ�չ��Ԥ�����Ρ�ȫ��֢״���ؼ��ؽ�����ʱӦ�Դ���Ϣ����֢״��������Ϊֹ�����Լ������ѹ����ؽ�����ʹ���������Դ�������ؽڷ��ö���Ϊ��Ӳ��ֻҪ���˿������ܣ���Ӧ�����й��ɵ����������Ĺؽڶ������Ӧ�������˱��ⷴ����ð���Ⱦ��������ز��顣ָ�����˺�����ҩ���Է���������������ʹ��������⣬�����������˵���������ƣ�͡���ַ��������־���������ó��ھ�ס��ʪ����ȡ�
�����ٴ������о������ķ�չ�����Ƕ����ʪ�ؽ����˽�Խ��Խ���룬ͬʱҲ�ƶ������Ƶ�Ѹ�ٷ�չ���Ӵ�ͳ�ķ���̴�����ҩ��ϸ����ҩ����������Ƽ����ٵ���������֢����ڵ������Ƽ����Լ�������Ե�����Ѫ��ϸ����ֲ�ͻ������ơ����ʪ�ؽ������ƵIJ���Ҳ����������ʶ����߷�������Ҫ��ת�䣬�����ת�����Ҳ��һ�����淴ӳ��ѭ֤ҽѧ���ִ�ҽѧ��չ��������á�
���ʪ�ؽ���(rheumatoid arthriris��RA)��һ������ϵͳ�����Լ����������ܹؽڻ�Ĥ��Ϊ��Ҫ���֡��������ƽ��������27�꣬���ٴ����ִӹؽ�֢״���ؽ�����֣�������أ����˶��졣���Ǽ������еIJ��˶������ܹؽ���ʹ֮�࣬�������еIJ��˶����йؽڹ��ܲ�ͬ�̶ȵ�ɥʧ�����ʪ�ؽ�����������ص�������⣬���緢�����ڿ��Թ����IJ��ˣ�10�����35%��50%��ɥʧ������������20�������50%��70%��ͬʱ��RA���˵�������������������Ҳ����ͨ��Ϊ���˹��⽫���༲������Ϊ��5D���������ʡ��������зϡ������ͻ���Ǯ��(discomfort��distress��disability��death��dollar lost)��
��ͳ�����Ʒ�����Ϊ�������Ʒ�������һ��ӽ���������ʼ�����ڣ��������Ƕ�RA����ʶ���㣬ֻ�ܴӼ��Ს��֢״���ֽ������ơ�20����40�����60���������RAʹ������ҩ���ǰ�˾ƥ�֡���70�����һЩ�����Ƶķ���̴�����ҩ��(NSAIDs)�õ���Խ��Խ��ҽ�����Ͽɡ���ʱ��Ϊ����RA�ǵ�������֢��Ӧ��Ϊ�����Եģ�����ʹ�ÿ����������㹻��ֻ�е�����X��鷢�ֹؽ��ƻ�����ʱ����ʹ��������ҩ��������Ʒ������˽�50�ꡣ��20����90�����ǰ����ʪ��ѧ�Һ��ٴ�ҽ���Ѵ�ע�����������ڷ��ֺͷ�ֹ����ҩ��ĸ������ϣ������ٹ�עҩ��Լ����������غ������ֹ����ʱ��һ�����е�˵��������㲻��ʹ����ʵ�������ø��ã����ٲ���ʹ֮��ø�����
��20���͵����ʮ�꿪ʼ����ʪ��ѧ�Ҷ�RA���ƵĹ۵㷢������̵ı仯��ͬʱ���ʪ�ؽ��Ľ��ҲԽ��Խ�á���һʱ�ڼװ�����MTX�Ĺ㷺�����Dz������ֱ仯����Ҫ������֮һ�����������ı䲡��ҩ��(DMARDs)������ʹ���Լ��������ơ���Щҩ��֮������Эͬ���ã��������ڼ��������������̲�ͬ�Ļ��ڣ�ʹ������ĸ���Ӧ���͡����Ž����������Ƽ�(�翹������������-���Ƽ��Ϳ�IL-1Ra�Ƽ���)�ij��֣�RA�������ַ�����һ���µĸ�������֮�������ϵı仯ʹ�����ܹ���������ʹ�����е������ֶΣ��Ӷ����õظ���RA�Ľ�֡�
����������ʪ��ѧ�ҴӴ�������RA���ٴ��о����ܽ������û��һ�����������Ʒ������Ի���ٴ���������������⣬����ֹ�ؽڽṹ����ɥʧ�Ľ��̣���һ���ֲ��˺��緢���ؽ����ǵIJ����涪ʧ���ڲ�������M
RI���Է��ֹؽ���ʴ����������Ҫ���������ͨ�ؽ�ƽƬ�������Ƶĸ���Ӧ�Ͳ���֢�������Ӳ��˵������ʣ���Ωһ��������Ԥ�ⷢ�����عؽ�����ʴ��ؽ��ⲡ��IJ�����һ��������λ��������MHC��HLA-DRB1���ϵ�3���߶ȿɱ�����QKRAA���������У����ٴ��Ͽ���������Ч��Ԥ��Ԥ��ķ����У����������ʾ�(HAQ)���������ʽ(MHAQ)�����ܲ��ԡ������ڷ�Ӧ��(ESR��CRP��)�����ʪ����(RF)��ˮƽ����˳���Ʒ��������ڰ�ο�����ơ�
2.�����ʪ�ؽ��ײ��������
(1)������������Ҫ�ԣ����ʪ�ؽ�����һ�����Բ��������ڶ�ͯ������֮����κ�ʱ�ڷ�����ͨ��������������ͬRA���ߵIJ���ñ�ָ�ƣ�����ÿ���˶�������֮������û�����������ܹ���ȫһ�������ݻ��߲���Ľ�չ������ʱ�����������״̬����֢��Ŀǰ�����Ӱ�졢���幦�ܵ��½�������������ɥʧ�̶ȡ�����ؽڵ��ƻ������������Ĵ�����������ͬ���������Ƶľ���Ŀ����������ͬ�������ƹ����У��ٴ�ҽ������������һ����ս���Ƕ�ÿһλ���ߵľ�����������ۺϵ���ȷ���������ƶ���Ӧ�����Ƽƻ����������õ���ѧ��(���ʪ��ѧ�����ѧ�Ϳ���ҽѧ��)����Ϻͻ��ߵ���ͬ���˽�ߵ���ԸҲ�dz���Ҫ��������������ʱ��Ҫҽ�������϶��ʱ�䡣�û����˽�Ŀǰ�Լ��IJ���Ϳ��ܵ�Ԥ���Լ����ƿ��ܷ����IJ������������ʹ���������Ƶĺ����Ժͱ����ԣ��������Լ����������ƻ��֢״���Ƶ�ͬʱ��Ҫ�е����̶ֳȵ�Σ�ա��ڶԲ�����������ͷ���Ԥ��֮ǰ��Ҫ�˽����м������ʵĺ��塣
�ٲ����ԣ�ָRAȫ���;ֲ�����֢���֣�����Ҫ���ٴ������ǻ�Ĥ�ס�һЩ�ٴ�ָ������������������Ļ�ԣ��磺���ؽ�����ѹʹ�ؽ��������˶���ʹ�����������Ե������������ϰ��������ͼ����ڷ�Ӧ��(ESR��CRP)��������ʪ��ѧ���ŷ����ʪ���˶��и��ԶԼ�����������ķ������������ٴ�ʵ�ʹ����е�Ӧ�ò������㡣RA�������ٴ�������Ѫ���ȣ�ͨ�����������ڶԲ����������
�ڲ��������ԣ���������ָ��A.�����Ļ�Գ������ڽϸ�ˮƽ��B.���ԵĹؽڽṹ������ɥʧ����������ɥʧ������ѧ�쳣����Ҫ�ؽ��û���C.����Ѹ�ٶ��п��ܲ��������Ĺؽڽṹ�ƻ�����������Ľ����
�۲����Ժͼ���ת��֮��Ĺ�ϵ�������ԺͲ���Ŀǰ���ٴ��������Ӧ����������Գ������ڸ�ˮƽ�������������ĺ����������Խǿ��������ַ�����Σ��Խ�����ڶ����ڼ��ɲ��������Բ����Ժ�ǿ���������Ϊ���ٴ���֢����������Ҫǿ�����ǣ���ʹ�����Խ�����Ҳ��������ɥʧ��������ص��������ƣ����Բ��ܽ��Լ��������ܺͼ����ĵͻ�������õ�Զ��ת���������
Ϊ��ʹ�������������㹻����Ϣͬʱ����Ѹ����ɣ�һЩѧ�߽���������������Ӧ����һ�ֹؽڼ���������ESR��CRP����ʹ��(��)���������Բ�����һ��ƣ�Ͷ��ձ���һ�ֹ�������(HAG��MHAQ)������ʹ�õķ����йؽ�������ָ�����ٴ����������ʾ�����ѧ����Ϊ�ӹؽ�ѹʹ����������õ���Ϣ���µ�Ӱ������M
RI�ͳ�������Եò��㣬���ʹ����Щ����ʱ���ܴﵽԤ�ڵ�Ŀ�꣬�������ض��������ʹ���Ѿ��㹻�ˡ����磬������Щ�����ʽ����Է�չ�IJ��ˣ��������п���Ҫ���������IJ��ˣ�ҽ��Ӧ������йؽڼ�����thompsoָ��(������lansburgָ��)ʹ����Խ��ٵĹؽ�����������������Ĥ���ɡ������á�Ҳ�е�ѧ����ΪӰ��ѧ�����������岡�˵�������ý�С���������ǣ�A.��ͬ���ٴ�ҽ����ͬһ��Ӱ����в�ͬ�Ŀ�����B.�����ƻ��ͳ���Ӱ��ѧ�쳣֮����һ��ʱ������C.Ӱ��ѧ�ı�Ͳ��˹ؽڹ��ܵı仯֮����ϵ��ǿ�����Ƕ���ͬһ��������˵�����ڽ���Ӱ��ѧ�Ƚϣ����˽ⲡ��仯�����а����ġ����о�����
Ѫ��YKL40�����������ǵ���39(gp39)��Ũ�ȿ�����Ϊ������ı�־���ȴ�ͳ��ESR��CRP�ã���������ۻ���Ҫ�õ���һ��֤ʵ��
(2)���ʪ�ؽ�������ǰ�Ļ����������������������Ӧ�á����С����š���ȷ����ʵ���С�ȫ��������ߡ�����ͳ��Ϊ����һ��RA���߲����ȷ���������ڹؽڼ���������������ʱ���ʵ���Ҽ�����Ӱ��ѧ��顣������ʪ��ѧѧ���ڡ����ʪ�ؽ�������ָ��2002�桷���Ƽ����ڿ�ʼ����֮ǰ�Ի��߽��л�������(baseline evaluation)(��16)��
(3)���ʪ�ؽ��ײ�����������ÿ�λ��߾���ʱ���ٴ�ҽ���������������Ƿ�����̶ȣ��Դ˾������Ƶķ���(��17)��
�������������ʪ��ѧѧ���Ƽ��IJ���������Եĺ��ı��ͼ��������(DAS)���㷨��
��������ʪ��ѧѧ���Ƽ��IJ���������Եĺ��ı���
A.ѹʹ�ؽ�������¼����ʱѹ�ȺͲ���28���ؽڵ�ѹʹ�ؽ�����Ӧ���ѹʹ�IJ�ͬ���棬��ֻ��¼����ѹʹ��
B.���ؽ���������28�������ؽڵ����������ֻ��¼���ס�
C.���߶�ʹ�����ۣ����������ձ�(ͨ��10cm)��Likert�ּ�����Ŀǰ��ʹˮƽ��
D.���߶Լ�����Ե��������ۣ���AIMS����д��Ŀǰ�����Ӧ�ṩһ���������ձ�(10cm)��Ҳ����Likert�ּ���
E.ҽʦ�Լ�����Ե��������ۣ����������ձ���Likert�ּ�������ҽʦ��¼��
F.���߶��������ܵ����ۣ����õ���AIMS��HAQ��MHIQ��MACTAR�ȡ�
G.�����ڷ�Ӧ��ˮƽ��κ�Ϸ���Ѫ����C��Ӧ���ס�
H.���������(DAS)���㷨��
DAS=0.54() 0.065(SwJ s) 0.33(lnESR) 0.0072(GH)
RAI��Ritchie�ؽ�ָ����
ESR����ϸ�������ʡ�
SwJ s�����ؽ���Ŀ��
GH��ͨ��100mm�������ձ����е�һ�㽡��״̬������
DAS�жϱ���
�ͶȻDAS��2.4�����Ʒ�Ӧ���á�DAS��1.2
�жȻ2.4��DAS��3.7�����Ʒ�Ӧһ��0.6����DAS��1.2
�߶ȻDAS��3.7��������Ӧ ��DAS��0.6
��DAS=���ƺ�DAS-����ǰDAS
���������������ʾ�(HAQ)��
A.���¼�ϴˢ�����ܴ��¹�����ȡ���·���?�����Լ����°�����Ŧ�ۡ����������¹���?����ϴͷ����?
B.���������ܴ�����������������֧����?
C.��ʳ�������������?���ܾ�һ����ˮ��������?
D.��·�����ܵ�����ƽ������·��?
E.����������ϴȫ����������?����������ϴ����?���ܿ�������ˮ��ͷ��?����ȥ��������Ͱ������Ͱ��������?
F.��ࣺ������ͷ����?���ܰ�����ͷ����5���Ķ���ȡ������?
H.���������ܿ�������?���ܴ�ȥ�Ѿ������Ĺ�����?������Ǧ�ʻ�ֱ���?
I������ܿ�������(�ų��ǹؽ���ԭ������)?�����Ͻְ��»�����?
J.�������������������(��������)?
˵��������ÿ������ѡ��������(0)��������(1)����Ҫ���˰���(2)��������(3)��
������ѡ��������(0)����Щ�����(1)��ֻ����ij�����ƻ�ܲ����(2)����ؽ���������(3)��
������ָ���ۻ��ٳ�����Ŀ�����õ���ƽ��������ǰ�Ľ���ָ����
(4)���ʪ�ؽ��ײ�����Ƶ�������
��ACR����������������ٴ�����������RA����ĸ��ƿ�����������ʪ��ѧѧ���Ƽ���RA���Ʊ�������������A.���ؽ�����B.ѹʹ�ؽ�����C.�����ڷ�Ӧ��(ESR��CRP)��D.��ʹ��(ʹ��Ŀ�������VAS)��E.VAS�����������ۺ�������F.��������(ͨ��ʹ�ý������������ʾ�)���������������4�����������20%��50%��70%�������˵�˲��˴ﵽACR20��ACR50��ACR70���Ʊ����ɴ˿��Կ�����ACR�������������ܹ���ⲡ��ı仯��
��Van der Heije��������Van der Heije����ͬ�·�����������������ŷ�ޱ��㷺ʹ�á��˷��У����ؽ�����ѹʹ�ؽ�����ESR�Ͳ��˶Բ�����ۺ���������Ϊ����õ��������أ��ڴ˻�����������������(DAS)������DAS���Ի��ߵľ���״̬Ϊ������
(5)���ʪ�ؽ���Ԥ�������������������Ϊ���˽⼲����չ�����ֽΣ�ͬʱ�ж�����Ч���ͽ�һ�������Ʒ�������Ԥ�����Ƕ�ת������Ԥ�⡣���ٴ���������˵���ڽ϶�ʱ����ʹ�þ������ٵ�ʵ�������ݶԼ�����ת�����Ԥ��Ҳ�Ǻ���Ҫ�ġ�һ�������RA����6����о���������1����������ָ��Ԥ���ֵ���ǻ����������(������������ʹ���������ؽڼ�����Ѫ�쵰��ESR)�����ʪ�������ԡ������Խ�ֱ�Ӱ��ѧ��ʵ�������ݸ�����Ч��Ԥ��Զ��ת�顣���˸��ݼ����IJ�ͬ���ж�Ԥ��(��18)��
һЩ�о����֣���HL
ADRB1���Ͼ���1����2��������λ��RA���˶Լװ����ʵ����ķ�Ӧ��������ٴ��۲�Ҳ�������ಡ������������Ľ����Զ�������Ҫ��������������ơ�Ӧ�ô��������������ٽ��Բ�ͬ�������������Ч�����ơ���һ������
Gd-DTPA���е���ǿM
RI�о��з��֣�M
RI����ʾ�Ĺؽ���ʴ�ٶ��뻬Ĥ�ݻ��߶���أ�����M
RI����ʾ�Ĺ���ʴ��������1����������ͨ����ѧ����з��֡���ˣ��о���ԱԤ��RA�еĻ�Ĥ������ͨ��֢���������ʱ��չ���صġ����ֻ�Ĥ�����ڼ������ǺDz����ƻ�������Ϊ�����ھ����ڹؽڲ�λ�Ķ��Լ�����
(6)���ʪ�ؽ�����������ָ�꣺������о����ֺܶ�������Ƕ���ϡ��жϲ����Ԥ���кܴ�İ���(��19)��������Щ���������岢δ��ȫ���������Ҽ�⼼��Ҫ��ϸߣ�����ʵ��Ӧ�����ܵ����ƣ�����ҲԤʾ��δ���ķ�չ����
3.����̴�����ҩ�� �������ǽ�����RA��ҩ���Ϊһ��ҩ��Ͷ���ҩ�һ��ҩ��ָ����̴�����ҩ(non-steroidl anti-inflammatory drugs��NSAIDs)������ҩ��ָ�ı䲡��ҩ(disease-modifying anti-rheumatic drugs��DMARD)��Ҳ��������ҩ(slow acting drugs)��֮�����������ķַ�������Ϊ�������������RAʱ����NSAID���Էdz�Ѹ�ٶ���Ч�ػ���ؽ���֢״����DMARDs�������ú��������Ҹ����úܴʽ�NSAID��Ϊ����RA����ѡ��ҩ���������Ƕ�RA��ʶ�����룬����NSAID�����ܱ����ǹؽڲ�����������DMARDs���Լ����ǹؽ��ƻ��Ľ��̡��Ӵˣ�RA�����Ʒ���Ҳ�����DMARDsΪ����NSAIDs��Ϊ��������֢״�ĸ�������(adjunctive therapy)ҩ�����������Ͻ�����ͳ��һ�ߺͶ���ҩ��ķַ��Ѿ�ʧȥ��ԭ�������塣����ġ�һ�ߡ�ҩ�ﷴ��Ҫ�˾Ӷ��ߣ�������ġ����ߡ�ҩ���Ϊ����RA�ĺ��ġ�
��ʵ������һλ�ж�ؽ�ʹ�Ļ�����˵�������ǰ����Ҫʹ�ü���ؽ���ʹ��ҩ������������ǰ������3��ҩ�ֹʹҩ��
NASIDs����Ƥ�ʼ��ء�ֹʹҩָ�����������ӣ����������ڽ�����ʹ���������������á������RA֮��������DMARDsΪ���������ڿ��Ʋ������ͣ������3��ҩ�
(1)��NSAIDs�������õ���ʶ���̣�����̴�����ҩ����һ����ҩ�����ҩ����н�����ʹ�������á�һ�������������Ч�Ͽ죬С������Ҫ�ǽ�����ʹ���ϴ�������п������á������ܹ�������֢��֢״�����������Dz���������������֢��ԭ����NSAID�Ը�����ʽ�Ĺؽ����п������ã������ǶԻ��������Ľ�չû�����ã�Ҳ�Ͳ��ܶ�����Ĺؽں�����֯�𱣻����á��ٴ��۲������������ʹ��NSAID���г������Ʋ�������ֹ�ǹؽڵ��ƻ����̡�
���Ƕ�
NASIDs����ʶ��Ϊ3���Σ�
��һ����1971�꣬Vane���NSAID����Ҫ���Ժ�����Ч�����ܹ����ڴ���ҩ�����ƻ���ø(cyclo oxygenase��COX)����ǰ�����ص�������
�ڶ�����1990�꣬Masferrer��ָ�����ܴ��ڷֱ��ɲ�ͬ�������Ļ���ø�ء����ܿ���롢��¡�õ�COX-1��COX-2����ͬ��ø�Ļ���D
NA(cD
NA)�������������о�����COX-l�ǽṹ�Ի���ø����Ҫ�鵼����������ǰ�����أ�����ϸ�����������ܣ���COX-2���յ��Ի���ø�����ڶ��ء���֢���Ӽ���֯���Ĵ̼������������յ�����һ�������������NSAID�ڿ���Ч����θ����������֮�����ϵ�����dz�����COX-2���Ƽ���������20���͵����ʮ�꣬COX-2���Ƽ���RA������������С�ĺ䶯ЧӦ��
һֱ������COX-1����Ϊ��һ�������ġ��ܼ�ø(housekeeping enzyme)���������ںܶ���֯�У�����θ�Ĥ����Ƥ��ѪС���������������ǰ�����صIJ�������Щǰ�����ؾ��б���ϸ����ά����̬�����á�NSAID�ܶ�ĸ�������COX-1�ܵ�������ء�
��һ������·Ǽ���ϸ��������COX-2������״̬��COX-2������ijЩϸ���У�������֯�����衢���ࡢ���١������θ�������ּ��͵�ˮƽ������������Щ������ȷ�еĹ��ܻ���ʮ���������ϸ����Ѫ��ƽ����ϸ�����ؽڻ�Ĥϸ���ʹ�����Ԫ��ֻ���ڷ����ء�ϸ�����Ӻ��ڶ��صȴ̼��յ��£�������COX-2������ǰ����ǰ�����صĺϳɣ�����COX-2�����յ�ø����֢��Ӧʱ�����ڲ���������COX-2ԶԶ����������ˮƽ��Ŀǰ����ģ��֤ʵ��COX-2�����(��)���յ�����֢��������ʹ�ͷ����йء��ڶ��������֯�У�COX-2����Դ����ʹ�ͷ�������ϵ������Ľ᳦��ģ�������Ĥ�����������˾���ϵ������������������йء�COX-2Ҳ����һЩ�������������̣����磬��ֳ���������Ѻ���̥ϸ�����Ŵ����ǵ��ؽ���COX-2������С����״ͻϸ������Ѫ����Ƥϸ���ڱ�������ƺ���Բ�����ʱ��ˮ��������Ѫ�ܽ�����ת��ø���Ƽ�(angiotensin-converting enzyme inhibitor��ACEI)��ʹ������ϵ�����������COX-2Ҳ�ɲ�����Ӧ�IJ�����Ӧ��
��������20����ĩ���о���Ա����˶�COX��������ʶ�������о����֣���RA���ߵĻ�Ĥ��֯�в��COX-1��COX-2�����������������ʪ��Ĥϸ����ʾ����ϸ��������άϸ������Ƥϸ��������������ϸ�����������ø���ó�COX-1��С���ܼ���Ի�����ϩ�����֢��Ӧ�����ó�COX-2��С�����Դ̼�ͬ���ɳ�����֢��Ӧ�����䷴Ӧ�̶�������������Բ��졣˵��COX-1�����ǹܼ�ø��Ҳ���յ�ø����������֢�����м�����֢�����ã���COX-2��������֢�йأ�������������δ�ز�������֢��Ӧ��
COX-1����Ϊ�ܼ�ø����ά���������̣�Ҳ��Ϊ�յ�ø������֢��Ӧ����֮��COX-2��Ϊ�յ�ø������֢��Ҳ��Ϊ�ܼ�ø����Ҫ�������ԣ���ˣ�������Ϊ2��ͬ��ø�й����ϵ��ص��������ϵĻ�������ͬ�Ի��巢�ӱ�������(ͼ42)��
NSAIDs��ҩ�����û����������ơ����ʵ��������£�NSAIDs�ܹ�����������ữ���ã��ܹ���
Ѫ�������û�����Դ�Կ����ģ�������ø��ø���ͷţ����Ʋ��弤������ĵ����ɺͻ��ԡ��������ϸ���Ƶ������£�NSAIDs�����������ø������ǿPGE1�鵼���ڻ�
���������ӵ��������Ӷ�����ǰ����ϸ���Ĺ��ܣ���������Ѫ�ܰ�ϸ���Է����ش̼��ķ�Ӧ������������ϸ���͵�����ϸ���ľۼ�������������ϸ���Ĺ��ܡ�NSAIDs���������ÿ��Գ����ڲ�����COX��ϸ�������Ҳ���ǰ�����ص�Ӱ�졣NSAIDsͨ����������ļ����źţ��Ӷ���������ϸ���ļ��NSAIDs���ܻ�������ɻ������ƶ��κ�ϸ����������������Ƶ���ϸ��
��֬øC�Ļ��ԣ��Լ�����NO�ϳɡ�
(2)NSAIDs�ķ��༰�����ص㣺
��NSAIDs�ķ��ࣺһֱ����NSAIDs�ķ����Ǹ��ݻ�ѧ��ɺ�
Ѫ����˥�ڽ��еģ�������鰴�����Ƕ�COX-1/COX-2���ƵĻ��Խ��з��ࡣ����COX-2�о��齨�齫NSAIDs��Ϊ����4�����ͣ�COX-1�����ԡ�COX�������ԡ�COX-2���Ⱥ�COX-2�����ԡ�COX-1���������Ƽ�ָҩ����Ҫ����COX-1���ٴ��ϲ������ɼ���COX-2�����������á�С�����İ�˾ƥ����Ωһ���ڴ����ҩ�COX�����������Ƽ�ָҩ���COX-1��COX-2�������������ٴ���û��������𡣴ֵ�NSAIDs�����ڴ��ࡣCOX-2���������Ƽ�ָҩ����������Ƽ���ʱҲ��������COX-1���������á�һ������£������Ƽ�����������COX-2������Ҫ��COX-1ǿ100�����ϡ�Ŀǰ�����Ƽ���
��������(celecoxib)��
������(rofecoxib)��COX-2����ָ���ٴ�������COX-2�����Ŀ�����ʹ����ʱ������������COX-1��һ���Ƽ��������ڴ����ʱ���Բ�����COX-1���������á������������COX-2��COX-1�����IJ����ڷ�������COX���Ƽ���COX-2���������Ƽ�֮�䣬��Ҫ����������(meloxicam)����������(nimesulide)��
���ж���(etodolac)��������ҩ������������COX-1��COX-2���������2��100�������ڲ�ͬ�Ļ����ٴ���Ӧ��ͬ����ʱҩ���Ч������Ԥ�ϡ������еĻ��߹涨һ��ͳһ�ļ���Ҳ�Ƚ����ѣ���Ϊ����ijһ���������ܲ�����ѵĿ�����ʹЧ����
��NSAIDs�������ص㣺������RA��NSAIDs����������֢�����á�ҩ�����պ���Ժܿ������ؽں졢�ס��ȡ�ʹ�������ƹؽڹ��ܡ�һ��NSAIDs��ʵ���Ҽ�������ʪ���ӡ�Ѫ����CRP��
Ѫ�������Ȳ�����Ӱ�졣������NSAIDs��RA������DMARD�����ڼ���ֵĹؽ�ʹ���ס�ѹʹ�ͳ���Ҳ���洦��������NSAIDs��ҩ��֢״�ֿ��Ժܿ츴������ͬNSAIDs�����������������ͬ������֯����Чҩ��Ũ���б�¶��ʱ���йء���ˣ�����Խ��
Ѫ����˥��Խ�����ٴ������ڴﵽ���Ч�������ǣ���ѡ����COX-2���Ƽ����ԣ����ż��������ӣ���Ч�����ﵽһ��ƽ̨�������������俹��Ч��Ҳ�����������ӡ���ʵ�ϣ����е�NSAIDs����С�ڿ�����ʹ��ʱ�����ܻ�����ʹ��NSAIDs����ʹ����һ�㱻��Ϊ�������Եģ�������о�������ѡ����COX-2���Ƽ�Ҳ������ֹ������ϵͳ�ͼ�������ʹ�Ĵ����Լ���ʹ�Դ̼��ĸ�֪������NSAIDs��ʹ��������һ���IJ��
��ŵ������һ�ֱȽ��µ�NSAIDs������ʹЧ������Ϊǿ��ͬ��ҩ������ٴ�����֤������NSAIDs�ﵽ�����Ч������Ч�����ƣ����Dz�ͬ�IJ��˶Բ�ͬ��ҩ�ﷴӦ������ͬ���������ҩ��Ĵ�л�����˶�ҩ��������ԺͲ��˵ĸ�������йء�NSAIDs��ͬҩ��ļ����Ͱ�˥�ڱȽϼ���20��
һ������£�����ٴ�Ч��������NSAIDs��ҩ��7��10���ڣ������������Ȼ���ܲ��������Ч������Ҫ���ǻ�������NSAIDs������Ƥ�ʼ��ء�
(3)NSAIDs�ĸ����ã�
�ٴ�ͳNSAIDs�ĸ����ã�
A.θ����֢״������ҩ�ﱾ����θ������ֱ�ӵĴ̼����ã�����Ӱ��ǰ�����صĺϳɣ��Ĥ���������ܵ��ƻ��������׳���θ�����Ĥ���á�����������Ѫ��֢״�ж��ġ�Ż�¡��ڱ����������Ѫ��Ϊ�˼�����ֹNSAIDs��θ�����ĸ����ã��������˲ͺ��ҩ���Լ��ٶ�θ�Ĥ�Ĵ̼���NSAIDs����θ��������֢��Σ�������У�a.�����ˣ�b.��θ����ʷ(��������ݸ˾���Ⱦ)��c.���ڷ�����Ƥ�ʼ��ػ���ҩ��d.��ѪС����ٻ�ѪС�幦���ϰ���e.����Ů�ԣ�f.���жȻ��ض�����˥�ߡ���Ӳ���������ܲ�ȫ��g.�а�˾ƥ�ֹ����������ͱ�Ϣ�ⲡʷ��
θ�����¼�(��Ϊ����θ���������ö���ҪסԺ���ƻ�����)���ֱ�(��21)�������ж��Ƿ�ʹ������ҩ����������Σ���ʳ���1.5����Ҫ����θ����������COX-2���Ƽ��봫ͳ��NSAIDs�Ƚϣ��ܹ����Խ���θ���������õ�Σ���ԡ�
B.�����ԣ����꼰�����ܼ����Ǵ���ҩ���������ั���õ�Σ�����ء�NSAIDs�����������ھ�����Ѫ�����õ�ǰ�����أ�ʹ����Ѫ�����ٶ�����NSAIDs�Դ�������˵�������Ӱ�춼�����ֲ�����ʹ�ô���ҩ�����Ѫ�弡�������ߡ�NSAIDs���������һ������һ���ط��Է�Ӧ�������������������ͼ��Լ��������ס�
C.�������ã�NSAIDs����ѪС���COX-1���Ӷ�����Ѫ˨��A2�ĺϳɣ�Ӱ��ѪС��ľۼ���
D.�ζ��ԣ�NSAIDs����ʹת��ø���ߣ��������ᡣ
E.������Ƥ�����Ҳ���Է�����NSAIDs���ԶԹ���������ƣ��Ӷ�������ϸ��ȱ���������ϰ���ƶѪ�����ָ����ÿ����������ģ����������
��̩�������ײ��������ĸ����ã�ʹ��ʱ����Ҫע�⡣
��ѡ����COX-2���Ƽ��ĸ����ã�
A.θ����֢״��ѡ����COX-2���Ƽ�Ҳ��θ����֢״�������Ǿ����������������������й�ѡ����COX-2���Ƽ��ij����о����ݱ�����ѡ����COX-2���Ƽ�����Ч���봫ͳ��NSAIDs���ƣ������нϺõ�θ������ȫ�ԣ����Խ�θ��������֢��Σ���ʽ���һ�롣һЩǰհ��˫ä�����ٴ�������ʾ���ھ�֤ʵ��θ�Ĥ��ʴ������ķ�������ѡ����COX-2��Ͱ�ο�������ƣ�����Ҫ�������������Ͳ�����顣���ǣ�����ο�����⣬�����������ڶ��ġ�����������ʹ��Щ֢״�ķ�������û�����������ˣ�ѡ����COX-2������������NSAIDs���������غ������Ը����ã����������Ը������ǵ�θ���������ԡ�
B.�����ԣ����µ��о����ϱ�����COX-2�Ե���������Ҳ����Ҫ�����ã�ѡ����COX-2���Ƽ��������ܵ�Ӱ���봫ͳҩ���ơ��о����֣�
����������������������С���˹��ʽ��ͷ�������ơ��ڶ�����о��У��밲ο����Ƚϣ���
������12.5mg/d����6
���ʹ��С���˹��ʽ���0.14ml/s��25mg/d��0.13ml/s����������50mg3��/d��ÿ��ʹ��С���˹����½�0.1ml/s����ˣ�ʹ�ô�ͳNSAIDsʱ���õ������ܱ�����ʩ�ڷ���ѡ����COX-2���Ƽ�ʱҲ��Ҫ���Dz��á�
C.�������ã�ѡ����COX-2���Ƽ����ܶ�ѪС���𤸽�;ۼ�����Ӱ�죬��������Ҫ����������²��ܴ��氢˾ƥ�֡������б������봫ͳ��NSAIDs��ȣ�ʹ��ѡ����COX-2���Ƽ����и��ߵ�Ѫ˨�¼�(�����ļ�������������)�����ʡ�
D.��������Ѫ�����������ٻ����ˮ��ʱ�����Ѫ������˥�ߡ������ۺ������Ӳ������Ѫ����ˮƽ��2.5mg/dl��Ҫ����ʹ��NSAIDs��ѡ����COX-2���Ƽ��������ϱ�����COX-2���Ƽ��ܹ�������֫ˮ��Ѫѹ����ͬ������˵�ģ������о�����COX-2����������������(������γɡ����ѵ�)�С��ڻ����Ӧ����ijЩ��Ӧ��һЩ���������о��и���Χ�����á����磬����ֳ�������Ĺ��ܡ�����IJ�������״̬���κ�Ĭ��(Alzheimers disease)�ͽ᳦ֱ�������У�COX-2����һ�������á���ˣ���������COX-2���������������Ӱ�컹��Ҫ��һ�����о���
4.�������͵�NSAIDs�Ƽ���
(1)
��ŵ����Lornoxicam(��Ʒ����������
Xafon)��
��ŵ���������
��ŵ�����������������̴�����ҩ��һ�֡��ڷ�����Ѹ�٣��ʼ������Թ�ϵ�����պ���ȫ�����ʱ��ƽ��1��2h��ƽ����˥��Ϊ3.5��4.5h���������ڵ�
��ŵ����Լ99%�뵰��ϣ�ѪҩŨ�Ⱦ�����ͣҩ��Ѹ���½������ؽ�Һ��Ũ��ȴ�ɱ�����Ժ㶨��
��ŵ�����ڸ����б���л����ȫ���Ե�5-�ǻ�
��ŵ������Լ1/3�����Լ2/3�ӵ�֭���Դ�л�����ʽ����ȫ��й��ͬ�ȼ�����˨���뾲��ע�����ȣ�ǰ���������ö�ֻ�к��ߵ�65%��74%������ֱ����ҩʱ����Ӧ�����ӡ�ʳ�����ʹ
��ŵ���������ռ���20%�����
��ŵ����Ӧ�ո����á��ظ���ҩ�����������ڲ��������������Ϊ��ҩ��˥�ں̡ܶ�
��ŵ��������������Ҳ�������������������˥�ߵIJ�������ҩ������ѧ�ص�������䡣
��ŵ������12��16mg/d�����¿����ڸι��������˲�������������8mg/d����ʱҩ������ѧ��������������������죬��˳��Ǹι��������أ�������Ҫ����ҩ�������
��ŵ��������������̴�����ҩһ��������ʹ�Ϳ���������ͨ�����ƻ���ø(COX)���ԣ��Ӷ�����ǰ�����غϳ���ʵ�ֵġ�
��ŵ��������COX-1��COX-2����ͬ��ǿ�ȵ��������á���Ϊ��������5-������ø���ԣ����Բ����ư���ϩ�ĺϳɣ�Ҳ���ı仨����ϩ����5-������ø��ת��;����
NSAIDsҩ�������ʪ�ؽ����е�Ӧ����Ҫ��Ϊ�˻��⼱������֢����ʹ�����Dz����ܸı�RA�IJ��̡�
��ŵ������Ȼ����DZ�ڵļ��ٹؽ��ƻ������ã������������û�û�����ٴ��еõ�֤ʵ����ҩ���ŵ��������Ŀ�����ʹ���ý�ǿ���ڷ���ҩ1h����ע25min�ɲ������ã������ÿ�ά��8h���ϡ�
��ŵ��������ʹ��������������Ŀ������������֢������ʹ��������ʹ�������Ź㷺��Ӧ�á��Ѿ��кܶ��ٴ�ʵ���
��ŵ������RA�е���Ч�����˹۲죬��Щ�۲�ȷ����
��ŵ��������Ч��ϵ����4mg 3��/d��8mg 2��/d��2��4mg 2��/d��Ч�����ƹ����м����Ļ��û���������ơ�
����Ϊֹ���ڲμ�
��ŵ�����ٴ������4349�������У����ܵIJ�����Ӧ������Ϊ24.9%��θ����֢״��Ϊ������֢״�����Ϊ������������ʹ�����ġ�Ż�º�к������������ķ�������0.5%��θ����������Ӧ�ķ����������ء���������ʱ�������˺�Ů�Բ��˳���θ����������Ӧ��Σ�ղ������ӡ���Ϊ
��ŵ����һ����ѪҩŨ���½��ܿ죬���ڹؽ���Ũ��ά�ֽϳ�����һ������
Ѫ��������˥�ڶ̣������ñ���θ�Ĥ�ͱ�����Ѫ������ǰ������ˮƽ�����θ�ҩ֮��ﵽ����������θ��������������̴�����ҩҪС�����⣬�������ࡢ���ࡢ��ϵͳ��Ƥ����Ӧ�Ȳ�����Ӧ�ı��������������ʼ��͡��ڽ������Ƽ���3��������1�����ϵIJ����У�������Ӧ������Ҳ���ơ������������Ӧ���ڿ�ʼ��ҩ���1�����ڳ��֡���֮��
��ŵ������4��16mg������Χ�ڳ���ʹ���DZȽϰ�ȫ�ġ�
��ŵ����������ҩ��֮������������������̴�����ҩ���ƣ����뿹��ҩ������ѪС��ۼ�ҩ���ÿ������ӳ�ѪΣ�գ�����ǿ������Ľ���Ч�����۽���������������úͽ�ѹЧ��������ǿ﮼����ԣ��ݼװ����ʿ�������
��ŵ����ѪҩŨ�ȣ��������涡�����
��ŵ����Ѫ��Ũ�ȣ��ߵظ����������������
��ŵ�����������
��ŵ��������������в�Ӧʹ�ã�����֪�Է���̴�����ҩ�й�����Ӧ�����м���θ������Ѫ����θʮ��ָ������ʷ���۾��в���ԭ�����Ѫϵͳ������������Ů�ԣ�����ҽ��ָ���IJ����ڸ�Ů������ҽ��ָ����Ӥ������ͯ��18�����µ������ꡣ
�����������ʹ��
��ŵ����Ӧ�����ؿ��ǣ�����������Ѫ�����������������ƶѪ���ھ��в���Ѫ˨�Ŀ��ܣ�������������(Ѫ������140��mol/L)��Ŀǰ����Ӱ�������ܵ����������ߣ�������С�����������������ܶ�
ˮ����������������ʹҩ�����ܡ�
��֮��
��ŵ������һ��ǿ��������ʹ����ҩ������RAҲ��ʹ���俹����ʹ��ҩ�����ã���������ʹ���棬������������������������̴�����ҩ���еȼ����İ�Ƭ��ҩ�����������������á���˿�����Ϊ����RA֢״�ĽϺ�ҩ�
(2)��������(meloxicam)������������������COX-2����ҩ�ﵽ�ﻬĤҺ��Ũ����
Ѫ��Ũ�ȵ�4%��50%������������ʽ�ڻ�ĤҺ��
Ѫ����Ũ�����ơ�����������Ҫͨ��ϸ��ɫ��P450-2C9��л��ҩ������������7��8ml/min�������˥����15��20h���ι����������ȵ��жȵ���������Ӱ������������ҩ���л�����������Եظ��������ס�С�����װ����ʺͻ����ֵ�ҩ���лӰ���С����
���ڵ����˫ä�ٴ����鷢����������7.5mg/d��15mg/d����˫�ȷ���100mg/d��������750mg/d��ƥ������20mg/d��Ч����Χ���ʰ�ȫ������(MELISSA)�о����֣���������7.5mg/d��˫�ȷ���100mg/d�����������������ԡ�������������ʹ�����ġ�Ż�º�кҪ�ٵö࣬���ܶ��߸��ƹؽ�ʹ�ij̶���ͬ��������������RA���Ƽ�������15mg/d��
(3)
��������(celecoxib����Ʒ��
Celebrex)��
��������������ҩ���
Ѫ������ʴ�Լ500ml/min�������ڵĵ��������97%���ң�ƽ���ֲ���
Ѫ���ͺ�ϸ����ҩ���
Ѫ�������˥����10��12h���㹻���Ƽ�������5���ɴﵽ�ȶ�Ũ�ȡ�
�������������վ����������࣬���ϸ�ҩ������Ҫ�����糿��ҩ�����ں�����ʵ�鷢�֣�ҩ����Ҫ��ϸ��ɫ��P450-2C9��л�������Ե���ʽ�ų���
��������������ҩ����ٲ����ٴ������Ե�����á�
�ڲ�ͬ�����������£�
������������ʾ�˶�COX-2�ĸ�ѡ���ԡ���һ��RA�ٴ������У���
���������ֱ�Ϊ200mg��400mg 2��/d����֢״�ĸ������������ڰ�ο���飬�����ּ�����
��������������֮��Ч��û�����Բ��졣������Ͱ�ο�����û�����صĸ���Ӧ��������
������������������˫�ȷ���ıȽ��У��ھ�֤ʵ
��������������������ķ��������Ե�����������˫�ȷ����顣
������������RA���Ƽ������dz���100mg2��/d��200mg 2��/d������֪��
�����������������
�ǰ�������������ݡ���������Ӧ�����˾ƥ�ֻ�����NSAIDs�й����Է�Ӧ���ˣ�������ʹ�ø�ҩ��
(4)
������(rofecoxib����Ʒ��vioxx)��
��������һ������4-�����������������������COX-2��������COX-1��1000�����ϡ���ҩ�ڷ���θ�������պܺã������������ö���93%���ң�ҩ���Լ85%��
Ѫ������ϡ�ҩ����Ҫ����ԭ��˫��
����������ͨ��ϸ��ɫ��P450;����25mg�ڷ����
Ѫ���������120ml/min����25mg/d����4���ɴﵽ�ȶ�Ũ�ȡ�
�ڶԹǹؽ����о��з��֣�
������12.5mg/d��25mg/d������Ч����˫�ȷ���150mg/d���ƣ�����˫�ȷ���������Ϊҩ��ĸ����ö�ͣҩ�ı���Ҫ���Զ���
�������顣��
��������������������
������250mg/d�������2400mg/d����˾ƥ��2600mg/d�Ͱ�ο���ֱ�����7�죬���
����������������밲ο�������ƣ����Ե��ڲ���ҺͰ�˾ƥ���顣
�������Ѿ���FDA�����ڹǹؽ������ƣ��Ƽ�����Ϊ12.5mg/d�ٷ������ص�����¿��Լӵ�25mg/d��Ӧע��
������������������ѹ�����ߣ������ٴ���Ѫѹ����Щ��˾ƥ�ֻ�������ͳ��NSAID�����Ļ��߲��ʺ�ʹ��
��������
(5)�����е�����COX-2���Ƽ���parecoxib��һ��ע���õ�COX-2���Ƽ����ܻ����������˵ļ�����ʹ�����ٲ��˶���ȵ�����ҩ��ע��ע���ɣ����Ҹ����ý�С���ڶε�3ĥ��(�ֳ��dz�)�IJ��˵��о����֣�20mg��40mg parecoxib��ֹʹЧ����60mgͪ����(ͪ����)�൱����parecoxib������ʹ��ʱ�����Ա�ͪ���᳤���俪����˾Pharmacia�Ѿ�������NDA������롣
Pharmacia��˾��������һ�ֿڷ�COX-2���Ƽ�valdecoxibĿǰ�Ѿ�������ڿ����Σ�������ֹʹ�����ʪ�ؽ��������ɵ����ơ�����Ĭ�˹�˾Ҳ���ڿ���etoricoxib(MK-663)��
5.�ı䲡��ҩ �ı䲡��ҩ(disease-modifying anti-rheumatic drugs��DMARDs)��������Ϊ����RA�Ķ�����ҩ������RA����Ӧ�þ������DMARD�����Ѿ���ΪĿǰ��ʪ��ѧ��Ĺ�ʶ������ҩ������װ����ʡ������ǰ���ड���űҩ���������ʡ�����������������A��
ù�����������٣����꿪ʼʹ�õ���������Ҳ�������ڴ���ҩ��֮�С�
(1)�װ����ʣ�
�ٶԼװ������������ʪ�ؽ�����ʶ���̣��װ�����(MTX)��20����40������ȱ�Seeger�ϳɣ������������������������ҩ�ڷ�ʪ���е�Ӧ������Ҳ����50�ꡣ���ܼװ�������������RA�Ļ�����δ��ȫ���ˣ�����Ŀǰ�ձ���Ϊ��������Ч��DMARDs��ҩ�����RA�����еļ�ֵҲԽ��Խ�ܵ����ӣ������ڰ����ٴ���������ǰ�����ⲻ��Ҫ��Ҫʹ�üװ����ʣ�����Ϊʲô���üװ����ʡ�
1972�꣬Hoffmeister��һ��������С�����װ���������RA��Ч������78�����˳���15����������У�45������(58%)ȡ��������Ч������28�����˻�á���ȫ���⡱���Դˣ��װ���������RA���ٴ��۲�Ѹ�ٿ�չ��1984��1985�꣬½��������4�������о��Ľ��(��22)�������ʾ��A.25%�����飬���˵Ĺؽ��ס�ʹ���Ը��ƣ�B.�����飬���˵ij�������ƽ��ֵΪ46%��C.�����飬���˵�ESRƽ���½�15%��
�ܶ�ѧ�߽��װ����ʺ���������ҩ���RA����Ч���бȽϣ�û�з�������һ��ҩ�����ڼװ����ʡ������ڶ�֢״�ĸ��ƻ�����Ӧ�ķ����ʷ��棬�װ����ʶ������������ʡ���ע�Ľ��Ƽ��ͼװ���������ͬ����Ч�������Ƽ��Ķ���Ҫ���ڼװ����ʡ�
��ŵ���ͻ�����A����ЧҲ�����װ����ʡ��װ����ʺ��������ص���Ч��ͬ�������۸�Ϲ�Ŀǰ�ձ���Ϊ�װ�������DMARDs�е���ʹ������Ч��ҩ�
һ���26��RA���߳���130���µĹ۲���ʾ��ʹ�üװ����ʺ�����������ĸ��ƣ�6���º���Ч�ﵽ���12���º�130����ʱ����Чû�������IJ������10��������130�����Ƴ̽���ʱ�����ٴ���Ч��Ȼ����ά�֡�50%�Ļ��߿���ͣ��Ƥ�ʴ���33%�Ļ��߿��Բ�����NSAID��ҩ����ҷ��ּװ����ʱ���������ҩ���������Ҫ�õöࡣ����Scully��124��RA�����üװ���������5���Ļع��Է���������31%�IJ����ܳ������ܼװ��������ƶ������ٴ����档����������ж����Ƶ�ԭ������Ϊҩ��ĸ����ã���������Ϊ��ȱ����Ч����Ȼ�ֲ��˻���ֲ�����Ӧ���������ᣬ����ֻ������������ɻ��⡣
�ڼװ����ʵļ������÷������ڲ�ͬ�IJ��ˣ���ѵļװ����ʼ����Dz�ͬ�ģ�����ͬһ�����ڲ�ͬ�Σ�����ļװ����ʼ���Ҳ��������������ҩ��������Ч����������С�����ڶ�����ʪ��ѧ�߾����żװ����ʵ�����ÿ�ܸ�ҩ1�Σ���ʼ����Ϊ7.5mg/�ܣ����������Ӧ�ϴ������Լ��١���������Բ�����Ӧ����������������2.5��5.0mg/�ܣ�ֱ������õ����ƣ���������Ӧ����������Ϊֹ��һ��4��12����Ч������Ŀǰ����RA��ѵļװ����ʼ���������ȷ���ٴ�����Ӧ��7.5��20.0mg/�ܣ������������Ҫ10.0��20.0mg/�ܣ����ֲ�����25.0mg/�ܣ�����������������нϺõ���Ч�������(30��50mg/��)��ʹ��Ҳ�����Թ������ٴ��������٣��д���һ���о����ٴ�֢״��������װ����ʿ�������������Ҳ�н�ÿ����ҩ��Ϊÿ������ҩά����Ч�ı������װ����ʵ���Ч�ʼ�������ԣ��䶾��Ҳͬ����ˣ������ϴ����Ӧ����ȡ�ýϺõ���Ч�������������������ܡ�
�װ����ʸ�ҩ;���пڷ���Ƥ��ע�䡢����ע��;�����ҩ��������һ�ָ�ҩ;������Ӧ��ÿ�ܵ����������Ա��ⶾ�ԡ��ڷ���ҩ�ȽϷ��㣬�����ղ���ע��;���ȶ���������߶����ӿڷ���������Ч��Ӧ�Բ����룬���Ը�ΪƤ�»���ע�䣬����ʱӦע��ҩ��Ķ��Է�Ӧ����Ϊ��Ϊע��;�����ܻ�����ҩ�����մӶ����߲�����Ӧ�ķ����ʡ��ؽ�ǻ��ע��װ����ʲ�δ��ʾ�ܺõ�Ч����
�۲���
Ҷ��������ͷ���������
Ҷ�����Լ����Ԥ���װ����ʵ��Ĥ��θ������Ӧ��ȫѪϸ�����ٵȲ�����Ӧ��
Ҷ���ķ���ÿ���ÿ�ܸ�ҩ���ڷ�1mg/d�����Լ���װ����ʵĶ��Զ���Ӱ������Ч����������5.0��27.5mg/�ܴ������
Ҷ�������ֲ�����С������ʾ�������Խ�ԡ���
Ҷ��Ҳ�����������ټװ����ʵĶ��ԡ��ڼװ����ʴ�л��˥���ڸ�����
Ҷ�������ͼװ����ʵ���Ч������
Ҷ�����Ƽ�Ӧ�ڼװ����ʸ�ҩ24h����á�����ĿǰΪֹ�����в���
Ҷ���ĸ������ڷ�ֹ��װ����ʵĶ��Զ�����100%��Ч����֪RA���߿���ȱ������ά���غͿ����ʣ����ߵ�ƶѪ�����Ƕ�����������ģ�����Ӧ�ø�֪������ע����ʳƽ����Ƽ�ÿ�첹�临��ά���ؼ�400��g
Ҷ��������Բ�����
Ҷ���ļ����Ͳ��Խ��еĶ����Ĵ����ٴ��о��ṩ�˿ɹ��ο����ٴ����顣���ǵĽ����ǣ�
a.����װ����ʼ�����5.0��12.5mg/�ܣ����ڼװ����ʸ�ҩ��1����赥������
Ҷ��2.5mg/�ܡ�
b.����װ����ʼ�����15��30mg/�ܣ����ڼװ����ʸ�ҩ��1����赥������
Ҷ��5.0mg/�ܡ�
B.�Լװ����ʶ��Է�Ӧ�Ĵ�����
a.��ȷ�Ӧʱ�����װ����ʼ���2.5mg/�ܣ�ʹ�������Ƽ�����
Ҷ������ֱ����Ӧ�����һ�������ý��������ԭ�������ƣ�
b.�жȷ�Ӧʱ��ֹͣ�װ�����ʹ�ã�ֱ����Ӧ���⡣��Ӧ������Ե���ԭ�װ����ʼ���5.0mg/�����¿�ʼ���ƣ������ǰû�в�����
Ҷ����֮������ѷ�����
Ҷ������ɽ����������2.5mg(�װ����ʣ�15mg��ʹ��5.0mg��
Ҷ�����װ����ʣ�15mg��ʹ��5.0mg��
Ҷ�������б�Ҫ�ɼ���7.5mg��10mg)�����2��3�ܺ�����û�и�������ɰ�ԭ�������ƣ�
c.�ضȷ�Ӧʱ��������Է�Ӧ���أ���������в��������סԺ���ƣ���ͣ�üװ����ʶ�����
Ҷ���ⶾ��һ�����Խ����������������״��������װ�����ʹ���DZ�Ҫ�ģ����������жȶ��ԵĴ����취���У����ҶԲ��˽������еļ�⡣
�ܼװ�����������DMARDsҩ����������ƣ�RA���Ƶ�����Ŀ������ֹ���ʵ��ƻ����̣������Ѿ��ƻ��Ĺ��ʡ��װ����ʿ��Լ������ƻ��Ľ�չ�������ڻ�����ʵ��ƻ�������һ�������ҩ���˺ܶ�ѧ������DMARDsҩ������ʹ�á����ڼװ������ǵ���ʹ������Ч��ҩ����Ӧ��Ϊ������ҩ�ĺ��ġ��װ�����-������A�������ƵĽ������ʾ��������ҩ����ʹ�ã���Ч��Ҫ�ã����ܺ��ú�Ѫ����ˮƽ�������������������Ժܺá�������A��ʼ������2.5mg/(kg��d)�������ٴ���Ӧ����ÿ4������0.5mg/kg�����ռ����ȵ���ҪС������ʹ�ù�����Ӧע�������ܵļ�⣬���������������30%��Ӧ���ٻ����صļ������װ�����-��������ण��װ�����-�������ʣ��װ�����-
�����-���������Ҳ����ʾ��Ч���ڵ�����ҩ���Լװ����ʷ�Ӧ������IJ��������Ч���½���չ�������Ƽ�Ҳ�������ͼװ���������ʹ�ã���
��������(������������-�����������Ƽ�)���ϼװ����ʣ���Infilximab(��������������-������¡����)���ϼװ����ʡ��о��������ڵ���Ч�������⡣��������(leflunomide)��һ���������ߵ��ڼ���ͨ��������वĺϳɶ������������ã������о�������װ����ʺ��ú���Ч��ǿ�������ò����ӡ������������ҩӦ����������Чͬʱ���ٸ����ã�����ȱ�����ڴ��ڲ����Ĺ۲��о����������Ϸ�������Ч�ԺͰ�ȫ�Ի���Ҫ��һ������������������ҩ��ͼװ���������ʹ��ʱ���ܳ��ֵķ�Ӧ(��23)��
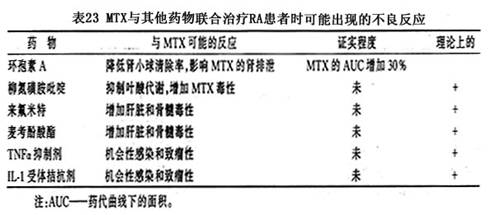
�ݼװ����ʵĸ����ã��װ����ʵĸ����ý϶࣬����θ����֢״���κͷ���ѪҺѧ�쳣������ֳ��Ӱ�졢�ѷ���Ƥ����Ӧ��������ϵͳ���Լ��Թ��ʵ�Ӱ��ȡ�Day���˷����װ�������ز�����Ӧ�IJ�������ҩ��ĸ���Ӧ����Ϊ4�ࣺA��Ϊ����������(��θ��������)��B��Ϊ�����Է�Ӧ(��װ����ʷ���)��C��Ϊ������������ԣ����Ը���ҩ���ܼ���Ԥ��(��ζ���)��DΪ�ӳ�ЧӦ������ͣҩ��Ҳ�ᷢ��(��װ������ڻ���ǰ3��������ĸ���Ӧ�������»�)��
A.θ������Ӧ��θ������Ӧ�Ǽװ��������ƹ���������ĸ����ã�Ҳ���������¼װ����ʼ�������ͣҩ��ԭ����ʳ�������ġ�Ż�¡���к����ʹ���������������ؼ���ȡ������������Щ֢״���Ƚ��������ڸ�ҩ���ʱ���ڳ��֣����װ����ʼ������١�ʹ������;����ҩ��
Ҷ�������Լ���֢״���������żװ�����ʹ��ʱ����ӳ������˿��������ܡ�
B.�ζ��ԣ��ڴ����������ऺͼװ������������ư�Ѫ���ã�������ά����Ӳ���ķ����ͼ����ڱ�����20����60�������ʹ��С�����װ����ʳ�ʱ��������м��ʱҲ���ֿ����շ���Ӳ��������֯ѧ�����ʾ�����ܼװ��������Ƶ�RA���˵ĸ���ᷢ��������IJ����ı䣬������������֬�����ԡ��˱��졢����������������֢�������Ը�ϸ����������������ά����Ӳ������ͬʱҲ����RA����м�������ڼװ���������ǰ�Ϳ��Գ������Ƶı仯��������ơ����֡�˥�ϡ�����һЩδ֪������Ҳ����ɸ����������������ӵ����أ����������е��쳣�ı䶼����ڼװ�������ȻҲ�Dz������ġ��װ��������������ԭ���������һЩѧ����Ϊ�װ����ʿ��Լ�����֬ϸ��������
��ԭ��������ƾ���ͬ����ʱ��Ϊ��������Щѧ�߱���������ʹ�üװ����ʺ����������������֯�мװ����ʺͼװ�����-glu2-7���ۻ��������Ʋ��
Ҷ����л�������������ϸ����ԭ��
��Ȼ�װ������н϶�IJ�����Ӧ�����������ڽ��ܼװ��������Ƶ�RA���߷������ظ��༲���Ļ����Ǻ�С�ġ�һ��ع��Ե��о���������ȸ���ά���ķ�������3%��35%���ж����ضȸ���ά����������0%��10%����Ӳ����������0%��2%���Լװ���������ǰ��λ��ıȽ�Ҳ�õ������ƵĽ�����װ�����ʹ���ۻ�������1200��2600mgʱ����ȸ�����ά���ķ�������0%��52%�����ظ�����ά����Ӳ���ķ�������0%��5������ظ��༲���ķ����ʵ���1/1��װ����ʸζ��ԵIJ����ּ�����24��
���ܼװ���������ĸζ��Է����ʵͣ�Ҳ�мװ��������µ����ظ������ı���������������ظ��Ļ��߳�����������Σ�����ء������֯�����쳣�ı�����ϵ���Ҷ����ڼװ����ʵ�Σ�����ذ�����a.ǿ������أ���ơ������β�ʷ�������ܲ�ȫ��b.����������أ��װ���������ʱ�䳬��2�ꡢ�װ������ۻ���������1500mg�������ù���������ְ�������c.DZ�ڵ�������أ��װ�����ÿ�ܼ�������25mg�����֡������ӺϵĦ�1��
�ȵ���øȱ����Felty�ۺ�������������ά����A���ơ�����NSAIDsҩ��뻷����A���á�
1994�꣬������ʪ��ѧ�ᷢ���˶Խ��ܼװ��������Ƶ�RA���߸ι��ܼ���ָ��(��25)��ָ���Ƽ����������ʷ�������Ҹλ���λ��ߡ������͵ij���Ѫ��ת��ø������Ӧ���иλ�졣���в��˾�Ӧÿ4��8�ܳ������Ѫ��ת��ø��
������顣Ѫ���ø��������12���»�RA�����ѿ��ƵIJ��˳���
������������ʱ��Ӧ���иλ�졣����ǿ������Ƶ�ʵ�ʵ���Ҽ�����©���Ըι�ø�쳣�ļ�ʱ���֣��κγ̶ȵ�AST���߶�Ӧ�������ӡ��Դ�ָ�ϵ�����������������������82%����������80%������Ԥ��ֵֻ��27%��
Ӧ��������ʪ��ѧ��ָ��ʱӦע�⼸�����⣺a.ǡ���IJ���ѡ�����Ҫ������һЩDZ�ڵ�Σ��Ӧ���Գ�ֵ�ע�⣻b.AST��ALT�κγ̶ȵ����߶�Ӧע�⣬�ι�ø��
�����ļ�������ɳ���8�ܣ�c.�͵���Ѫ֢����˵��RA��Ե����Ӷ����Ǽװ����ʸζ������£��β�����ĵ͵���Ѫ֢��ʾ�ι��ܺܲ���͵���Ѫ֢��ԭ����ȷʱ�����೬������������������������£����೬���������ų����ظβ���d.�װ������������ظβ�ʱѪ��AST��һ�����ߣ������ָ�϶��ڼװ�����ÿ�ܼ�������25mg����������10g�IJ��˿��ܲ�̫���á����ԣ��Դ�ָ�ϲ��ɹ���������
Ϊ�˼��ټװ����ʶԸ���Ķ��Է�Ӧ���Ƽ�ÿ�ܶ�����ÿ��ʹ�üװ����ʡ������ϣ����ܸ�ҩ;�����Ա���������ЧӦ���ȿڷ���ҩ���ȫ��Ȼ����һ�㲢û���㹻��֤��֧�֣�������Ϊ�װ������������ij���ѭ������֭�е�Ũ�Ƚϸߡ��ܶ�ѧ�߽����ڼװ��������ƹ����в���
Ҷ������
Ҷ������Shiroky�ȱ���������
Ҷ������ʹ60%��ø���ߵIJ��˳���ø�Ľ��ͣ���ʾ�ι�ø���߿�����
Ҷ��ȱ�����£���
Ҷ�����б���ЧӦ������װ����ʶԸ���Է�Ӧ�����
Ҷ������������������ܶ��ٴ�������ʹ����װ�����ÿ�ܼ���������1/2��1/4����
Ҷ�����ڼװ����ʷ��ú�12��24h���á�
C.����RA����ʹ�üװ�����ʱ�����Գ��ַ�����ʱ�dz���������������Ӧ�����ٴ������ߵ��㹻���ӡ��װ�������ط�����5���ٴ����ͣ�a.���Լ����Է��ף�b.������ά����c.����Դ�Է�ˮ�ף�d.��Ĥ����Ĥ������e.�ν�ڡ�����������Ǽ��Լ����Է��ס�����RA�������������μ�����ά��������ʱ���ַμ�����ά���Ƿ��ɼװ����������൱���ѡ����зμ����IJ���ʹ�üװ����ʶ�Ӧ������һ�������ƹ����г��ַμ�����ά����ֻ��ͣҩ����۲졣����Դ�Է�ˮ����Ĥ�ײ����ܳ����������ڴ�����װ�������������ʱ����������RA�г��ֵĿ����ԡ��ν�ڵķ���Ҳ�൱�ټ��������й��װ���������RA��Ѹ�ٳ��ַν�ڵı������ٴ�����Ϊ���Ժ����̣��װ�����ͣҩ��֢״���������Դ��ڡ�
�װ�������ط��ĵ����ٴ�����Ϊ�Ǽ��Բ��̣��ɿȡ����̺��ز�����������Ҫ��֢״�������з��ȡ�ƣ�С��������ٺͺ������ѵȡ���̵����ϲ���Ⱦ���ز����ʾ�����������Ĥ���������������¡��Ӽװ�����ʹ�õ����ַ���֮���ʱ�䲻������1�ܵ�480�ܾ��С���ʼ���ַ���ʱ���װ����ʵ��ܼ�����7.5mg��3600mg��û��һ���ٴ�֢״����ϼװ�������ط���������ģ�Ӧ�����ƹ����г��ֵ��κ���������־��裬������Ʋ���ʱ����в������Ӱ��ѧ������������ϼװ�������ط��dz���Ҫ���������ز�Ӱ��ѧ���ų��װ��������µ����صķ����װ�������ط�������͵�Ӱ��ѧ���֣���˫����ʺͷ��ݽ���������˫��εף����ֱ��ֱ���Ϊ�Ƿ��ݺͼ��ʵIJ����ı䡣�װ�������ط������������ı���4�֣��ֱ��ǣ������Է��ס�ϸ֧�����ס���ϸ�����ۺͼ�����ά����������֢����Ҫϸ���������ܰ�ϸ�������κ˰�ϸ��ż���ɼ������о�ϸ���γ���ѿ�ף���������ϸ������2�ͷ�����Ƥ�����ͷ����쳣��Ҳ�ɼ���ˮ�ͷ���������������չ�������Է�����(��26)��
�װ�������ط�����ϲ������ף������ٴ���ʵ���Ҽ���ۺϷ�����������ϱ��ɹ��ο���
Kremer��(1997)����Ҫ����a.����֤ʵΪ�����Է���(���²��������֤��)��b.�зμ��ʺͷ��ݽ����Ӱ��ѧ֤�ݣ�c.Ѫ��̵������Ϊ���ԡ���Ҫ����a.��������8�ܣ�b.�ɿȣ�c.���ڿ��������£�Ѫ�����Ͷȣ�90%��d.DLCOռ��Ӧ����Ԥ��ֵ��70%��e.��ΧѪ��ϸ��������15��109/L����������Ҫ��a.������Ҫ��b.��c.�Ӵ�Ҫ���е�3����Ϊ�϶���������Ҫ��b.��c.�Ӵ�Ҫ����2����Ϊ�ܿ����Ǽװ��������µķ���
�˱��ѱ����������ͱȽϾ��мװ�������ط��IJ��ˣ����������ص�Σ�����أ������ǵ������Ժ������Ի�����ȷ���еIJ��˾�����ȷ�ļװ���������Է��ף�������������ϱ������еIJ��˷β����䲻���ɼװ���������ģ�ȴ������ϱ�����û���о���������3�����Ƿ�ȼۡ����еı����Ƿ�����ģ�����Ҫ�ı�Ӧ���ǿ��ػ�֧���ܾ��λ������������ı䣬Ӱ��ѧ��ʾ�������Լ��ʻ���ݽ����β�ϸ��ѧ�����Է��֡�
�Լװ�������ط��Ĵ���������廯��һ����������3���棬���װ�����ͣҩ��֧�����ƺ���Ƥ�ʼ��ص����á��еIJ���ͣ�üװ����ʺ�֢״�ɵõ����⣬�еIJ���Ч�������еIJ���������ͣҩ���еIJ���֢״��ת���Կɼ���ʹ�á�֧��������Ҫ�Ǻ���֧�֣��������������ȡ���Ƥ�ʼ��ؿ��Լӿ�װ�������ط��Ļָ��������еIJ��˲�����Ƥ�ʼ��أ��������װ�����ͣҩ�Ϳɻ����ȫ���⡣��Ƥ�ʼ��ص��÷�����������������60mg/d��֢״�����2��4���ڼ�������û�м��ؼ��������з������ı�����������Ҫ
����֧�ֺ������Եķμ��ʺͷ��ݽ�����Ӧ�ü��ص�ǿָ����û��֤�ݱ�������
Ҷ������
Ҷ�����Ի���װ���������Է��ס�
�װ�������ط��ķ����ʺܵͣ�Ϊ2.1%��5.5%�������װ�������ط�������ȫ������С���ֲ������������Է����еĿ��Բ�����Ⱦ�������ϲ�֢���Ӷ������������ڼװ���������֮ǰӦ�˽ⲡ�˵ķβ���������⣬Ӧ���Ѳ�����Ӧ�üװ������ڼ�Է����ķβ�֢״Ҫ���㹻�����ӣ���ʱ�������������ϣ����ڴ�����
D.ѪҺѧ�쳣��ѪҺѧ���쳣������ϸ�����١�ѪС����١�����ϸ����ƶѪ��ȫѪϸ�����١��ڼװ��������Ƶ�RA���߷�����С��5%���ٴ������Ե�ȫѪϸ�����ٷ�������1%��2%������ѪҺ�쳣��Σ�����ذ����������ܲ�ȫ������
Ҷ��ȱ�����������������Բ�����Ⱦ�����ơ��͵���Ѫ֢�ͺ��ñ����ᡢ
�ǰ�������ҩ�ƽ����ϸ�����(MCV)���������߿�����ΪѪҺѧ�쳣����ʾ�����е�ѧ����Ϊ��ϸ������ֲ�(RDW)�ķ�Χ�仯����MCV�ı仯������ԤʾѪҺ�쳣���磬���ɿ�����MCV�쳣����ʱ������ϸ����
Ҷ����ά����B
12Ҳ�DZ�Ҫ�ġ���װ������շ�ѪҺѧ�ı�ʱӦ������
Ҷ����һ���ڼװ�����ʹ�ú�24��48h��������Ч��������װ����ʵ�ͬ����Ѫ����Ƥ�ʼ��ػ���Ѫ�������ӵ�ʹ�öԻ���װ����ʵ�ѪҺ��������Ч��
E.������ϵͳ���ԣ��װ����������������ϵͳ�ĸ���Ӧ���ֶ�����������������ʶģ����������ˡ���˯��ͷʹ��ƣ����֢״����Щ֢״�����ڷ�ҩ��24h�ڷ��������������ҩ��ʱ���ϵ����ȷ����������װ�����(��1mg/m2������)��������Է�����Ϊ15%���ң�ͨ���ǿ���ļ����������Բ�������Ϊ����ʶģ����ƫ̱��Ҳ������Ǩ�������ʲ���һ��ع��Ե��о���ʾ��ʹ�üװ��������Ƶ�RA�����У�������ϵͳ���Եķ�������1%��35%���ȡ�
F.�װ���������ĹDz����װ����ʹDz����������Թ��ʼ��٣������ǹ�Ƥ�ʶ�ʧ����֫�ֹǡ���Ǻ��Ź�ѹ���Թ��ۣ����ͱ�����ͻ���ľ�����ʹ������ʱ���ء���ͨƽƬ��ʱ���ܷ��֣�99mTc����ɨ�������а�����RA���߷����������ֹ��¶˵Ĺ�������ʹ����ʱ������Ϊ�ؽڻ�Ĥ�ķ�����
�װ����� 10mg��ע��Ĥ����Ƥ�ʺ�С���ڼװ�����Ũ�Ȼ�ܸߡ�����ʵ������װ����ʿ��Ժ��������Ƴɹ�ϸ����ֳ���̼��ƹ�ϸ���ľۼ����Ӷ����ӹ��ƻ���Ҳ�������ƹ��۵����ϡ�
G.�װ����ʵ����������ã��ܶಡ�˷��üװ����ʺ����ַ������������ʡ��ؽ�ʹ�ͼ�ʹ��֢״������������Լ�����Щ֢״��������С����������ҩ��Ϊ�ڷ���ִθ�ҩ���Լ��ᷴӦ��
������ļװ����ʿ������������˥�ߡ�С�����װ�����Ҳ��������С���˹��ʺ���С�ܹ��ܵ��½���ͣҩ���ʹ�����ָܻ����������װ�������NSAID��ҩ�����ʱ��������Ķ��Խ�����ء�С�����װ���������ʱҲ�ɳ����ѷ����������յ��ĺ�߷�Ӧ��ݡ�����Ƥ��Ѫ���ס���ή���پ��������鷿Ů�Ի�Ҳ�����ڱ�����ͣҩ��������Իָ��������װ����������Ե��»�̥���á�
�װ������������Ƕ��صģ�������Լ8%����������ҩ�����»������֣����Ҿ��������ڹؽ���֢����ʱ�����͵������Ƕ��С��ڣ���ʱΪʹ�ԣ�����ָ�Ͳ�������λ�����������ֺ���������ϳ��֣�λ�����ࡢ�κ���Ĥ�ϵĽ�ڿ��������ص��ٴ�֢״���װ�������ؽ�ڵķ������ܺ��Ŵ������йأ���Ϊ��HLA-DRB1
*0401�����(OR8.7��95%C.I.2.2-36)
2����Խ�ǿ����ϵ�����ֽ�ڵ���֯ѧ�����ʪ������ƣ����γɿ�����
����A1����ٽ���˾�ϸ���ۼ��йء�
�װ�����Ӱ��
���װ����Ĵ�л��25mg/�ܼ����ļװ����ʿ���ʹѪ��
���װ���Ũ��һ�������ߣ�С�����װ����ʲ��������ı�Ѫ��
���װ���Ũ��ˮƽ������������
���װ�����л�쳣�Ļ��߱�����߾��衣����
���װ�������Ѫ�ܼ�����Σ�����أ�����ǰ�����ƹ����е�ѪҺ����DZ�Ҫ�ġ�
���ڼװ����ʿ��Բ�����������ЧӦ���ʳ���ʹ�ÿ��ܻ����Ӹ�Ⱦ�ķ����ʡ��װ�����ȷʵ����������ͨϸ����Ⱦ����״����ͻ����Ը�Ⱦ(�������������ϸ��������ū�����Ϳ��Ϸ��ҳ��)�ķ�������һ����ʺܵ͡�����Ƥ�ʼ��غ�������������ӡ���Ⱦ�IJ�λ����ں��������������Ƥ���������Ⱦ�ķ�����Զ������Ƥ�ʼ�������ĸߡ��װ����ʲ�δ����Ϊ��һ����������ҩ����ܼװ��������ƵIJ���Ҳû�����������ķ����ʡ�һЩ����ʹ�üװ����ʵ�RA�����У����ֻ��ǻ�����ܰ�������Խ϶ࡣ����Щ�����У����װ�����ͣҩ���ܰ�����������������ڴ������ֹ�ϵ���װ����ʱ���Ϊ���ܰ���������ء������ɻ���ǣ�����Щ�ܰ����кܶ���Լ�EB��������EB�����������ܰ����ķ�����������ԡ����Լװ��������ܰ���֮��Ĺ�ϵ�����һ���о�����������EB������Ⱦ��RA����ʹ�üװ�����Ӧ������
���ڼװ�������Χ�����ڵ�ʹ����������Ƚϴ��е�ѧ����Ϊ�װ����ʿ������������Ⱦ�Ļ��ᣬӰ���˿����ϣ���������֢����������ǰ�������ͣ�üװ�����1�ܡ���Grennan�ȹ۲�388������������RA���ˣ���������Χ������ͣ�û�ͣ�üװ����ʣ���������üװ����ʵIJ��ˣ������������Ⱦ�Ͳ���֢�ķ����ʲ�����������������ǰͣ���װ����ʣ������ط�ʪ���Ļ��
���������е�RA���˶��ʺ�ʹ�üװ����ʣ�����ѡ������DMARD�������˶��죬Ӧ�ۺϲ��˵ĸ���������������������ܲ�ȫ�������иβ���β����������ơ�����Ȳ��˶�Ӧ����ʹ�üװ����ʡ���Ϊ�װ�������Чʱ��Ͽ죬������Ϊ����ϻ�ؽڹ��������˵��Ƽ���ҩ����ҩ֮ǰ����Բ��˵�ȫ������Ͳ���Ļ��������ϸ�����ۣ���ҩ������ҲӦ���ڼ�⣬��ʱ������ҩ����
(2)�������أ�
���������ص�ҩ���ص㣺��������(Leflunomide����Ʒ����
������)���������������������ߵ��ںͿ���ֳ���ԣ�1998�걻FDA���������ʪ�ؽ������ơ�����ģ����ʾ��ҩ�������ƹؽ��ס����������Լ�����������ֲ���涼��Ч����
�������صĻ��Դ�л����A77 1726��������������ø��������������������ø(DHODH)������ø����ऺ���������һ����(rUMP)�ĺϳ�������Ҫ�����á������Ƶ���һ����������ा���ϳ�;�������ٲ��衣���ڼ�����ܰ�ϸ������ֳʱ��Ҫ����ळ���չ��Լ8����Ϊ�˴ﵽ��һҪ���ܰ�ϸ�����붯����ऺϳɵľ���Ͳ���;��������DHODH����ֹ�ܰ�ϸ���ۼ��㹻����ण��Ӷ�Ӱ��D
NA�ĺϳɣ������ܰ�ϸ������ֳ�ܵ����ơ��о�����������A77 1726�����������ἤø���ԣ�����ø��G0/G1��Tϸ����Bϸ�����źŴ����������á��������������Ƽ�������Ҫ������ΪDHODH�Ļ����ܵ����ƣ��Ӷ�����һϵ�е�Ӱ�졣Manna�ȷ����������ؿ�����ֹ�������������յ��ĺ����Ӧ�B(NF-��B)�����-��B�����ữ����ֹ��-��B����ø(IKK)�������AP-1��c-Jun Nĩ�˵���ø�ļ�������������������յ��ĵ������������ػ�������������������ϸ��������������������������ǰ��Ի�Ĥ��֯���л��ʱ���֣����ƺ�Ĥ��֯�о���ϸ����ICAM-1��VCAM-1��IL-1�ºͻ��ʽ�������ø�������١�
�������ؿڷ���ܿ���θ�����ڱ���л������Դ�л����A77 1726��������Ҫ���A77 1726��Ũ���ڸ�ҩ��6��12h�ﵽ��ֵ����˥��Լ14�졣ҩ����Ҫ�����κͳ���л������ѭ�����������ղ���������и�ռ40%���ҡ�������������Ӧ�õ�ʱ�䲻�����й�ҩ��֮�������û������˽�ú�������֪����ƽ��������A77 1726�ķ�Ũ�ȴ�40%��
���������ص��ٴ�Ӧ�ã��������ص��ٴ�Ч���Ѿ���һЩ�ٴ�������֤ʵ��Smolen�ȶ�358�����˸����������ء���������ऺͰ�ο����˫ä�������鷢�֣���4�ܺ���������ٴ�Ч���������ڰ�ο���飬������������Чʱ�����(4��8��)����2��ʱ��������ؽ��ƻ����̶������������������������������������ٴ����Ƴ̶Ⱥ�ʵ���Ҽ�鷽��(����ESR)û���������죬�����ڹ��ܲз�������������������������������ड���1���2��Ĺ۲��У������������HAQ������ʲôʱ�ζ�������������������飬��������ʱ����ӳ����丱���ò������ӡ�Strand�Ƚ��������غͼװ����ʽ����˱Ƚϡ���12���µĹ۲��У��������ط������õ�ʱ��Ҫ�Կ��ڼװ����ʣ��ڹؽ��ƻ����̵ıȽϺ��ܸ��Ƴ̶��ϣ����������������ڼװ������飬����Ϊҩ��ĸ����ö�ͣҩ�IJ���Ҳ�ȼװ�������ࡣEmery�ȶ��������غͼװ����ʽ�һ�����бȽ�Ҳ�ó������Ƶķ��֡�����A77 1726�İ�˥�ڽϳ��������������������Ҫ2���»������ʱ����ܴﵽ�ȶ���ѪҩŨ�ȡ�һ����÷���ǰ3���ȸ�������100mg/d�Ժ�10��20mg/dά�֡���������һ�������������Ϊ�����ö����ܼ�֣������жϼ�����ٸ�����ѧ�߽�����Ը��ݲ��˵IJ�ͬ��������Ժ�ļ���������ÿ��100mg�����20mg��
Kremerָ�����������ؿ���������वĺϳɣ������ܰ�ϸ������ֳ�����װ���������ϸ�����ӵIJ��������ʵ�����ϳɣ�������Ҫ
�������ͷš������������غͼװ����������ڲ�ͬ�Ļ��ڣ���������ʹ�ý�����ЭͬЧӦ��Weinblatt�ȿ������������غͼװ���������ʹ�õ�������۲����Ϊ30���ڼװ����� 17��4mg/�ܼ����²�����Ȼ���RA���ˣ����Ƕ�����10��20mg/d���������ء�52���Ժ�57%�IJ��˴ﵽACR20���������Ʋ�û��Ӱ������ҩ�Ĵ�л�����������Ժܺá���������ʱ�����õķ����¼���152�𣬶�Ϊ�ᵽ�жȣ������������θ������Ӧ(��к�����ġ�θ��)������Ƿβ�֢״(���ԡ��������ѡ�����Ⱦ)��Kremer�ع���������������Ľ������266�����RA�IJ��ˣ�������ܼװ����� �������ػ�װ����� ��ο�����ơ�24�ܺ�װ����� ����������ﵽACR20�IJ���Ϊ46.2%�����װ����� ��ο������ֻ��19.5%�������õķ�������ǰ�Ĺ۲����ƣ�������ҩ������2.3%�IJ��˸�ø������������ֵ3��������������0.8%����Щ�ٴ���������ʾ������������װ������ڻ��RA������������ʹ�����ڼװ����ʵ���ʹ�ã��������������á�
�������صĸ�����ͨ�����Ƚ��ᣬ���ҷ�����Ҳ���ߡ���������Ҫ��θ������Ӧ�����и�к��22%��26%������9%��13%��Ƥ��ռԼ12%���������ѷ�ռ��Լ8%����Ѫѹռ6%���ң���ø����(AST��ALT)ռ6%��10%���ָ����ö�����ҩ����������ڷ��������Һܶ��Ҫͣҩ�Ϳ��Ժ�ת����δ����ѪҺϵͳ���渱���ú�Ⱦ���ʵ����ӡ��������ؼ�������20mg/dʱ�����õķ��������ӡ�
�������ص�ʹ��ʱ�䲢���ܳ�����۸�Ҳ�Ƚϰ���Ŀǰ�в���ȡ���װ����ʡ�����ѧ�߽���Լװ����ʵ��÷�Ӧ���ѵIJ��˿��Լ����������أ����ڲ������ܻ���ʹ�üװ�����ʱ�������װ����ʡ������������أ������ø���ߵ����ñȽ�ͻ����FDA����ʹ��ǰ�Ϳ�ʼʹ�ú�ÿ�¼���øˮƽ���ȶ������ÿ2��3���¼��1�θ�ø�������ҩ�����и�øˮƽ��������2���������ޣ�����Ҫ��ҩ������������øˮƽ����3��������������Ҫͣҩ������ϩ�����������ӿ��������ص�������ڷ�8g����ϩ����3��/d��24h����Խ�ҩ��
Ѫ��Ũ�ȼ���40%��48h�����50%��65%���������ؾ����»����ã����������и�������ҩ������������ʱ��Ҫ����2�����ҵ�ʱ�䣬���ʹ�ø�ҩ���Ů������뻳�б���ͣҩ������ʹ�ÿ���ϩ����ʹҩ��������������ʪ��ѧѧ���ڡ����ʪ�ؽ�������ָ��2002�桷��ָ�������Ե����������β��������Ը��ס����ص���������״̬������ֵĻ�������ʹ������ƽ����Ϊ�����������ƵĽ���֤��
(3)��������ण�
����������व�ҩ���ص㣺20����30���ĩ��Svartz�״ν�
��ɳ����(
5-����ˮ����)��
�ǰ����ͨ��ż�������ӣ��ϳ�����������ल���1942�걨�������ڷ�ʪ�Զ�ؽ��������Խ᳦���������Ʒ�Ӧ��1949��Sinclair��Duthie�����˱Ƚ���������ड����Ƽ��Ͱ�ο�����õķǶ����ٴ����������ý����ʾ��3���Ƽ���Ч���������Բ��졣�ڴ˺��30���ڸý�����㷺���ܣ����Ҷ�����������ڷ�ʪ�Լ�����Ч���о�Ҳ������ֹ�ˡ�ֱ��1980��McConkey������74�����ʪ�ؽ��IJ��˲����������������ȡ�������˹���Ľ����4�ܺ��ٴ�֢״���Ը��ơ�C��Ӧ����Ѫ�������½�����֢״��������8�����¡��˺ܶ�������ٴ����鶼֤ʵ�������������RA�е��������á�
��������व�����ֻ��10%��20%�������յ�ҩ��95%������
Ѫ������ϣ���ҩ��4��6h
Ѫ�����ֵ����˥��һ����6��17h���ֵ�ҩ���ڷ��ú�᳦���ڴ˴���ϸ���ֽ��
�ǰ������
��ɳ������ǰ�߿������ڷ�ʪ������������ã����������������Խ᳦�Ļ��Գɷ֡���������वĴ�л������������������������Ӱ�죬���������ÿ�ĸ�����Ч�ϲȻ����û�з���
�ǰ����Ѫ��Ũ�Ⱥ��ٴ�Ч��֮��Ĺ�ϵ�����������ҩ������ѧ���ٴ�Ч�������õķ����ʲ��������Ӱ�졣
�����������������RA�������Ѿ�����50�꣬�������û��ƻ�û����ȫ�������������ि���Ӱ��ܶ����Խ��ʡ���������ण�����̶�����
��ɳ�����������ã���������ɶ��κ�ϸ���ͷŵĻ������ʼ�������ҩ�ﻹ���Ʋ�ͬ��ǰ���������ʵIJ���������IL-B4��5�ǻ���ʮ̼��ϩ���Ѫ˨��A2��������������ƿ��Լ���ѭ���ļ����ܰ�ϸ��������Bϸ�����ԣ���������IgM�����ʪ���ӵζȣ������ܰ�ϸ���Դ̼��ķ�Ӧ��10%���ϵIJ��˻����Գ��ֵͱ�����Ѫ֢���������������16�ܺ���Ըı䳦�Ĥ�ܰ�ϸ����Ⱥ�ķֲ�����������ऻ�����������IL-1����IL-1�º�������������-��Ũ�ȣ�����IL-6�IJ�����Carlin����ͬ��֤ʵ��������ऺ�
�ǰ�������������Ƶڶ���ʹ�����������Һ�ơ����Ͷ�����������
��������Щ���ÿ���������ҩ����
��֬øC��������������������ϵ���ˮƽ�����ã��Դ˿��ܽ���ҩ�����֢���ʺ��ܰ�ϸ�����ܵ����á���������ऻ����Դ�ʹϸ���п�����
�����Ļ��ۣ����������ڼװ����ʵ�ҩЧ���á�
����������व��ٴ�Ӧ�ã��������������RAʱ���Լ���ȫ�����ؽھֲ�����֢�����Ƴ����������Խ���Ѫ����C��Ӧ���ס��������������˫ä����ο�������ٴ�����֤ʵ����������� 3g/d���ٴ���Ч���������߶���ʾ�˽ϸߵ������ж���(Pinals���о���28%)����Ҫ�������������ĸ����á��ڶԲ�������12���µ�RA����ʹ����������व��о��У���������Բ����ǹؽ���ʴ���ٵ����ơ���һ��48�ܶ�����RAʹ����������ऺ�
������ıȽϵ��о��У���������ल������ø��죬������24�ܡ�48�ܺ�3�����ù������������������ʾ�˸���Ĺؽ���ʴ���̡�
�ڴ��о��У������������ҩ��4�ܼ�����Ч�����Կ��ڿ�űҩ��һ��4����������Ч�������ʱ�����ܲ���Ч����Ӧ���ǵ������ơ�McConkey�����������������RA����Ч��������1.5g/d���������ձ�ļ�����2g/d����Ƭ�������β��з��á�Ϊ���ٶ�ҩ��IJ����ܣ����Դ�0.5g/d��ʼ��ÿ������0.5g��ֱ�����Ƽ���Ϊֹ���о�������2g/d��3g/d�ļ������ٴ���Ч��û�����������˼������Ӳ�һ����������Ч����������व���Ч����Ƽ�����ù���൱��������ҪС��������Ч���ڿ�űҩ��
��ŵ�����������ʶ������װ����ʣ���Ҳ�е��о���Ϊ�����������װ����ʵ���Ч�൱����ŷ����������व�ʹ�ý϶࣬������Ӣ����������Ϊ��ѡ��ҩ��
�������ǵ�ע����ת����������ऺ�����ҩ�������ʹ�á���������ऺͼװ����ʵ�����ʹ����ʾ���ٴ�Ч���еȳ̶ȵ����ӣ������뵥����ҩ��û��ͳ��ѧ���죬�����ò������ڼװ����ʵ��á���102��RA���˵�Ϊ��2��˫ä�о����֣��װ����ʡ���������ऺ�
�������������ʹ�õ���Ч����������3��ҩ�ﵥ��ʹ�á��Ժ������RA����ʹ����������Ҳ���ֿ��Բ����������ٴ�Ч������ʾ�����յ���֢�Ļ�������ӻ��ؽ��ƻ��Ľ�չ��
��������वĸ����ü���27��һ����Է�Ϊ���ࣺһ���Ǽ�������ԣ����ڿ���Ԥ�ڵģ���ͷʹ�����ġ�Ż�¡���������Ѫ��ƶѪ����һ��Ϊ��̬��Ӧ�ԣ�������أ��Dz���Ԥ�ڵģ���Ƥ������ϰ���ƶѪ��������������Ѫ�ȡ������ĸ����ö����ڿ�ʼ���ƺ�2��3���³��֣����ټ��������ڼ������Ӧ�ķ�����������������ƹ����еļ�����28��
(4)��űҩ��
�ٿ�űҩ��ҩ���ص㣺��űҩ(antimalarials)�״��������ʪ�ؽ���������1951�꣬Ŀǰ�ٴ��ϳ��õ���
���(chloroquine��CQ)��
�����(hydroxy-chloroquine��HCQ)��
�����������ϸ���˺���ø�壬����Ч���Ϻã�����������ҩ����������
��űҩ��ҩ�����ñȽϸ��ӣ������в�ʮ����������о���Ϊ����űҩ����ͨ���ı�ϸ���ڵ�������Ӱ��ϸ���Ĺ��ܣ��Ӷ���������֢�����߷�Ӧ��ø���Ե�һϵ��Ӱ�졣��Щ���õ�ʼ������(�ֳ�����ø������)���Է�������Ϊ��űҩ�������ԣ����Խ�����ø�壬ʹpHֵ���ߣ��������������Ի�����ø���ԡ�
������������Ƶ��ķ��ںͰ��ڼӹ����̡���űҩӰ�����߷�Ӧ�Ķ�����档Fox��Kang��Ϊ����pHֵ�ĸı��Ӱ��������ԭ�ӹ���������ԭ�����������Ҫ��֯���ݿ�ԭ�Ľ�ϡ�
������������ܰ�ϸ���Դ̼�����ֳ��Ӧ�������ں����ⶼ��������NKϸ���������ܰ�ϸ����ת���ͽ�ϸ���Ļ��ԣ������Ǧ������ʪ���ӵ����ɼ��٣��ܰ�ϸ���ͳ���άϸ����ֳ�ܵ����ơ������⣬
������Լ���ϸ��������ʹ
RNA�ı���Ӷ�����IL-1��IL-6��������������-����IFN-�õ����ɣ�������������
Ѫ�����ͷš�
���������ͨ������IL-2���ɺ�Tϸ����IL-2��Ӧ������Tϸ������ֳ����űҩ�����Լ��ٺܶ�ø�Ļ��ԣ�����
��֬øA2����������ø�͵�����ø�����˶�øֱ�ӵ����������⣬��űҩ�������ȶ���ø��Ĥ��������ø����ø���ͷš���űҩ������������ϸ�������������ɹ��ܡ�
����ڷ�����Ѹ�ٶ�����ȫ��һ�����2��3hѪ��Ũ�ȴﵽ�߷壬�������ö�Ϊ75%���ֲ��ݻ��㷺�ֲ���ȫ������Ƣ�������Ρ��ġ��ε���֯��ҩ��Ũ��Ϊ
Ѫ���е�300��500����
�����
Ѫ����˥��Ϊ3.5��12�죬ѪҩŨ����Ҫȡ������ֲ���������й������˥ʱ�������������
�����Ҫ�ڸ����л��ԭҩ�����л������Ҫ������й����Ʒ�Ժ��к�ɫ�ص�Ƥ�����۵�����֯�кܸߵ�������
�ڿ�űҩ���ٴ�Ӧ�ã���űҩ����û�б���Ϊ�ܼ����ؽڵ���ʴ������ΪDMARDֻ��������ʷ�Ľз�������ʹ��
�����
���������RA�Ķ�������������ؽ���֢���Եõ����ơ������Ķ����Ķ����о�����ʾ��������RA�п�űҩ���Լ��ٹؽ���֢�ͳ������������ظ����õķ����ʺܵ͡��ڿ����Ե��о��У�60%��70%�IJ��˿������Ե��ٴ�Ч����1991��Davis������Ѫ������30mm/1h��C��Ӧ������20mg/L�Ҳ������IJ��ˣ�ÿ��ڷ�400mg
������нϺõ���Ч����ʾ��űҩ�������ں���ȵ�RA�����õ��������ã��˵�ҲΪ������ʪ��ѧѧ�ᡶ���ʪ�ؽ�������ָ��2002�����϶���
�������RA֢״���Ƶ�Ч������������़�������A�൱�����Ҳ���HCQ���������������ʹ��ʱ��Ч�������
���������ʹ�ò����ܼ����ǹؽ��ƻ��Ľ��̣�������������RA�����������Ʋ��˵ij���Ԥ�������˽�HCQ���װ����ʺ������������������ʹ����������RA��������Ч����������3��ҩ���ã����ҿ��Ը��õؼ���ǹؽ��ƻ���
��űҩ����Чʱ��Ƚ�����һ����3��6���£�����������ԣ�Ŀǰ�н�����һ�����ýϿ��ҩ��(��װ�����)���õ������ü���Ϊ��
���4mg/(kg��d)��
�����6mg/(kg��d)�����һ��Բ�������RA����ʹ�ò�ͬ����(400��800��1200mg/d)��
��������Ƶ��о����֣�������������Ч��á�Weinblatt��Ϊ
�����
���������������ԣ�����������Ϊ
���3��4mg/(kg��d)��
�����6��7.5mg/(kg��d)����������ٴ��۲췢�֣�
�����ÿ�����������400mgʱ�İ�ȫ�Ժܺá�
��űҩ�ĸ����ñȽ��٣��䷢��������йء��ϳ�������θ������Ӧ����ġ�Ż�µȣ�������ʹ��к���з�����Ƥ��Ҳ���ڳ����ĸ����ã����䷢�����˶��졣��ϵͳ����ĸ�������ͷʹ���ۻ���ʧ�ߺͽ��ţ����صķ�Ӧ���٣����ż����ļ��ٴ����档���ⲡ��ķ���һ����٣�������֫���˼�������(һ���ڿ�ʼ�������º�)���ͼ�����ɳ����쳣����űҩ���۲���Ӱ����3���棺��������ϰ�����Ĥҩ�����������Ĥ���䡣ǰ���ֲ��������ת����3�ֲ�����Դ������õ�ʧ���������ҵ��ǣ��ڳ������Ƽ����·����ʷdz��͡���1960��1989���ܹ�ֻ������18�����˷���������Ĥ���䣬������16��
������ļ���������7mg/(kg��d)��Ŀǰ��Ϊ
�����6��7mg/(kg��d)�ļ���һ�㲻���������Ĥ���䡣һ����������Ĥ������֢״��Ӧͣҩ�����ôٽ�
�����й��ҩ����
�Ȼ��������ά����C�����������غ�2-�ϻ������ȡ����⣬��űҩ������������˥�ͷ��Ҵ������͡�
��űҩ�ĸ����÷����ʺܵͣ�����Ϊ�DZȽϰ�ȫ��DMARD�����Ҽ۸�Ҳ������ʹ��ʱҲ����Ҫ���ж��ڵij���ʵ���Ҽ����Ѫϸ���������������ܵȣ�������Ҫ���ڽ����ۿƼ���Լ�ʱ���ֿ��ܵIJ��䡣���еĸ�Ů������ʹ�ã���Ϊҩ����ܻ�Ӱ�캢�ӵ��������е�ѧ�߽����ڿ�űҩ�����ڼ�ɲ������29�ķ�����
(5)�������ʣ�
���������ʵ�ҩ���ص㣺��������(azathioprine��AZA)��һ�����ʵ������������Ѹ�ٱ�ת����������(6-�ϻ�����)����һ���ܴλ����ʺ��ս�����ø(HG-PRT)��������������ᣬ���߾��������Ƽ�����ĺϳɡ���Ϊ��������
��������������ǰ�壬���Ƽ�����ĺϳɽ���������D
NA�ĺϳɡ�����������ϸ������������ҩ�����S��ϸ�����������Ҫɱ��Ѹ�ٷ��ѡ���ֳ��ϸ�����������ʿ�������ϸ���鵼�����߷�Ӧ����Һ���߷�Ӧ�����ڳ��εĻ��ٴε�����Ӧ������������á��������ʶ�Tϸ�����������ñ�Bϸ��ǿ����������NKϸ�����ԡ��������ʾ��п������ã����Ի���RA�Ĺؽ����ͺ���ʹ��
���������ʵ��ٴ�Ӧ�ã���������һ���50mg/d��1��1.5mg/(kg��d)��ʼ������������ÿ�����1��2�������ӵ�2��2.5mg/kg��ÿ1��2������25mg����ʹ���˾��и��õ����ܡ������������ʶ�Ѫ�ܴ̼��Խ�ǿ��Ŀǰһ�㲻������ҩ���������ʿ�ʼ��ҩ�������ñȽϻ�����һ��3��6������Ч��һЩǰհ�Ե��ٴ�����֤����Ч�������װ����ʣ������������ϼװ���������RA��Ч��Ҳ���ȼװ����ʵ�����Խ����������Ŀǰ�Ѿ���������RA�����ƣ����Dz��˶�����ҩ�ﲻ���ܻ�Ӧ���ã�����RAȫ�����ֻ�ϲ����������֯����RA���ߡ������������ٴ������ձ��Ӧ������Ϊ������Ƥ�ʼ���������ҩ��������SLE������������������
�������ʳ����ĸ�������θ�������ʣ��������ĺ�Ż�£������˯ǰ��ҩ���Լ���θ������Ӧ��15%��30%�IJ��˻����ڴ˸����ö���6������ͣ�á���ø�����߿ɼ���5%��10%�IJ��ˣ����صĸζ��ԡ���֭�ٻ����ټ��������ԵĹ�������Ҳ�ϳ�����������йأ������ڼ�Ӧ�ö��ڼ��Ѫ�����صĹ������Ʒ����ʽϵͣ�����Ϊ�Ƕ��������ʵ��ط��Է�Ӧ�����ֲ����еĴ��������ʼ�ת��ø���Զ��ϵͻ�ȱ����������������ø�ĺ���������Ա���ʹ�ú������ع������Ƶ��¼������˱���������������������ֲʱ���������ܰ���ֳ�������ķ����ʣ����Ǵ��౨����δ����RA�����ơ�
(6)����������
�ٻ���������ҩ���ص㣺���������ǵ�������������Ϊ���Ե����ʣ�����ϸ����P450���������ɾ��л��ԵĴ�л����Ӷ�ʹD
NA˫���������ᣬ�谭D
NA���ƣ�ʹ��˿���Ѳ����������С���������Ϊ���ڷ�������ҩ�����ֳϸ���ͷ���ֳϸ������ɱ�����ã����Ǹ���ϸ�������жȲ�ͬ��������������ʹTϸ����Bϸ���ľ�����Ŀ���٣������ܰ�ϸ����ֳ�����ٿ������ɣ��������������ڽ����е�����Ӧ����̡�����������B�ܰ�ϸ��(������Ϣ�ͱ������ϸ��)���������ñ���Ϊ�ڸ�ҩ���ٴ������з�������Ҫ��Ӱ�졣
���������ڷ��������ã��ܿ챻��л�ɻ��Բ���������������˥����2��8h���ֲ���ʩ��12mg/kg 24h��
Ѫ�����Ѿ��ⲻ����������ԡ����������ֶ������Ե���ʽ��������й��Ȼ��Ҳ��10%��20%��ԭ���ų��������в��ֻ��Բ��
�ڻ����������ٴ�Ӧ�ã�1951�굪����Ϊ��һ���黯��������������RA�����ƣ��˺���������Ϊ����RA����Ҫ�黯���������������Ը���RA��֢״��Ҳ������һ���̶��Ϸ�ֹ����ʴ���ڷ�����Ϊ1��2mg/kg����100mg/d��������ҩ200mg��������ҩΪÿ��2�Σ�ÿ��200mg�����ܻ���������RA��һ������Ч�������ڳ���ʹ�õĸ����ýϴ����ٴ�Ӧ���ܵ����ơ�ĿǰFDA��û����������������RA�����ƣ���ѧ����Ϊ�����������ʪѪ����ʱ���Ծ���ʹ�û��������������������Թؽ��װ������������ڸ�����ʹ�û�������֮ǰҪ�����ٴ�����ͷ��ա�
�������������ĸ�����Ϊ�������ơ���Ѫ�����ס����Ӽ��١��ѳ�����˥���ѷ���θ������Ӧ����ġ�Ż��һ����ᣬ��ע���ҩ�Ƚϳ�����һ�����12h���Ҽ�����ʧ���ѷ��ķ����ʱ�ʹ�������黯��Ҫ�ߣ��������ҩ3��4�ܺ����ڻ��������Ļ��Դ�л��������Һ�ų��������д̼����ã��ʿ��������Ѫ�����ס���������ż���շ����װ���һ����ڻ���������������12gʱ���������ҩ;���ء�
�����ڼ�Ӧ���ڼ��Ѫ���棬����������Һϸ��ѧ��飬�������˶��ˮ�������������Ӷ����ٻ���������л�����ڰ�����ͣ����ʱ�䡣��ѧ�߽���ͬʱʹ����˾���Լ��ٰ����ԡ�
(7)������A��
�ٻ�����A��ҩ���ص㣺����ù��(cyclosporine)��һ����֬�ԵĻ�״���ģ���Ҫ������������ֲ�������ڴ����ʪ�ؽ��������������۲��ȵ����������Լ�����Ҳ����Ӧ�ã���Ӧ�ý϶���ǻ�����A(CsA��CyA)��
����ù�ؿ�����������(cyclophilin)����γɸ�����ø�������Խ�ϲ����ƸƵ�����ø(calcineurin)��������һ��˿����-�հ������ữø�������ữø�����ƿ��Է�ֹ����Tϸ���а�Һ��������ϸ���˵���λ��������λ��ϸ������(��IL-2)����ת¼��Tϸ������������ġ����Ի���ù�ؿ�������CD4 T�ܰ�ϸ�����Ժ�����Th1ϸ�����ӵIJ���������CD40����((CD40L)��T�ܰ�ϸ���ı����һ�����û��ֹTϸ��ͨ��������CD40L;����Bϸ�������źš�
������A�������սϲ�ұ仯�ܴ�֬��ʳ�������������գ��������öȴ�Լ30%�����ʱ��Ϊ1��8h�������˥��Ϊ3��20h��ҩ�����պ�㷺�ֲ������ڣ�����Χ��֯�е�Ũ�ȴ���
Ѫ��Ũ�ȡ�ҩ����Ѫ����
Ѫ�����ס���ϸ����֬����ϡ�������A�����ڵĴ�л����й��Ҫ���������ص�Ӱ�졣һ��P-�ǵ���(P-GP)������һ��ҩ�������ã����Խ�ҩ���绷����A�ȱó�ϸ���⣬�ñ��ڳ���Ƥϸ�����б����һ����CYP3A4øϵͳ��������A��Ҫ����ø��л������øϵͳͬ����С����Ƥ���о��л��ԡ����P-GP����ҩ������룬CYP3A4��ʹҩ��Ĵ�л���������������ƻ�����A���������öȣ���������������Ӱ���ҩ�ﶼ����Ӱ�컷����A��ѪҩŨ��(��30)��
������A�����ڿ��Ա���л������20�ִ�л��ڷ�������A�����ֲ�ͬ����ʽ���ϵ��������䷽(��Ʒ��Sandimmune)���µ�����䷽(��Ʒ��Ueoral)���¼��͵Ĵ��ʱ����ϼ�������25%��ҩ������Ũ�Ⱥ�Ũ���������������Լ50%���¼���Ŀǰ�Ѿ���ȡ�����ϼ��͡�
�ڻ�����A���ٴ�Ӧ�ã�1979��Herrman��Mueller�״ι۲��˻�����A��RA�е�Ӧ�ã���ʼ�ļ����ܴ�(����10mg/kg)�����������صĸ����á���һ��ʹ��С����������A����RA�����˫ä��ο������������Dougados�Ƚ��С����������52�����ˣ�������A��ƽ��������5mg/(kg��d)��һ���۲���4���¡�������54%�������õ�����Ч������ο����Ϊ8%����������13��Ѫ������������50%��ҩ���������1������12���ָ��������Ժ�ܶ��ٴ����鶼֤���˻�����A������Ϊ��ҩʹ�û�����������ҩ�ﶼ���Ի���RA��֢״�������ؽ��ƻ��Ľ��̣����Ҵ����ʹ�õ�Ч��Ҫ����С���������Ƕ���Ҳͬʱ���ӡ��ܶ��ٴ�����ʹ�ò�ͬ��ҩ�������ͼ�ҵ�һ����Ѽ�����ʹЧ����ö�������С��Dijkmans��Ϊ2.5��3.8mg/(kg��d)�ļ�����ƽ����Ч�Ͷ��Ե���ѷ�Χ��Jaffe����Ϊ4mg/(kg��d)��������ļ�����Ŀǰ������A�Ƽ��Ŀ�ʼ������2.5��3.5mg/(kg��d)�������η��ã������5mg/(kg��d)��������A��ЧҲ��Խ�����һ��4��8����Ч����12���Ժ�ɴﵽ�����Ч��ʹ��ʱ���Դ�2.5mg/(kg��d)��ʼ��ÿ4��8������0.5mg/(kg��d)����������Ч���ȶ������ÿ4��8�ܼ���0.5mg/(kg��d)��ֱ������С�ļ���ά�֡���ҩ4��6���������û���ٴ�Ч����Ӧ��ͣҩ�����ϼ��͵Ļ�����1��1���������¼��͵��������ӣ�Ӧ�����ܳ��ֵĶ������á�
Landewe���е��ٴ����������������A��
����ֱ�����24��ʱ��Ч�൱����1�������A�������Ч�����Ա�
�����Ҫ�á����ڻ�����A����IL-2����������Tϸ�����ԣ����װ���������IL-1������ϸ���;���ϸ�����������Ǿ���Эͬ���ã���������ҩ����ʹ��Ҳ�Ǻ����ġ��о���������������A�ͼװ���������ʹ�����ڼװ����ʵ���ʹ�ã������ڶԼװ����ʷ�Ӧ���õĻ�����Ҳ������һ������Ч��������ҩʱ������A�ļ���ҲС�ڵ�����ҩʱ�ļ�����Ŀǰ���ٴ�����������ʾ���ϻ�����A�����ƿ�����������RA��ȡ��һ����Ч�������ڵ��ٴ��۲����ڽ��С�
������A�ĸ�������ͻ�����������ԣ��������н��ܴ�ҩ���ƵIJ��˶������Ѫ��������������Ϊ�����ԣ��ڻ�����A������ͣҩ��ɻָ����������ֵ��ٴ��۲춼���֣��ڿ�ʼ���Ƶ�2��3�����ھͻ���ּ��������������Ժ���Ա���12���µ��ȶ�ˮƽ��Ҳ���о��������������Ƶĵ�1�꼡��ˮƽ���Ա����ȶ���һ���ֻ����Ժ�����ˮƽ����������������ֵ��30%�����Ҽ�ʹ��ҩ�������Ҳ���ܸ��ƣ������ò�ͣҩ��һ�����ֲ�����Ļ�����A�յ�����������һ�����ص����⡣�������Ļ����в�ʮ����������ܰ�������Ѫ��������Ѫ˨�غ���Ƥ�ص����ӣ�����Ѫ�ܵ�ǰ�����صļ����Լ�Ѫ�������Եĸı䡣���Ի�����A�յ�����������������֯ѧ�ı��Ǿ����Լ�����ά����С��ή����С�������쳣��Forre��Ϊ������A��������7.5mg/(kg��d)ʱ���Ը��仼�ߡ������ಡʷ����������������ж��Ե�ҩ��ʱ��������ʹ������Σ�������ߣ���˻�����A�ļ���Ӧ������5mg/(kg��d)����Ѫ�弡��ˮƽ����50%����ʱӦ�õ���ҩ�������
������A�����������û��и�Ѫѹ�������ʴ�Լ��20%��������ʹ�ý�ѹҩһ�㶼���Կ��ơ�θ������ӦҲ�Ƚ��ձ飬��һ�㶼���ᣬ��������ʱ�Եģ����в���Ϊ�˶�ͣҩ�������������ж�ë�����������������Ƥ���о��쳣���鷿ѹʹ����Ѫ֢����þѪ֢��Ѫ�������ߵȡ�
���ڻ�����A�ĸ����ýϴ�����������RA�����û��������顣������A���ϼװ����ʵ������Ѿ���ʾ�����õ�Ч����������1���ڵİ�ȫ�Զ����Խ��ܣ�������������Ϊ����DMARD��Ӧ���ѻ�����ʱ�������������Ϊ���Ƽװ����ʷ�Ӧ����RA����������ҩ��֮һ��ʹ�ø�ҩ��ʱҪС�ģ����Բο���31��ָ�ϡ�
(8)���٣�����Ϊ��ì��ֲ���ȫ�꣬��������ľ���ϳ��ݺͺ�ҩ�ȣ��Ժ���ζ�࣬�д���Ƥ�ж��������������ʪ�ؽ������н�30�����ʷ������20����70������ϲ������ٺϼ�����RA 80��������Ч��95%�����ϲ�������������Ҳȡ��������Ч�������˷�ҩ3��5�����ʹ���ɼ��ᣬ������ʧ���������������ƹ��ܡ����ٵ������Ƽ�����ա�
����������ȡ�����Ƭ��������ǽ���������RA����һ����Ч��������Э��ҽԺ�������˫ä�������鷢�֣���������(���ٶ���)60mg/d����3���£����ٴ���ʵ����ָ��ȶ����������ԵĽ�������������RA�Ļ���Ŀǰ��Ȼ��̽���У����Ϸ������������ٿ������Ƶ���ϸ������IgM(����IgM RF)���ٴ��۲���������ٶ���Һ��ϸ�����߶������á�
�������ٵ��Ƽ��ڶ࣬�������÷�Ҳ��ͳһ�����Ͼ����ٴ��۲췢�֣�ʹ����������ÿ��60mg��30mg�ڴ��ٴ���ʵ����ָ��ĸĽ�����𣬲���ÿ�����30mg����ʱ���ظ����õı����������١���ѧ����Ϊ���٣��������Ը��Ʋ��˵Ĺؽ�֢״������Ϊ��Ҫ�����ڼ��Ի�ڣ����������ٻ���Ƥ�ʼ��ص�ʹ�á�Ŀǰ��Ϊ������Ч�죬ƽ��7��(1��15��)��Ч��������Ч�϶���
���ٵij����������и�к��Ƥ����ס�ɫ�س��š��ѷ���Ƥ���Ĥ����ϸ����ѪС�彵�͡�����ֳϵͳ��Ӱ��ȡ�����ֳϵͳ�⣬����������һ�㶼�ǿ�������������ͣҩ����֢���ƺɻָ������ٶ���ֳϵͳ��Ӱ����Ҫ�ر�ע�⡣�����ڸ�Ů��ҩһ��2��3���º�����¾����ң����ð����Լ52%�Ļ��߳��ֱվ���ͣҩ���¾��ָ���������Լռ70%�������40���ߣ���ʹ���ڷ�ҩ��ɵ��±վ���ͣҩ�������������ḾŮ��ҩʱ��ϳ�Ҳ����ȫ�վ�����ҩʱ��3�����ϼ�ʹͣҩҲ�ѻָ����ҿɰ����������˺�������������١�����������1��32��Ů�ԣ���������6�꣬����ʬ�췢���ӹ�����С���������ѳ�����ή�����ѳ������������������ʶԶ�ͯ��δ��Ů�Ժ�ϣ�������������ڸ�ŮҪ���ñ�ҩ�������ԣ�С�������پͿ�ʹ�������ɼ��٣���������������Ի�����Ҫ���ô�ҩ��
�������ٶ�RA������Ч�������ұ�����һ�������жϵı�Ҳ����ȫһ������˽�����Խ��бȽϡ������ܷ�ı�ǹؽ���ʴ�Ľ������ޱ�������Զ����ЧҲ��Ҫ��һ���۲졣Ŀǰ��Ϊ���٣�ȷʵ����һ���Ŀ��������������ã���������RA�Ľ�����ЧҲ�ȽϿ϶������ǻ����൱����������������ʻ�Ҫ���д��ڲ��������˫ä�������ٴ����飬�Խ�һ���۲�Զ����Ч�Ϳ��ܴ��������⡣����ѧ���о����֣���������RA����Ч�����Ͷ�����Ӧ��������������ѽ�ֹʹ�������������ֳϵͳ�ĸ����÷ֿ��������ѡ���˵�ʱ����Ҫ�������ء�
6.��Ƥ�ʼ��� ��ĿǰΪֹ����û�з��������κ�ҩ���������Ƥ�ʼ���(glucocorticoid)һ��Ѹ�ٶ���Ч�ؿ��ƻ�Ĥ�ͻ������ʪ�ؽ���֢״��������Ƥ�ʼ�����RA��ʹ�õľ����Ѿ�������50�����ң�Ŀǰ����������һЩ���顣�о���Ƥ�ʼ�����RA��Ӧ�õ���ʷ˵������һ�����Լ��������ƽ�����з����Ǻܸ��ӵġ�
(1)ȫ��Ӧ�ã�
����Ƥ�ʼ��ص�ҩ���ص㣺��Ƥ�ʼ���ͨ��������������ǿ��Ŀ������á��о���������Ƥ�ʼ��ض����ߵ��ڵ������ߵ���ϸ���������ã��������������������������Խ��ʵIJ��������á���������ϸ���ľۼ�����������ϸ���ļ���ȡ�ͨ������£���Ƥ�ʼ��ض�ϸ�����ߵ�����ǿ�ڶ���Һ���ߵ����ơ��ֽ���Ƥ�ʼ��ؿ��Ŀ��ܻ��Ƹ�������(��32��33)��


��С������Ƥ�ʼ�����RA�����е�Ӧ�ã���20����50�����Ӣ��ҽѧ�о�����ίԱ��(Medical Research Council)��Naffield����Ὺչ��һЩ�ٴ�����۲���Ƥ�ʼ�����RA�е���Ч�����������ʹ�ð�˾ƥ�ֺ��൱��ÿ��16mg������(prednisone)����Ƥ�ʼ��ؽ��бȽϣ��۲췢����������Ч�������Բ��졣��2������ͬ�����ְ�˾ƥ������Ƥ�ʼ���������RAʱ�ٴ�Ч��û�����Բ��죬������Ƥ�ʼ��������з�ֹ�ǹؽ���ʴ�����ƣ�������һ����������ͳ��ѧ���졣�˺�ʪ��ѧ��ӣ������������ٴ��۲�Ľ������Ϊ��Ƥ�ʼ�����Ȼ���кܺõĿ������ã����Dz��ܻ���ǹؽ��ƻ��Ľ��̡���3���ٴ��۲���Ȼ�ǽ���Ƥ�ʼ����밢˾ƥ�ֽ��бȽϣ�����3����÷�����Ƥ�ʼ������ٴ�֢״�������������ڰ�˾ƥ�֣�������Ƥ�ʼ������Ƶ�RA������ؽڲ����չ���ٶ�Ҫ�������ڰ�˾ƥ���顣���ǵ���Ƥ�ʼ��س���ʹ���������ĸ����ã���ʪ��ѧ������Ȼ�������б���̬�ȡ�Weiss��1989��������������ǰ�ٴ��۲�����ݣ����С����ʹ����Ƥ�ʼ��صĹ۵㽥�����������ǵ�ע�⡣1995�꣬Kirwan�Ⱥؽ����ʪ������ίԱ��С������Ƥ�ʼ����о���(Arthritis and
Rheumatism Council Low Dose Glucotorticoid Study Group)��չ��һ�������ٴ����飬�۲�С������Ƥ�ʼ��ضԹǹؽڲ����Ӱ�졣�о������еIJ��˶�ʹ������DMARDsҩ����DZ�����ֳ����飬һ�����7.5mg/d������������һ����ð�ο��������2�����ã����о�����ʱ���ֺ�����Ƥ�ʼ����ڷ�ֹ�ǹؽ��ƻ��Ľ�չ����Ҫ�������ڰ�ο���顣Boers��Wassenberg���˸��Խ��е��ٴ��۲�Ҳ������Ƥ�ʼ��ضԹǹؽ��ƻ����������ı������á�
��Ƥ�ʼ��صĸ������Ѿ������dz���˽⣬���ǵķ������������ʹ�õļ�����ʱ���йء���Ƥ�ʼ��ز����ĸ����ð������漸�����棺����(��������Ӧ�����ӶԸ�Ⱦ������)���ڷ��ںʹ�л(������-����-���������ܵ����ơ��������½�����֬Ѫ֢���ͼغͼ��ж������ٹ����½����˿����������½����������ӡ�����ƽ�⡢���ļ���)����Ѫ��(Һ����������Ѫѹ����������Ӳ��)��θ����(�����ס�����)���������(�������ɡ�ȱѪ�Ի���������)��Ƥ��(���ơ���ë��Ƥ���������ӡ����ߡ��)����(�����ϡ������)������(�����ı䡢ʧ�ߡ�����������������)�ȡ��������ɼ���Ϊ7.5mg/d�����ʱ�����ϴֵĸ����ú��ٷ�����������Щ���������������ӡ���Ƥ��֢״���������γɡ��������½�������ʧ���Ժܿ췢����
�����е��о������ʾС������Ƥ�ʼ��������ڼ���RA�ǹؽ��ƻ��Ľ�չ������������Ƥ�ʼ��صĸ����ã������÷���δ������ѧ�߽��ܡ������ڹ۲�С������Ƥ�ʼ��ص��ٴ������У����ʱ��������4�꣬���ڸ���ʱ��С������Ƥ�ʼ����������ķ���/Ч���(risk effective ratio)��Σ�������ȷ�𰸡����⣬�ڱ����ǹؽڷ��棬С������Ƥ�ʼ����������ķ���/Ч�����DMARDs�������ķ���/Ч��ȶ����������ӣ�Ҳû�п϶��Ĵ���ˣ�����Ҫ����ʱ��������ٴ��۲죬�Խ�һ���о���Ƥ�ʼ���������С����ʹ����RA�����еĵ�λ��Ŀǰ�Ƚ���ͬ�Ŀ�����RA��ʹ����Ƥ�ʼ��ص�����У�A.����в�����Ĺؽ�������(���磬���ʪѪ���ס����ʪ����)�����ƣ�һ��ʹ���еȻ�������B.����̨��������Ϊ��������(bridging)���ÿ��ƻ�Ĥ�ף��Եȴ�DMARDs��Ч��C.����RA���Է���������������ڼ���С���������Կ��ƻ�Ĥ�ס�
С������Ƥ�ʼ���(�����ɣ�10mg/d)�Ի�����л��RA���˵�֢״���Ѿ��dz���Ч��һ���ڸ�ҩ��ļ����ڹؽ���֢״�Ϳ��Ժܿ컺�⣬���ֲ�����ͣҩ��֢״�ܿ�Ϳ��Ը��������ٲ��ֲ��˼�ʹ��ʹ���㹻��DMARDs����Ȼ��Ҫ��Ƥ�ʼ����Կ��ƹؽ���֢״���Ӷ���Ҫ������������Ƥ�ʼ��ء����ⲿ�ֲ��ˣ���Ƥ�ʼ�������Ӧ��������С������ܹ�ʹ�������ɡ�10mg/d���Ի���RA���Է���ʱ��֢״���ԣ�һ����÷��������������7.5mg/d������ٷ���֢״�������Ը�Ϊ����7.5mg�������ܣ�Ȼ��ÿ3���7.5mg�������ܣ�������ͣҩ��������ҩ�ߵ�ͣҩ����Ҳ�����˽��С�
������С��������Ƥ�ʼ��س���ʹ�ã�Ҳ������ȫ����ijЩ���ظ����õķ�����������ǰӦ������ϸ���Ϳ��ܲ����ĺ����ȡ�û��ߵij�����⡣�����ƹ����У�Ҳ��Ҫ���ܼ���Ե�����ҩ��������Ƥ�ʼ���ʹ�ò������������صĺ����Pincus��Corbett��ѧ��ָ������������˵ʹ����Ƥ�ʼ��ص�RA�������������ӡ������ھ����Բ��˳���ʹ����Ƥ�ʼ���֮ǰҪ�������ؿ��ǡ�
(2)�ֲ���ҩ�����ڻ�Ĥ��֢״���ء����۹ؽ��١�ȫ�������н��ɵIJ��ˣ����йؽ�ǻ��ע����Ƥ�ʼ��أ��Ի������۹ؽڵ���ʹ�����ͣ����ƻ�Ĥ��֢״�����ƹؽڹ��ܡ�McCarty�ùؽ���ע����Ƥ�ʼ��ؼ�С�а�̶�3�ܣ�ÿ���ɿ�С�а壬�ʵ��������������Ĺؽ������٣������ֹؽ���ע�䲻�ܸı䲡���չ��ֻ��һ�ָ������ơ�
�ؽ�ǻ��ע��ҩ���Ч�����˺ؽڲ�λ��ͬ���졣��������˵Ļ�Ĥ���ܵõ��ϺõĿ��ơ���RA���̵����ڶ������������صĹؽڽ��йؽ���ע�䣬�������Բ���ȫ�����洦��ע��������ݹؽڴ�С��������һ��Ϊ10��30mg��������ʪ��ѧ������IJο�����Ϊ���ֺ����С�ؽڣ���������2.5��15mg����Һ����Ӧ��ҩ��еȴ�С�Ĺؽ��������ؽڣ���������10��20mg��ϥ����.��ؽڣ���������20��50mg���Źؽڣ���������25��50mg��һ������£�ͬһ���ؽ���3������ֻ��ע��1�Σ������Ҫ�ظ�ע��Ĵ����������Ҫע�����ؽڣ�˵����Ҫ����������Ƽƻ�������Ҫǿ�����ǣ��ڹؽ�ǻ��ע����Ƥ�ʼ���֮ǰ�������ų�����ԭ������Ĺؽ���֢��
7.�������� ���ʪ�ؽ����������߽鵼���������Լ��������ص��ǻ�Ĥϸ������ֳ����֢�������ڽ��ؽ���֯���ƻ�����ȥ��ʮ������ʪ�ؽ��������Ƶ��о���ǰ����һ�����ڷ��������о��Ľ�չ���������ʪ�ؽ��ķ���Ҳ��֮�õ���չ�����������ڵ�ǰ���ŵ������Ƽ����棬��ν����δ���������֢��Ӧ�ĸ�������������������Ƽ����34��ʾ��
(1)Tϸ����Ϊ���ư���Ŀǰ���еĹ۵���Ϊ��RA���ɿ�ԭ�����Tϸ���鵼��Tϸ������Ĥ����һϵ�е����Է�Ӧ����
������Ѫ�ܺͻ�Ĥϸ����ֳ�Լ����Ǻǵ��ƻ���Ҳ����˵��Tϸ����RA�쳣��Һ��ϸ�����ߵ������ʹٽ�����������Ҫ�����ã���֤��Ϊ��RA��Ĥ�µĴ����ϸ������T�ܰ�ϸ����ͨ������T�ܰ�ϸ���Ĺ���(�����ص���������ȫ�ܰͽ����䡢�ܰ�ϸ����
Ѫ����ȡ��)���Ը���RA���ٴ�֢״����ˣ���Tϸ��Ϊ���������Ŀǰ�о���Ҳ�Ƚ϶࣬����ֱ������ܡ�
��CD4��ԭ��CD4��Ϊλ��Tϸ������ķ��ӣ��ǿ�ԭ������Tϸ������(TCR)�ĸ������壬��Tϸ���ļ���������������Լ���֢��Ӧ���յ�����������Ҫ�����á�ʹ�ÿ�CD4����¡�����������������Լ����ǻ���������Ӧ��Tϸ�������߷�Ӧ�б���ԭ���ϴ̼��Ŀ��ǡ���CD4����¡�������ͨ������;��������ϵͳ���������ã�
A.ͨ��ֱ��ɱ��(����鵼���յ�����)��Խ���˿���ϸ�������(�����Fc����鵼�Ļ���)���ƻ�CD4 Tϸ����
B.�����ڿ����ϸ�������á�
C.ͨ������CD4
Tϸ���뿹ԭ�ݳ�ϸ��(
APC)֮��ķ�Ӧ���Ӷ����������ڢ�����֯�����Ը������Tϸ����Ӧ��
D.��CD4 ϸ�����������źš�
E.�������Tϸ��תΪ��Ϣ״̬��
F.�յ���Th1ģʽ��Th2ģʽת����
���Ϳ�CD4����¡��������������������RA����Ч���������������Ŀ�ԭ�ԣ�Ӧ���ܵ����ƣ��ڴ˺�������У����Ϳ���ͱ�Ƕ���ͺ����Ϳ�����ȡ����Ƕ���Ϳ����������ĺ㶨�������Ϳ���Ŀɱ����ں϶��ɣ��ȵ��������Ϳ��������ԭ��ҪС��Ϊ�˽�һ�����ٿ��������ԭ�ԣ�����Ŀ������ʹ�������Ϳ���Ļ���������(CDR)�����߶ȿɱ������֡�
ѭ���п�CD4����¡�����ˮƽȡ����ע��ļ�����Ƶ�ʡ�����Ƕ���Ϳ�����˵��ע���������10mgѪ���вſ��ܼ����ǽ���Կ��壻��20mg����ע���Ѫ��Ũ�ȷ�ֵ�ɴ�1��2mg/L����24h�ⲻ����������ע��10mg����CD4����¡���壬����ѭ���е�CD4 ϸ�������������ϣ����ؽ��ڵ�CD4 Tϸ���뿹���ϵú��٣�ֻ��ʹ��50mg��������5��ע��ؽڻ�ĤҺ�е�CD4 Tϸ���Ż�϶���뿹���ϡ��������ڵĿ���������Ե�����֢��λ�ۼ�������֮����CD4 Tϸ���϶����֯��Ҳ���н϶�Ŀ��塣
����Է�������(non-depleting)��CD4����¡������ٴ��о����֣���������73%�IJ��˿ɴﵽACR20����32%�IJ��˲������Ը���50%������Ѫ�ͻ�ĤҺ��CD4 ϸ���뿹���ϵı������ٴ���Ӧ��ء��Բ��ֲ�������ǰ��Ļ�Ĥ��췢�֣����ƺ�ĤҺ�������������Ӻ�IL-6ˮƽ��ͣ�ͬʱTϸ����Bϸ��������ϸ����𤸽���ӵı���Ҳ�½�����Щ��ʾ��CD4����¡��������ͨ������ϸ�����Ӷ�𤸽���ӵ��ϵ���������֢��Ӧ��
��CD4����¡����ļ�����10��700mg/��ʱҲ���������صĶ�����Ӧ�����Ƶ���Ҫ�������Ƿ��ȡ�ͷʹ��ż����Ѫ������ѧ�ϰ���������Ӧ����ʹ�����Ϳ���Ҳ���ټ��������ܰ�ϸ�����ٿ��ܻᷢ��������ʱ�������������û�б�����Ⱦ���ܰ������������ӡ�
��һ���������Կ�CD4����¡����OKTcdr4a��Ч���Ѿ���������RA�������ϵõ��˹۲졣���ֿ�CD4�����ǽ����Ϳ�CD4(OKT4A)����¡�����CDR������Ƕ����IgG4/kappa�����Ŀɱ�������һ��2�ڰ�ο�����������У�36��������RA��
�˲��������顣���ܴ����(450mg/��)��CD4����¡����(OKTcdr4a)�IJ������ƺ�õ��ٴ����⣬��ʾ����¡�������֢���������á�C��Ӧ����ˮƽ�����ƺ�Ҳ�õ����͡�OKTcdr4a��������CD4
Tϸ�������ģ�CD4����ı��Ͷ������ڿ���ļ�����
�������Կ�CD4����¡�������Щ�϶��Ľ����ʹ�˶Դ����Ƽ��Ľ�һ���о���Ŀǰ���������������Ŀ������ڽ����ٴ����顣��������������ٴ���Ӧ���������Ƴ�����ʱ��ͼ����������ٴ�����Ŀ�չ����ʹ�����Ʒ����ĺ����ԺͰ�ȫ�Եõ���һ������������CD4����¡�����������Ƽ�������Ӧ��Ҳ��ֵ�ý�һ���о������⡣
����Tϸ��Ϊ������������壺�������Tϸ���ķ�����������CD52����CD5����IL-2����Ϳ�Tϸ�����濹ԭ�Ŀ��塣CD52��һ�ֶ��ģ�λ�����е��ܰ�ϸ��(B��T�ܰ�ϸ��)��һЩ����ϸ�����档CAMPATH-1H��һ������Ŀ�CD52����¡���壬����Ƥ��ע�����ʹ�á���һЩ�ٴ������У����ֲ��˵õ��������ٴ����ƣ���������Ѫ�ܰ�ϸ��(��Ҫ��CD4 �ܰ�ϸ��)�ļ��ٳ���ʱ��ܳ�����������Ѫ�ܰ�ϸ���������٣�һЩ���˲���Ļ����Ȼ��ǿ�����Ҵ��йؽ��û��IJ����п��Է��֣���Ĥ��֯����Ȼ���д�����CD4 T�ܰ�ϸ�������������û��������ȡ�Ƥ��ͺ�ս��ĿǰCAMPATH-1H�Ѿ����ٱ�����RA���ơ�
CD5������λ�����е�Tϸ���Ͳ���Bϸ�����棬���ܶ�Tϸ������鵼���źŴ������Ե������á���һЩ�����Ե������У���CD5����¡�����ʹ�û���������Tϸ����Ŀ�ļ��٣�����Tϸ���Կ�ԭ�ͷ����ص���ֳ��ӦҲ�ή�͡�����������һ�������鲢û��֤ʵ��CD5����¡���������������ٴ�Ч�������Ŀǰ�����Ƽ�Ҳ���ٱ�ʹ�á�
��Tϸ�������һЩ�ض��Ŀ�ԭ���������Ե�IL-2����(CD25��IL-2R)���������Щ��ԭ�ھ�Ϣ��Tϸ���ϲ������ڡ��ܶ�������������(����RA)�������Tϸ���������ӡ����IL-2R�����ƿ���ѡ���Եؼ��ٻ������߷�Ӧ�������ž�ϢTϸ����Ŀǰ�Ѿ������������IL-2�����붾��(
����ٵ�������)�ĸ�����Ϳ�IL-2R����¡����(��CD25)��DAB486IL-2��DAB389IL-2����IL-2R������ϸ�����أ�����ѡ���Ե���IL-2R��ϣ���������鵼�±�Tϸ�����̣����̵�ϸ�����ؽ�����ϸ�����������������е�һϵ���ٴ����鲢�����˹��裬ֻ��С���ֲ��˲�����һ���ķ�Ӧ��
����Tϸ������Ϊ����Tϸ��ͨ������������(TCR)���Ͽ�ԭ�ݳ�ϸ���ӹ��͵ݳʵĿ�ԭ��Tϸ���������������׳����壬��Tϸ��������Ǧ�/��TCR�������Ĥ��������Ӧ��Tϸ��ֻ����һ�����С��Χ��TCR����ѡ����������Щ�ܰ�ϸ��������ʧ��Ӧ�ÿ��Լ��Ს�顣һЩ�о���������������RA��ĤҺ����Ĥ��֯������Ѫ�е�Tϸ���������С��Χ��TCR V����V�»���Ƭ�Σ����ڲ�ͬ������仯��Χ�ϴ�ͬʱҲ��һЩ����֤��Tϸ��Ϊ���¡�������Щ�о��IJ�������кܶ�ԭ���������IJ�ͬ�Ρ�ȡ�IJ�λ�IJ�ͬ���о������IJ�ͬ�ȡ���������Ĥ��Tϸ��Ⱥ��ΪRA���ܰ�ϸ�����ص�Ҳ������������⣬��Ϊ����ֻ��һ����Tϸ�����������Tϸ���������ڽ��е����߷�Ӧ�Dz���Ҫ�ġ�IL-2����(CD25)�Ǽ���Tϸ���ı�ǣ�RA��ĤTϸ���д�Լ��10%��15%����˱�ǡ�����Щϸ�����о�������TCRΪ����¡��������Ҫ��V��17��V��14��V��3��
ʹ�ü����IJ�ԭ�������������Ƴ��������Ƹ�Ⱦ�Լ�������Ϊ����֪��ʹ��Tϸ����������Tϸ���鵼���������������ǻ��������ļ�˵��������������Դ�Կ�ԭ�����Tϸ������������˼����Ĺ��̣����ǵ�TCR�ɱ��������ؾ�����Խ�С�ķ�Χ���������������������Ķ���ģ�͵��о�Ҳ�����²�Tϸ��ȷʵ�������С��Χ��TCR����Ƭ�Ρ�
��Կ�ԭ������Tϸ���������ڶ���ģ�͵�Ӧ�ã����ֿ��Է�ֹ�ؽ��ķ���������
��ԭ�Ϳ�ԭ�յ��Ĺؽ��ס������������������Լ����д�����²�Tϸ�������V�»���ɷֱȽϾ��ޣ����������ЩTϸ�����е����ƿ��Լ����²�ϸ�������ö��������������ơ�TCR��������յ�������Ӧ��Tϸ����������ܣ��������ǵļ��١����ƺ�ʧ���Щ��������ٴ�Ч���Ļ��ƱȽϸ��ӣ�������ʹ�õĵ������йأ��������յ�������TCR���壬��Ϊ�еĶ���ģ���в�δ��ѭ�����ϵĿ�TCR���壬���²�V��
��Ⱥϸ��Ҳû�м��١�
���������������V��17��CDR2�ṹ��������ġ�15���������жȵ��ضȻ��RA�IJ�
�˲��������飬���������10��g��30��g��100��g��300��g����48�ܵĹ۲����п��Լ����ٴ�֢״�ĸ��ƶ�û�м��������á�����2���ٴ�����ʹ�õ���V��17��V��14��V��3������ĸ������99����
�˲��������飬������90��g��300��g���ֱ���0��4��8��20��ʱ��������ע���۲���Ϊ32�ܣ��˼�û�в�����Ϊ�����ö��˳���90��g��������56%�IJ����ڵ�3��ע���ﵽACR20��50%�ڵ�4��ע���ﵽACR20����������Ϊ19%��300��g������ֱ�Ϊ25%��37%������������������ܣ����кܶ�����δ����������糤���ظ�ע�������һϵ�����⡣�ٴ�Ӧ�û���Ҫ�����ģ���о������顣
�ܸ����̼����ӣ���һЩ����ģ���аѸ����̼�����(��������)��Ϊ���������Լ����������о�����Ŀǰ��Щ������CD40��CD40����(CD40L��Ҳ��CD154��gp39)��B7��CD28(B7����)��CD154���������������Ӽ��嵰�ף���һ�֢���ϸ�����浰�ף��ɼ����Tϸ�����CD40��һ��ת���źŵ����壬��������һϵ�е����ߺ����Է�Ӧ���������ڼ����Tϸ����λ��Bϸ���ͼ���ľ���ϸ���ϡ�
����ģ����ʹ�ÿ�CD154��CD40���嶼��������CD40/CD154���Ӧ�����Ҷ�ʱ���Ӧ�þͿ��Բ����ϳ�ʱ����Һ���߷�Ӧ�����ơ������֤����ʾ������CD40��������RA��Ĥ�������������ӵIJ��������ٿ��Բ���RF��Bϸ����Ŀǰʹ������Ŀ�CD40����¡������ٴ��������ڽ��С�
����Tϸ����Ҫ����һ���ź���
APC�ϵ�B7��ط�����Tϸ���ϵ�ϸ�������ܰ�ϸ����ؿ�¡4(CTLA4-Ig)��CTLA4���ӵ�����á�CD28��һ����Ҫ�ĸ����̼����ӣ��ɾ�Ϣ��Tϸ�����B7���������壬λ�ڼ����Bϸ���ϡ�CTLA4(��CD28ͬԴ)Ҳ��һЩ�����Tϸ���ϱ��B7��������������CD28��20��100������CTLA4�İ��ⲿ������IgG2a��Fc�����ں��γɵ��ںϵ���(CTLA4-Ig)ע�䵽�������ڿ��Է�ֹB7��CD28�Ľ�ϣ���ֹ
��ԭ�յ��Ĺؽ��IJ������ڶ���м�����˵�1���ٴ������У�CTLA4-Ig���ƿ��Դ���50%���ϵ��ٴ����ơ�Ŀǰ�����Ƽ�����RA�����н���������
����Ҫ��֯�����Ը�����������
APC��������Tϸ���ļ������ͨ�����
APC�����Tϸ��ʶ��ṹ������ֹ��������Ҫ��֯�����Ը�����(MHC)���������Ķ���ֱ����Լ�������Ԣ���MHC��λ�������ĵ���¡�����Ѿ��������������Ķ���ģ���н����˲��ԣ����������Ʒ�Ӧ�Ļ��ƻ���ʮ�����������ЧӦ���ܹ��ڢ���MHC�ĵ�����ϣ���Ϊ���Ʒ�ӦҪ�ڿ���ע��ܳ�ʱ���ų��֡�����̥����֯����ȡ�Ķ��¡����ע�䵽RA�������ϣ���Լ50%�IJ��˵õ��ٴ����ơ�ʹ����Ŀ�HLA-DR/DP����������������յ�����Դ�Կ�MHC���壬�������Ʒ��������������ٴ����ƿ��Գ�������6���¡������DR4/DR1����Ϊ����������RA����Լ1/4�IJ��˻�������塣��һ�ַ����ǹ���һ�ֵ����Ŀ��������Ӧ�Ģ���MHC��λ��������Ŀ�ԭ�ʵݶ��������Bϸ�������ַ���Ҳ����Ҫʶ��������ԭ��ͨ����ϼ�������Ԣ���MHC��λ����(��DR4)����RA�����о��С�
(2)ϸ�����ӵ������Ƽ���������������������鶼������ϸ��������RA�ķ���������������Ҫ�����á�������RA�йصĺܶ�ϸ�����ӵľ�ȷ���������о��У�Ŀǰ����IL-1��������������-����RA�ķ��������ŷdz���Ҫ�����ã����������ϸ�����ӳ�Ϊ�о�RA����������Ҫ��Ŀ�ꡣ������Щϸ�����ӵ��Ƽ��������ٿ�����ϸ���������壻��ϸ�����������������ۿ�ϸ�����ӵ���¡���壻������Fc�ṹ��ϸ�����ӻ������ϸ������������ں���ݶ�Ŀ��ϸ�����Ӿ��з��������õ�ϸ�����ӡ������ķ�����������ֹϸ�����ӵļӹ���ϳɵȡ�
�ٿ�������������-���Ƽ���������������-���ǵ�������ϵͳ�ڸ���ϸ������õ��ڶ�ϸ������֮һ�����ܺܶ�ϸ�������Բ���������������-��������֢��λ��Ҫ���ɾ���ϸ��(macrophage)��������������������1984�걻��¡���������Ƿ������������(cachectin)��ͬһ�ַ��ӣ����Һ��ܰͶ���(lymphotoxin��LT)�д�Լ30%ͬԴ������������������-����LT(��ʱ�౻����������������-��)�Ļ�����6��Ⱦɫ���Ͻ���������������������-����ǰ���Ǿ���26kd�Ŀ�Ĥ���ף�������������-��ת��ø�ɽ�����гɾ���17kd�Ŀ�����Ƭ�Σ���Ƭ��һ����ϸ��Ĥ�ͷžͿɾۼ���ͬԴ�����塣�����������ӿ�Ĥ���Ϳ�������ʽ���ɲ�������ѧЧӦ��������������-��������������ʽ��p55(������������R-I��CD120a)��p75(������������-��CD120b)�����Ƕ����а��ڡ�����Ϳ�Ĥ��������ṹ�ɱ�������������-��ת��ø���������γɿ��������������������壬��Ϊ������������-����Ȼ�������������������/������������R��Fas����/Fas��CD40����/CD40�ȶ���ͬһ����ij�Ա��
�����������Ӿ��кܶ����Ժ����߷�Ӧ���ԣ������������Է�Ӧ�����л��ڣ�������
A.��Ѫ��ϵͳ�����ã�a.ͨ������NF-��B�ϵ�𤸽�����������(ICAM-1��VCAM-1��E-selectin)��b.�̼�Ѫ�����ɣ�c.������Ƥϸ���Ĵ�������(�̼���֯�������ɡ��µ�Ѫ˨������)��
B.������/����ϸ�������ã�a.���ߵ���(�����ܰ�ϸ����������ϸ��)��b.�յ�����άϸ����ֳ��
C.�Է�Ӧ���ʵ����ã�a.�յ�ǰ���Խ��ʵĺϳ�(�磺IL-1��IL-6��GM-CSF)��b.�յ�ǰ�����������ӵĺϳ�(�磺RANTES��IL-8��MIP-1����MCP-1)��c.�յ��������Խ��ʣ�ǰ�����ء�����ϩ��ѪС�����ӡ�NO�����������ʵȣ�d.�յ�����Ǻ������ƻ��Ľ�������ø�ϳ�(�磺
��ԭø�������ܽ���)��
D.����ЧӦ��a.������ʹ��b.������ʣ�c.���ڷ��ȣ�d.ʹ���Ѹ�(���ƹ�ϸ������ӡ�����)��
��ʮ������о�������������������-���Dz������ʪ��Ĥ�ؼ���ϸ�����ӣ����ܵ�֤���ǣ�a.������������-����������Կ��Խ��Ͳ���RA�IJ������̣���������ϸ���ľۼ��ͼ����Ĥϸ������ֳ������Ǻ������ƻ���ϸ�����Ӻ�ø��Ũ�ȼ����Ե����ӣ�b.RA��Ĥ��֯��������������-����������������-�������ϵ���c.�����⣬��������������-����������IL-1������ǰ����ϸ�����ӵ��µ���d.���ֱ���������������-����ת����С�������ʴ�Թؽ��ף�����֯ѧ�ص���RA���ƣ�e.�ؽ��Ķ���ģ��֤ʵ����������������-�����ʿ��Լ��Ს��̶ȣ�f.��RA���п�������������-�����ƿ��Բ����Ϻõ��ٴ�Ч����
a.��������������-������¡���壺ĿǰFDA���Ŀ�������RA���ƵĿ�������������-������¡������Centocor��˾��infliximab(��Ʒ��
Remicade)������20����90����������������ȱ�������������RA���˵Ŀ�������������-������¡���塣infliximab��װ����ʺ��ÿɼ��ᵥ�üװ�������Ч�Ļ��RA���˵�֢״��2000��7�·�FDA����С���Ƽ�infliximab��������Ӧ֤Ϊ����RA���˵Ĺؽڽṹ��
b.infliximab��infliximab(
Remicade)����/��Ƕ���Ϳ�������������-������¡���壬����IgG1�ͣ�Ҳ������ѡ��������������������-���ĵ�һ���Ƽ���infliximab��75%�˺�25%��Ŀ�����ɣ���������������-������Ŀɱ�������IgG1�ĺ㶨���ںϹ��������Ŀ���(ͼ43)��������������Ժ�Ĥ����������������Ӧ���ϣ��������о�������ͨ������鵼�Ϳ�������ϸ���鵼��ϸ���������ܽ���������������Ӧ���ϸ����infliximab��˥��Ϊ8��9.5�죬ʹ��ʱ������ע������2h��infliximab���Բ�����������ЧӦ������ǰ����ϸ�����ӣ������ܰ�ϸ���ڹؽڲ�λ�ľۼ������ٻ�Ĥ��Ѫ�����ɡ�infliximab����Ѫ��IL-6��IL-1��ˮƽ���Ի�Ĥ���ķ������ֻ�Ĥ��֯����ϸ������IL-1��Ҳ���١�Ѫ��ͻ�Ĥ��֯�������������IL-8�͵���ϸ����������(MCP)-1��ˮƽ����ҩ������١�infliximabͬʱ���Լ��ٻ�Ĥ��֯��Ѫ��𤸽����E-selectin��ϸ����ϸ��𤸽����-1(ICAM-1)��Ѫ��ϸ��𤸽����-1(VCAM-1)�ı��Ѫ����E-selectin��ICAM-1Ҳ���١�����ϸ�����Ե���(MIP)-1����MIP-1�º͵��������������������������(Gro-��)�ڻ�Ĥ��֯��ˮƽû�з����仯���������������������������-������(p75��p55)�����ƺ�Ѹ�ٽ��ͣ����ܿ���ϸ������IL-10�����ӡ���Ƥ𤸽���Ӻ��������Ӷ�ϸ�������۹ؽڵľۼ���ؼ������ã���infliximab�����ǵ����ƿ�������������ϸ����CD3
Tϸ����Bϸ���;���ϸ���ڹؽڵľۼ���ͬʱ���ܰ�ϸ����CD4
��CD8
Tϸ��ˮƽ�������ƺ�ܿ�������infliximab���Լ���Ѫ����Ƥϸ���������ӵ�Ũ�ȣ��Ӷ����ٻ�Ĥ����Ѫ���γɡ�infliximab�����Լ���
Ѫ��NO�ϳ�ø��MMP-1(����
��ԭø)��MMP-3(�����ܽ���-1)������Щ����Ҳ����Ϊ����RA��֢���ƻ��Ĺ��̡�
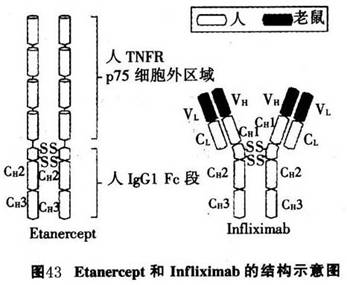
c.�����infliximab��Ϊ��һҩ����еĿ���������ٴ�ʵ�鷢�֣��ڸ�ҩ��24h�ڣ�����֢״����ij̶ȾͿ��Դﵽ60%��������ʹ�������ؽ����ͣ�2��4��Ч���ﵽ���infliximab��Ч���ʼ��������ԣ�1mg/kg�ļ���ʱ��44%�IJ��˴ﵽACR20��10mg/kg�ļ���ʱ��79%�IJ��˴ﵽACR20���м���Ч����1mg/kg��10mg/kgʱ�ֱ�Ϊ3�ܺ�8�ܡ���infliximab�ij�����Ч�Ĺ۲��������1mg/kg������һҩ�������£�������60%�IJ�����3�ܺ�ﵽACR20�����������ظ���ҩ������Ч������ά�֡���3mg/kg��10mg/kg������Ϊ��һҩ���Ч����ά������16�ܡ�1mg/kg��3mg/kg��10mg/kg�ֱ���װ���������ʹ��ʱ����ЧҲ����ά�֣������ں���������¾���14�ܵĸ�ҩ��ͣҩ����Ч�Կ���ά��12�ܡ��о���ʾ��С�������ظ�ע������յ������϶�Ŀ�infliximab���壬���ϴ�ļ�������װ����ʺ��õ�����¿���������١�������Щʹ���˼װ����� 15mg/kg��������Ӧ�������RA���ˣ�����infliximab����װ���������ʹ�ã������������ȡ�ýϺõ���Ч��ʱ���������ģ������ٴ��۲���ʾ��infliximab��ʹ�ÿ������������ؽ���ʴ�ؽ�ǻ��խ�Ľ��̣��������ָ�������Щ�ٴ�֢״�Ļ��Ⲣδ�ﵽACR20�IJ�������ɳ��֡���infliximab�ͼװ����ʺ���ʱ��50%�IJ������������˹ؽ��ƻ���ֹͣ�����ܲ����Ѿ��ܳ�����428���װ����ʲ����еIJ��˽��е�3���ٴ�����(ATTRACT����)��ʾinfliximab��װ���������ʹ�ÿ���ʹ��Щ���˻���������ٴ�Ч��������ֹ�ؽ��ƻ��Ľ�չ��2����淢����Ч���Գ���102�ܣ�����infliximab��������и�����Ч�����ơ���Щ����Ѿ���2000��11�¾��е�ACR��64������Ϲ�����
d.infliximab�ĸ����������¼������棺��Һ��Ӧ��С���ֲ����ڵ�ע��1��2h�ڷ�������Һ��Ӧ���������ȡ���ս��������ݡ������ķη�Ӧ(��ʹ����Ѫѹ����Ѫѹ�ͺ�������)�����صķ�Ӧ����������ݡ������ķ�֢״�ķ�����Ϊ0.5%����Щ��Ӧ�ڶ�֢������ֹͣ��ע����ɻ��⡣��Ⱦ�����ٴ������У�infliximab����26%�IJ��˷����˸�Ⱦ����ο����Ϊ16%�����������FDA������ҩ����г�����������ڴ�Լ6����ʹ��infliximab�IJ����У��������(��Ϊ�̷�)14������˹�ؾ���Ⱦ2�����������Ⱦ7�������Ϸ��ҳ����5�����������Ⱦ8����ͬ�������infliximab�Ƿ�ȴ�ͳ��DMARDs���Ӹ�Ⱦ�ķ�����û�о����ٴ�֤ʵ��������infliximab���壺�ظ�ʹ��infliximab���Բ�����infliximab���壬���ٴ������з����ʴ�Լ��11%���ϴ����(3mg/kg��10mg/kg)�����ϼװ�����ʹ�ñ�С����infliximab����ʹ��ʱ��������Ҫ�١���������/���Ǵ��ۺ������ڴ�����װ�����/infliximab����ʹ��ʱ��26%�IJ��˲����˿��˿��壬����������IgM����ο����ķ�������6%����Լ4%�IJ��˲����˿�ds-D
NA���塣�������IJ��˲�����������ϵͳ�Ժ���Ǵ����ٴ�֢״(���Ǵ��ۺ���)����û�в��������������ϵͳ����ͣ��infliximab�ͽ���ҩ�����ƺ�֢״���⡣��������/�ܰ���ֳ�Լ�������ʹ��infliximab�IJ�����Ҳ�в���ʵ�������ܰ�ϵͳ�����ı���������û��֤�ݱ���infliximab�����Ӷ��������ķ�����
e.FDA�����Ĺؽ�����ίԱ���������infliximab�ͼװ���������ʹ���Լ���RA���˵Ĺؽ��ƻ����÷�Ϊ������ע����ʼ3mg/kg���ڵ�1����2�͵�6��ʱ��ʹ��1�Σ�Ȼ��ÿ8��1�Ρ����л�Ը�Ⱦ�IJ��˲�Ӧʹ�ã�������ƹ����з�����Ⱦ��Ӧ���й۲졣Ŀǰinfliximab��RA���Ʋ����еĵ�λ�����ںͼװ���������ʹ�ã�����Ϊ��һҩ��ʹ�ú����������ߵ��ڼ�����ʹ�õļ�ֵ���д��ڽ�һ���о���
f.��������������-������¡������о����ƣ���ȫ����Ŀ�������������-������¡���壺D2E7��ͨ������D
NA������������ȫ����Ŀ�������������-������¡���塣���ֿ������һ������������IgG1������ͬ�Ľṹ����������������-�����нϸߺ�����������������к������������ϵ�������������-������ҩ��İ�˥����6��13.7�죬Ƥ��ע�������ע��ҩ���ٴ��۲췢�֣����������IJ��˿��ԴﵽACR20���ٴ�֢״�Ļ���������24h��1���ڷ�����1��2�ܺ���Ч�ﵽ����ڼ�������1mg/kgʱ������Ӧ�ﵽһ��ƽ̨��һ������£���Ѽ�����40mg������Ӧ��ȷ������ע�䷴Ӧ����Ⱦ���ܰ���ֳ�Լ����ķ����ʲ�δ�Ȱ�ο����ߡ��Ը�ҩ12���µĹ۲�Ҳ��ʾ�ؽڵ��ƻ��õ������ļ������������������á�
���Ҷ�����(-PEG)�����������������-��Ƭ�Σ�CDP870��һ���ø߷�������
���Ҷ������εĿ�������������-������¡����Ƭ�Σ����ε�Ŀ����Ϊ���ӳ������
Ѫ����˥�ڡ�ʹ�ü����ֱ�Ϊ1mg/kg��5mg/kg��20mg/kg��CDP870���ƵIJ�����8�ܺ�ﵽACR20�ı����ֱ�Ϊ25%��75%��75%������ο����Ϊ16.7%����һ����2�ں�3�ڵ��ٴ��������ڼƻ��С�
B.������������������-�����壺Ŀǰ���еĿ�����������������-��������Immunex/Wyeth-Ayerst��˾��
��������(��Ʒ��enbrel)��
������������һ�ֻ���DMARD��̫��Ч�����ض�RA���ˣ���������������������������RA���ӻ��ؽڽṹ��Ŀǰ���ȴ�����������RA��
a.
����������
��������(enbrel)�����û��̲����ķ��ӣ������Ϊ��������75kd(p75)������������R�İ��ⲿ�֣�������IgG1��Fc�������������߾���CH2��CH3�ṹ��ͽ�������
��������������������������͵������������ӽ�ϣ�������ʹ����ϵ�ϸ���ܽ⡣
��������ƽ����˥��Ϊ4.8��(4.1��12.5��)��ʹ��ʱƤ��ע�䣬25mgÿ��2�Ρ�
��һ���������ٴ��۲��з��֣�
����������ʹ�ÿ��Լ��ټ��ػ�װ����ʵ��������ٲ��ֲ�����������ֹͣ���ػ�װ����ʵ�ʹ�á�������ڼ䣬�����õķ���
����������������鲢û������������Щ����Ѿ���2000��11�¾��е�ACR��64������Ϲ�����
���������ĸ����������¼������棺ע�䲿λ�ķ�Ӧ����Լ��40%�IJ�����ע��IJ�λ������ȵ��жȵķ�Ӧ��ͨ��������3�ܺ���֡����ַ�Ӧ������ʱ��ƽ��Ϊ4��5�ܣ�����ҩ��ļ���ʹ�÷�Ӧ����ʧ��Ҳ�еIJ��˷�Ӧ������ʱ��Ƚϳ�����Ⱦ���۲����
���������Ͱ�ο�����и�Ⱦ�ķ����ʺ�Ⱦ������û�������IJ����
���������ͼװ����ʵıȽ��У����߷������ظ�Ⱦ�ļ��ʱ�ǰ�߸ߡ���FDA�Գ���2.5��������ʹ��
�����������5���µĵ����У�30�������淢�������صĸ�Ⱦ����������ŧ��Ѫ֢������6�������������еĴ�����������Ի��Ը�Ⱦ��֮ǰ���ڵĸ�Ⱦ�������������������Ⱦ�����ء����FDA�Դ�Լ8������ʹ��
���������IJ��˵ĵ�����ʾ����˸�Ⱦ1�������Ϸ��ҳ����2�����������Ⱦ11�����������Ⱦ108������ϵͳ���䣺������ʾʹ��
�����������ܻ��յ�����������ʲ��䣬������ϵͳ������������ʲ��䣬�����½������Ļ��Ķ��Ӳ���������������ȡ�����
���������������ʲ���Ĺ�ϵ����ȷ�������������������ʲ���IJ�����ʹ��
��������ʱӦ���Գ�ֵ�ע�⡣ѪҺϵͳ���еIJ���������������ȫѪϸ�����٣������ں�����������������Ƶ�ҩ������ʹ��ʱ��һ����ڿ�ʼ���Ƶ�2�ܺ�����һ���������ص���Ѫ�쳣Ӧ��ֹͣ
����������ʹ�á�������
�����������壺��16%�IJ��������ٷ��ֳ��ֹ�һ�η��к��Կ�
�����������壬���ֿ��������Ʒ�Ӧ��Ӧ֮��Ĺ�ϵ����ȷ������������/���Ǵ��ۺ�����ʹ��
���������IJ�����11%�����²����Ŀ��˿���(��ο����Ϊ5%)��15%�IJ����з��ֲ����˿�ds-D
NA����(��ο����Ϊ4%)��û�в��˲������Ǵ��ۺ����������������������ٴ����֡���������/�ܰ���ֳ�Լ�����ʵ�����ķ����ʺ���NIH��SEER����Ԥ��ֵ���ơ�û��֤�ݱ����ܰ����ķ�������
����������ʹ�ö����ӡ�
������ŷ���Ƽ��ڶԼװ����ʷ�Ӧ���ѵIJ����п��Ե���ʹ��
������������װ���������ʹ�ã��Ƽ��÷�Ϊ25mgƤ��ע��ÿ��2�Ρ�����DMARDs�����RA����Ч�кã�
���������������жȵ��ضȵ�RA��������¶��������ڶԼװ����ʷ�Ӧ���õIJ��ˡ�������RA�ĸ�Ϊ�������������ư�ʾ
�������������ڲ����е�Ӧ��ǰ�������൱������FDA����Ƽ�������RA��ʹ��
�����������ӻ��ؽ��Ľ�չ���Ʋ��˵�֢״����
�����������ϼװ�����Ŀǰ������RA�����л�û����Ϊ���η���������
�������������Ʋ����еĵ�λ��Ӧ�ý�һ�����������������һ�����ٴ��۲����
���������Ի���û�и����ã��������ܻ�������������̥�����и���������С��4���ͯ������RA�İ�ȫ�Ի���Ҫ������
����������Ӧ���ھ��л�Ը�Ⱦ�IJ��ˣ���������ƹ۲��з������صĸ�Ⱦ���³��ֵ���ϵͳ֢״����Ӧ��ͣ�á�
b.������������������-��������о����ƣ�lenercept����������55kd�Ĺ���������������R�İ��ⲿ�ֺ�����IgG1��Fc�������Ӷ��ɡ��ٴ��۲췢�ָ�ҩ��Ч�ͼװ��������ƣ�����Ӧ����ע�䷴Ӧ����ȵ��Ϻ�������Ⱦ����lenercept����IJ����Ƚ��ձ飬��������������Ч��Ӱ�����Ӧ���������˿���Ϳ�ds-D
NA����ı����ֱ�Ϊ13%��3%�����Ǵ��ۺ�����δ������������lenercept�������ڼװ����ʣ�����Ӧ��ǰ������������
���Ҷ������Ŀ����Ԣ���������������R��
���Ҷ�����������������Ԣ���������������R��Nĩ�ˣ��÷��ӵĶ�������ж������������Ӻܸߵ���������һ��ҩ���ȱ���ǿ�ԭ�Խ�ǿ���ظ���ҩ���������壬�Ӷ��ӿ�ҩ������������ҩ��İ�˥�ڡ��ڶ���ҩ���Ѿ������Ƴ�����С��ģ���ٴ������������100��g/kg��1000��g/kg�����������Զ��ܺã����Ի����ٴ�֢״���������˶�ҩ������˿��壬��û�м����ٴ�Ч�����Եĸı䡣����ҩ�������ԭ�ԡ���Ч�Ͱ�ȫ�����ڱ���һ�������С�����ģ����ʾ��ҩ����IL������������Ӧ�ò������ٴ�Ч�����á�
c.ʹ��������������-���������������ƣ�����������������-���������Ը���RA���˵�֢״�������������������ǹؽ��ƻ��Ľ�չ�����Dz�������ȫ��ֹ�����Ľ��̡�ʹ���ܹ���������������-��������Эͬ���õ�ҩ�����������Ч����Ϊ�װ����ʳ�������������������-���⣬������ϵͳ���ж������ã�Ŀǰ����������ʹ�üװ����ʺ�������������-���������������ܻ�������õ��ٴ�Ч����ATTRACT�ٴ��������õ���������ʾ��������ҩ����Խ�ԣ���Щ����Ѿ�������������������-��������CsA����CD4����¡���塢��IL-12�����IL-1��������������Ӧ��Ҳ�����о��С����ڴ�����ķ�ʪ��ѧ�Ҷ������ŶԳ��ε�RA������ѡ������������-��������ʹ�ÿ��������������Ƽ�֮ǰӦʹ�üװ�������ͼ���15mg/������3����(�������ڼװ����ʶ��Զ�����ʹ��)�������Ч���ѡ�ÿ��������������Ƽ�������Ϊֹ�������о������������������Ƶ��ٴ�������ѡ�ɵĶ����Dz��̽ϳ�������Ƚ��أ��Լװ�����Ч�����õ�RA���ˡ���Щ���˲���һ����ʹ�ÿ����������������Ƶ���Ѷ������ԶԿ��������������Ƽ�������RA����ʹ�õ��о��Ƿdz���Ҫ�ģ������о�����һ����ʾ��������������������RA�����еĵ�λ��
�ڿ�IL-1�Ƽ���
A.IL-1��������(IL-1Ra)��IL-1����������IL-1����IL-1�º�IL-1Ra������IL-1����IL-1�¶��Ǿ��л��Եķ��ӣ�����Ӱ��ܶ�ϸ���Ĺ��ܡ�IL-1Ra��IL-1����Ȼ��������Դ�RA��Ĥ��֯�ľ���ϸ���м���IL-1Ra������IL-1�����ϣ��Ӷ���ֹIL-1��IL-1����Ľ�ϣ�����IL-1Ra��IL-1����Ľ�ϲ�����ϸ���ڴ����źţ�Ҳ������������IL-1������һϵ�е����η�Ӧ�������⣬Ҫ�����ȫ���Ƶ�Ч����IL-1Ra��Ũ�ȱ�����IL-1��10����100�������������У������IL-1Ra(rIL-1Ra)������ֹ��IL-1�յ���һϵ�з�Ӧ��������Ĥϸ������PGE2������ϸ������
��ԭø�������ǵ��˱�Ͱ����Ͼ��Ǻϳɵ����ơ���IL-1Raȱ����С��ģ���У����Թ۲쵽������RA�����Թؽ��ı��֡�
�ٴ����������rIL-1Ra�밲ο���ȽϿ��Բ����������ٴ�Ч��(һ��������2�ܺ���)��Ѫ�������ķ�ӳ(ESR��CRP����)�����ҹؽڲ���Ľ���Ҳ��������������Ҫ�������˱�ļ�����ҩ������ѧ���֣�rIL-1Ra�İ�˥��Ϊ6h���������ö�Ϊ95%(Ƥ��ע��)������rIL-1Ra��ע����24h��ѭ��Ũ�Ƚ��ܿ��½����������������һ����ҪIL-1Ra��Ũ��ΪIL-l��10����100����������IL-1�Ļ��ԣ���ÿ���ҩ������ÿ�ܸ�ҩ���ٴ�����Ҳ֤������һ�㡣�����������30mg/d��75mg/d��150mg/d�Ĺ۲췢��150mg/d��Ч��Ҫ������������������һ���ֲ���������ǰ��ֱ����˻�Ĥ��죬������֣����ƺ���Ĥ��ľ���ϸ������Ĥ�µľ���ϸ�����ܰ�ϸ���������٣�ϸ��𤸽����Eѡ���ء�Ѫ��ϸ��𤸽����1(VCAM-1)��ϸ����𤸽����1(I-CAM-1)Ҳ�õ����µ���
��rIL-1Ra�ͼװ���������Ӧ�õ��ٴ����鷢�֣�����Щ�Լװ����ʵ���ʹ�÷�Ӧ���ѵIJ����У�rIL-1Ra���ϼװ����ʿ���ȡ���������Ч���������ٴ�֢״�����ڹؽ��ƻ��ĸ����Ͼ����ڼװ����ʶ��ã����������Ժܺá�����������rIL-1Ra����Ѽ�����1.0mg/(kg��d)��
Ŀǰ���۲쵽��rIL-1Ra�����ú��٣���Ҫ��ע�䲿λ�ķ�Ӧ����������62%(����������Ϊ175��)�����ڲ������ܶ��ж����Ƶ�ֻ��5%��������rIL-1Ra����DZ�ڵ��������Ƶ�ЧӦ�������ٴ��в�δ���۲쵽������rIL-1Ra�������������ܰ�ϸ������Դ�Է����ػ�ԭ����ֳ��Ӧ��Ҳ�����ư�ϸ���ķ�Ӧ�����鷢��rIL-1Ra����Ӱ������Կ�ԭ��ϸ������Һ���߷�Ӧ��rIL-1RaҲ�������Ӹ�Ⱦ���ܰ���ֳ�Լ�������������������Σ�ա�
һЩ�о����֣����������ܸ�ҩ��һ��ע�������Ч��Ҫ�á�ÿ��Ƥ��ע��ĸ�ҩ��ʽ�����ܴﵽ�����ѪҩŨ����ʹIL-1����õ��������к͡������ķ�չ�����ǽ�һ���Ľ���ҩ�����������ȡ����ѵ���Ч��
�й�rIL-1Ra�Ƽ�kineret(anakinra)���������ϱ�����kineret��װ����ʺ��õ�RA������42%�����ٴ�Ч�������װ����ʵ���ֻ��23%��Ч��kineret�Լ��ٹؽ��ƻ����ۻ���ЧӦ�����ּ�����kineret�����Թ۲쵽�ؽ���ʴ�����ؽ�ǻ��խ���������ơ�
B.������IL-1����(sIL-1Rs)��IL-1����IL-1��ͨ��ϸ��Ĥ�ϵ�IL-1���������ã�IL-1������2�֣��ֱ��Ǣ��ͺ͢��͡�IL-l�����IL-1�����ϲ���ת���κ��źţ����Ԣ������屻��Ϊ���ջ����塣����İ��ⲿ�ֱ������������γ��˿�����IL-1���塣���Ϳ�����IL-1������RA���˵Ļ�ĤҺ�пɼ�������������Զ�ؽ�������Դ�Ԣ��Ϳ�����IL-1������һ����Ȼ�����Ŀ������ӡ����������������ڵ�Ũ�Ⱥܵͣ����Բ����Բ����ٴ��Ͽɹ۲쵽�Ŀ������á�
��������������IL-l����(rhu sIL-1Rs)���������Եؽ��IL-1����ֹIL-1��ϸ�����������������ϣ��Ӷ������������ڿ�IL-1��������á����ڵ�һ���ٴ�ʵ����������߽���Ƥ�»�ؽ���ע�����sIL-1��������4�ܺ���֢״������û�����Ժ�ת���о����֣�����rhu sIL-1R��IL-1Ra��ϵı�������IL-1�£������������Ϣ���rhu sIL-1R��ʹIL-1�µ�������ǿ���Ӷ�������֢�ķ�չ���������ٴ��ϲ�û�й۲쵽֢״���ص����������
���ڢ���rhu sIL-1R�������ں�IL-1������IL-1Ra��ϣ����Կ��ܻ����ٴ����������á�����ģ��Ҳ��������rhu sIL-1R�������������ٴ�֢״����֯ѧ���䡣Ŀǰ�����Ƽ���û���������塣
C.����IL-1�ļӹ��ͷ��ڣ�IL-1�±��ϳ�Ϊ���Ե�ǰ�������ϸ�����С�IL-1�µķ��ڰ����Ű�ϸ������ת��ø(ICE)�����ļӹ�����ϸ������ת��ø��һ��ϸ�����ӵ���ø����ǰIL-1�¼���Ϊ17kd�ij�����ʽ��ȱ��ICE�����С����֬����(LPS)�Ĵ̼���Ҳ���ܲ���IL-1�£�ͬʱ���ȱ��IL-1��������С���
��ԭ�յ��Ĺؽ���Ҳ�����С�Ԥ����ʹ��ICE���Ƽ����Լ���
��ԭ�յ��Ĺؽ��ķ��������Ѿ������Ĺؽ���Ҳ���Լ�����������(����ģ��)����������ICE�����ӳ�ϸ������ʱ�䣬��������DZ�ڵ����Ӷ������������������Լ����ķ���������ICE�ó��Ķ���ģ���в�δ�������Ƿ������������ļ������ӡ�ICE���Ƽ��д��ڶ�������Σ�Ӧ�������廹��Ҫ�ܳ�ʱ�䡣
��������ϸ������Ϊ��������ƣ�
A.����ĸ����أ�������(interferon��IFN)�Ǿ��ж�������ЧӦ��ϸ�����ӡ�IFN-����IFN-�¾��п������Ϳ���ֳ��ЧӦ��IFN-�ó�����Щ�����⣬���������ߵ��ڵ����á��������������߲��������У������ؿ��ܻ�ռһϯ֮�ء�
IFN-����Tϸ��������ϸ�����ӣ������յ�����ǿ����MHC��ԭ�ı��������RA�ķ�������һ�����á��ڶ���ģ����ע�������IFN-�ÿ������ƻ�Ĥ�а�ϸ���ľۼ���IFN-�ÿ���ͨ������Bϸ��������ѭ���е�������ϸ��������ǰ����ϸ�����ӵı���Ϳ���ֳ�Ļ��������ã��Ӷ�����RA��֢״��Ȼ�����ڴ��а�ο�����յ������У�IFN-��ֻ��ʾ�˷dz�С���ٴ�Ч��������Ŀǰ�Ѿ�����IFN-����ΪRA���Ƶ��о�ҩ�
�Ѿ����������IFN��-1b�ڶ��Ӳ������һ������Ч�����ұ�FDA���������ƶ��Ӳ��������ģ����ʾIFN-�¿�����������
��ԭ�յ��Ĺؽ��ס�С��ģ���ٴ����鷢�ֲ���RA���˿���ȡ��һ������Ч����һ�����ٴ��������ڽ����С�
B.IL-6��IL-6��Ҫ��T�ܰ�ϸ��������ϸ���ͳ���άϸ�������������յ�Bϸ���ֻ�������T�ܰ�ϸ�����յ���ϸ���ϳɼ����ڵ��ס�������������-����IL-1�����յ�IL-6�����������������-����IL-1��ͬ���ǣ�IL-6���ܴ̼���Ĥ����άϸ������PGE2��MMP-1(��֯
��ԭø)��
����ģ�ͽ�ʾ��IL-6�IJ������á���
��ԭ�յ��Ĺؽ��ס����������Ǵ�ģ�ͺͿ�ԭ�յ��Ĺؽ����з�����IL-6�IJ��롣����Щģ���У�ʹ�õ���¡���彫IL-6�кͺؽ��϶�������ᡣIL-6ȱ����С���������
��ԭ�յ��Ĺؽ��ķ������ܹ������������ԡ����ǣ�IL-6ȱ����С��ͬʱҲ��ʾ��������Ĵ����ԡ���������ݰ�ʾ��IL-6���ܾ��п������á�
����IL-6��RA�е�������δ�о�����������ٴ�Ӧ�������IL-6�������ܵ��ܴ�����ơ���Ϊ��Ҫ��һ���İ�ο��������������ȷ����IL-6��RA�е�����Ч�����������IL-6�������ᵽ�����ճ��ϻ���ϳ���ʱ�䡣
C.IL-10��IL-10�������ƾ���ϸ���ĺܶ�ܣ���������IL-1����IL-1�¡�IL-6��IL-8��������������-������-����ϸ������̼����ӡ���ϸ������̼����Ӻ�MMP�IJ�����IL-10�����Դ̼�IL-1Ra��TIMP-1�Ϳ��������������������塣IL-10Ҳ��������
����������NO�ȵĺϳɡ��о�������IL-10��Tϸ����Bϸ���Ĺ��ܶ����������á���֮��IL-10��һ�����п������õ�ϸ�����ӣ����Ի�������ǰ���Է��ӵ����á�
��������Ҳ������ʹ�������IL-10��������
��ԭ�յ��Ĺؽ��Ľ��̣���������Ǻϳɵ����ơ�IL-10��IL-4����ʹ�ÿ�����ת���ǵ��˱䣬�������Dz����ٵ���ϸ����RA��Ĥ�ľۼ�����
��ԭ�յ��Ĺؽ��Ķ���ģ���У������ؽ�ǻ��ע�����IL-10��������岡���������ƹؽ��ķ�չ(������ע��ؽ�)��
��ĿǰΪֹ���Ѿ������һ��������IL-10��RA����Ч���ٴ����顣����IL-10��װ���������ʹ���Լ�IL-10����ʹ�õ��ٴ����鲢δ������������Ч��������IL-10��RA�����е��о�Ŀǰ��չ���ࡣ
D.IL-4��IL-4ͬʱ���п��ס����ߵ��ں����ߴ̼������ԡ�IL-4�ڵ���Thϸ�����͵�ƽ��������Ҫ���ã��ٽ�Th0ϸ����Th2����ת����IL-4�������Ƶ���ϸ������IL-6��IL-8��������������-����IL-1��MMPs�������ƹ�ϸ���γɣ�ͬʱ�̼�IL-1Ra�����ɡ�
��Ȼ�ڶ���ģ���й۲쵽�������IL-4�������������ƹؽ����������ڵĹؽ���������֢ϸ���ľۼ�������Ѫ������γɺؽ���ʴ�ķ������ź����ǣ���RA���ٴ������У������IL-4��û�в����������ٴ�Ч�������Ŀǰ���Ƽ�û�м�����Ϊ����RA���о�����
E.IL-11��IL-11���Լ���ǰ����ϸ�����Ӻ�NO�IJ�������Դ��IL-11�ɹؽ�����ϸ���ͻ�Ĥϸ�����ɣ����Ĺ��ܰ����̼����Ǻͻ�Ĥϸ������TIMPs�����ں��������鶼����IL-11���Բ����������ã�����ֱ�������ڼ���ľ���ϸ����IL-11Ҳ�ܴ̼�һЩ�����ڵ��IJ������������ÿ��ܻή�����Ŀ������á�
1�ں�2���ٴ�����֤ʵ������15��g/kg�����IJ��˿��Բ��������ĺ�ת������IL-11�Ľ�һ���о����ڽ����С�
F.IL-12��IL-12��Th1��Ⱥ���յ�����˿��Կ���������ת�ƺͿ�Ѫ���������⣬IL-12������ǿNKϸ�����ԣ��ϵ�HLA-DR��𤸽���Ӻ�ǰ����ϸ����������ı�������̼�IFN-�õIJ�����ȱ��IL-12�����ʹ�ÿ�IL-12�����С����Լ���ؽ��������ԡ��ڲ�����ڽ���IL-12����Ϳ������������Ӧ���������ʹ���ܹ�����Эͬ���ã���������
��ԭ�յ��Ĺؽ��ķ�չ������IL-12������ѧ���ԣ�����IL-12�ķ������ܻ������������߲������ơ���IL-12����¡������RA�����е�Ӧ�������о��У�������IL-12�Ƽ����о����ܼ����������������Ƽ�����ʹ���ϡ�
G.IL-13��IL-15��IL-16��IL-17��IL-13���кܶ���IL-4���Ƶ����á���
��ԭ�յ��Ĺؽ���ģ���У���ת����IL-13�����ϸ�����룬���Բ������ƹؽ���Ч����
IL-15�����յ�Tϸ����ֳ��Bϸ�����죬�յ�Tϸ�����������������ӣ����Ա���Tϸ����ֹ���������Щ����ʾIL-15���ܻ��ΪRA���Ƶ��о�����
IL-16��CD4�����壬����ʹ����CD4��ϸ����Ӧ���ڶ���ģ����ע�������IL-16�����������ٻ�Ĥ��IFN-�á�IL-1�º�������������-����
IL-17��CD4 Tϸ�������������յ���Ĥϸ���������Խ���(IL-6��IL-8��PGE2��)��Ҳ�����յ�����ϸ�����������������Ӻ�IL-1�¡�IL-17��֤�������ǵ��ƻ��йأ��������ٵ����ǵĺϳɡ�����IL-17�����ɺͻ��Կ��ܳ�Ϊ����RA��һ���ֶΡ�
H.�����ؼ���ĵ���ø��ϸ���������̼��·���һϵ�з�Ӧ����Щ��Ӧ��ϸ��Ĥ���忪ʼ��������Ӧ�ļ�ø����������ϸ�����Ӻ��������ӵı���Ӷ�����ϸ�����ߡ���֢�������Ϊ��P38�ǵ���ø֮һ�����ļ�������ϵ������������ӡ�IL-1��IL-6��IL-8����������ͻ���ø-2�ı�����ͨ������p38���ܻ�������Щǰ���Բ�����µ����ںܶ༲��ģ���У�p38���Ƽ����Բ���һ����Ч����������֢����Ⱦ���ݿ˺ؽ��ס�һЩp38�����Ƽ����ڱ��о������������߲������ơ�
I.������kB(NF-kB)�������������Ӻ�IL-1�����Ǹ��Ե���������ϸ���ڲ���һ����ͬ�ļ�ø�źŴ���;��(NF-kB)������Խ���Ϊ�������������Ӻ�IL-1������ЧӦ�����ص�����Ҳ�ṩ��һ���������ˮƽ���������ϸ���������õ��µ�����;�����о����֣���Ƥ�ʼ����ܹ�����IkBa m
RNA��ת¼��IkBa���ĺϳɣ��������Լ���NF-kB�ĺ�������Ҳ��������Ƥ�ʼ��ؿ���Ч������Ҫ���ơ�
���������Ѿ�֤ʵ�˿�NF-kB���������Լ����е�DZ���������á����ܻ�ڷ�ʹ���ܹ�����NF-kB���Ƽ����Խ��Ͷ���ģ�ؽ������س̶ȡ�
(3)��𤸽���Ӻ�Ѫ������Ϊ���ư�����𤸽���Ӻ�Ѫ������Ϊ��������ƾ��й�����ǰ�������Ϳ�ICAM-1(ϸ����𤸽����)����¡����������������֤��𤸽���ӵķ�����RA�����еĿ����ԡ���һ�������������У�32��RA���˽����˲�ͬ���������Ϳ�ICAM-1����¡���塣�����ʾ�а����IJ����ٴ�֢״�õ��˸��ƣ�����Щ���˽��ܵļ������Ƚϴ�����RA�ĸ��Ƴ̶�Ҫ���ڲ��̽ϳ��IJ��ˡ�����Щ�����У�����Ӧ�ķ���Ҳ���ձ飬��ͷʹ�����ȡ����ġ�Ż�º�Ƥ����Ӧ����������Ч�IJ������ϣ�T�ܰ�ϸ���ʵͷ�Ӧ�ԡ�������������Ϳ����������ķ�Ӧ�ձ���ڣ���ʹ�����Ϳ���������ܵ����ơ�
CD44��hyaluronan(HA)�����壬Ҳ�ǿ��ܱ�����RA�����е�һ��𤸽���ӡ���RA���˵Ĺؽ���HAƬ���쳣���ߣ���ЩƬ�ε����߱���Ϊ����֢��λ��ϸ���鵼��HA���Ӱ��⽵��Ľ����������Ϊ�����������ǡ����ң�HAƬ�ξ��дٽ�Ѫ�����ɵĻ��ԣ��������RA�Ľ�չ�ͳ���������һ�����á����磬CD44��RA��Ĥϸ���Ľ�Ͽ����ϵ�Ѫ��ϸ��𤸽����-1��Ҳ�����յ�����������𤸽���ӵ���ֳ���������֤��˵����ͨ��CD44��HA�����ϸ����Ͽ�������һЩǰ���Է��ӵı��һЩ�о����Ѿ�������CD44����¡���������ھ��н�ǿ�Ŀ������ã�����ģ��Ҳ�����������������ƹؽ��ף������ֿ������õķ����뿹CD44����¡�������ư�ϸ���ۼ��ͼ����˫�ػ����йء�
����Ѫ���γ���RA�ؽ���Ѫ�����γɵ���Ҫ���ơ��ٽ�Ѫ�����ɵ���������Ŀǰ��û�б�ȷ������ĤҺ����֯�и����ٽ�Ѫ�����ɵķ��ӣ�����IL-8��Ѫ����Ƥ�������ӡ�����άϸ���������ӺͿ�����𤸽����(���磬Eѡ���ء�Ѫ��ϸ��𤸽����)����
��ԭ�յ��Ĺؽ����У�Ѫ�����ɵ����Ƽ�(��������ù��������A
GM-1470)���Գɹ��ط�ֹѪ���������Ѫ�ܵ��γɡ������ئ�V��3������Ѫ���γɵ���Ҫ�������ӡ��ڿ�ԭ�յ�è�ؽ������ڣ��ؽ���ע�������ئ�V��3�������������ƻ�ĤѪ�����ɣ����ٻ�Ĥϸ������Ѫ�����γɺ�������ʴ������֮�⣬���Թؽ����Ц�V��3������ʹ��Ҳ������Ч�ؽ��ؽ������س̶ȡ�IL-8�Ƕ��ܰ�ϸ����������ϸ�����������õ�ϸ�����ӣ�ͬʱҲ���дٽ�Ѫ���������ã���Ҫ�ɻ�Ĥ����ϸ����������RA��ĤҺ���쳣���ࡣ�����������Ӻ�IL-1�ܹ�Эͬ���ٽ���Ĥ����άϸ��IL-8�ı���ͷ��ڡ���è�Ĺؽ�ǻ�ڳ���ע��IL-8�����������صĹؽ��ף���������IL-8���ܻ����RA��
(4)�������Ƽ����������ļ�����Բ����ܶ���Ը�������ǿ��Ծ������߱��������ߵ��ڻ�ٽ���֢�����ԡ��������ĩ����ɷ�C5a��C5b-9����㷺��Χ����֢��Ӧ��C5a��һ���������������ӣ����Ե��ڶ�����֢�������ӡ���C5����¡����ij���Ŀ���Ƿ�ֹC5�����гɾ������Ի��Եĸ�����ھ����յ��Ĺؽ����У�ʹ�ÿ�C5����¡�����������С�����ڼ������ĩ���壬�����߹���С����ؽ��ķ���Ҳ���Ա���ֹ������RA��SLE��������ʹ�����C5a����¡����ļ����Ͱ�ȫ�����Ѿ���ɣ�û�й۲쵽���ԵĶ��ԡ����ֵ���¡�����2���ٴ��������ڽ��С�
(5)ϸ����������RA�У�Tϸ������Ļ��Ƶ�Ŀǰ��δ�˽����������������ʾCD4 /CD28-��Tϸ����Bcl-2���ϵ�Ϊ������Bcl-2��һ�����浰�ף����ܻ�ٽ�������Ӧ��Tϸ���Ŀ�¡����������RA��Ĥ�У�Fas���е�Tϸ�����Ա����������Tϸ����������ԭ�ı�λ������ʾ�Կ�fas�������Կ�����RA�б�����Tϸ����ѡ���ǡ���Ȥ���ǣ��װ����������ʾ����ͨ��������CD95��;����ѡ���Ե��ƻ�����ѪTϸ������RA���������������Լ����У������Ļ��ƻ���Ҫ��һ���о���
���ӻ�Ĥϸ���ĵ�����RA���Ƶ���һ��;������������ǿ�������ٲ��ּ�����Ĥ��ֳ�Ľ��̡�Fas(CD95)����������������ֳϸ�������������壬������Ĥϸ����Fas�뿹Fas����¡�����Fas���彻�����յ�ϸ���������ڶ���ģ���У�����Fas��������Fas����IJ�������ע����ؽ�ǻ�ڣ���ʱ���ڹؽ����͵�֢״�ܿ켴����ʧ��֤ʵ�˻�Ĥ��������ǿ����֢�ļ��ᡣ�ڹؽ�������ת����CD95�������Ҳ��ʾͬ���Ľ�������ԣ���ǿ��Ĥϸ���ĵ���������ΪRA�����Ʒ���֮һ��
(6)��������ø���Ƽ���RA�����Ǻǵ��ƻ��Ǽ���MMPs(��������ø)���õĽ��������ø���ɼ���Ļ�Ĥϸ���ͽ���ľ���ϸ�������ġ��������������ӺͿ�IL-1����ͨ����������ϸ���Ӷ�����MMPs�IJ���������ҩ�������Ƥ�ʼ��غͼװ�����Ҳ���Լ���MMPs�ı��
�ڢ���
��ԭ�յ��Ĺؽ����У���Ĥ��ע��TIMP-1�����������ؽ������س̶ȡ����ǣ��Ƿ���Դ��TIMPs��ע�������������ò���ʮ�ֿ϶�����Ϊ�ڵ����DZ����ǰ��TIMPs�ܹ������������ǵ������١���һ�ַ�����ͨ��ʹ����ά����A�������Ӿֲ�TIMPs�ĺ�����
�Ļ��ؿ������Ƽ���
��ԭø����ʴø��
���Ե���ø����������(����ŵ����)Ҳ������ͬ�����ԡ���С��������RA���˳���4����ٴ��۲������ʹ����ŵ�������и���IJ��˵õ����⡣���������Ե�����MMPs�ĺϳ��������о��С�
8.���ʪ�ؽ������Ʋ��� ���ʪ�ؽ��������Ƕ��ģ�����������������������ʳ��ҩ���ƺ��������ơ���ѧ����Ϊ�����ʪ�ؽ��ײ��̵IJ�ͬ�Σ����ƵIJ��ص�������ͬ��Ϊ���������Ϊ�ؽ�RA�IJ��̻���Ϊ��ȷ���RAǰ��ȷ��RA������RA��������RA����ʱ�ڽ��з�����
(1)��ȷ������ʪ�ؽ���ǰ���½������Ĺؽ���ʹ�ͽ�ֱ������ij�����Լ����ı���֮һ��Ҳ�����������Բ��̡����ಡ��ֻ���ٲ������ջᷢչ��RA����Լ����һ����˻���ȫ���⡣����ͳ�ƹ�1994����������������HMOҽԺ��RA���˴ӷ���������������ʱ��ƽ��Ϊ36�ܡ���ô����ʱ�����벡�˺��ٴ�ҽ����̬�ȶ��й�ϵ��һ���没�˲�Ը����ΪһЩС����ȥ��������һ�����ٴ�ҽ����Ը��������˴���RA��ñ�ӡ���Ҫǿ�����ǣ���ʹû��ȷ��Ҳ��Ҫ���л�����Ч�����ơ�
����ȷ���֮ǰ��ҩ�����Ƶ�Ŀ����Ҫ����ʹ������ʹ����ʹҩ�����̴�����ҩ��������������(����Ϣʹ)���������ⱨ����û�иβ��������ÿ
������õ�3g����ࡣ��������������ɴ������������ҩ������ʹЧ�����ѡ�����ҩ�ﵥ������ʹ�ò�Ӧ����6�ܡ�
����̴�����ҩ��δ�ֻ���ؽ�����ʹ��Ҳ�϶ࡣ�����е��о���������˾ƥ����ͬ��ҩ�и����ý�С���Ƚϰ�ȫ����������
ˮ����(��ˮ����
ˮ����)��ȫ�Ը��ã����Ƕ��ʺϳ���ʹ�á�����̴�����ҩʹ��ʱҪע��θ�����ĸ����ã��������Խϲ�Ļ��߿�ѡ������COX-2���Ƽ���
��������(celecoxib)�ȡ�һ��ʹ�ô���ҩ�ﶼ�������õ�������������ǣ��ٴ����NSAIDs�����ý϶ࡣ������еȼ���NSAIDs��֢״���Ʋ����⣬�����п��ܷ�չ��RA���������Լ�������ʱ����Ҫ��Ӧ�����ƣ��ʲ���Ҫʹ����������NSAIDs������֢״��
����һ�㲻�����ڴ��ಡ����ʹ�ã���Ϊ����ʹ����֢״��ɻ���ܿ죬���������ڸDz��飬����ʹ�ø����ýϴ�
����Ӧ����ͬʱ���У����ڼ��緢�ֿ��ܵIJ���
ͬʱҽ��Ӧ�ý������ˣ�������֢�ؽ���˵�������˶���Ȼ���Լ�����֢�����ʵ����˶����Ա������ɥʧ�ؽڹ��ܣ���������Ҫ�����ҵ��˶�����Ϣ�����ƽ�⡣����ʹ�Ĺؽڼ������ڼа�̶��������Ҳ������б����˶����Է�ֹ�������������ж���֢�Ĺؽڶ��ԣ�������еȳ��������Բ����㹻�ļ������������عؽ���֢״��ÿ����м��γ���6s������������Է�ֹ�ؽ���Χ����ή�����Թؽ���֢����Ϳ�������IJ��˿��Խ����ʵ�������ѵ�����ܹ��������Ƽ�������ʹ��ƣ�͡�
(2)����ȷ�����ʪ�ؽ������ƣ������ߵ��ٴ����֡�ʵ���Ҽ���Ӱ��ѧ�����Ѿ��ܹ���ȷ���RAʱ��������Ȼ��ҩ��Ϊ����ͬʱ��϶Բ��˵Ľ�������������ƺ������ȶ����ֶΡ�
��ҩ�����Ƶķ�����
A.�������ƣ��о���������RA��ʼ�������ںܶ���г�����Ի�Ĥ�IJ��˻���ֹؽ����Dz���������ֲ�����1���ڷ��������ҹؽ�����ƻ��̶ȵ�50%�����ڼ�����ǰ5���ڡ�����Ϊֹ�������ٴ����鶼֧�����ڻ���������(early aggressive therapy)���Ը��õظ���RA�Ľ�֡�Pincusʹ������4��֤���ܽ��˶�RA���ڽ�����Ч�ͻ�����Ԥ��ԭ��
a.20����80������о������������ΪRA�IJ�����5��20���ڹؽڹ��ܺ��������ʽ������½���ͬʱ������������
b.�ֲ��˹ؽڵĹ���ʴ�ؽ�ǻ�ı�խ�����������2���ڣ������Ժ��ʱ���ڳʽ����Է�չ���������2����Ӱ��ѧ����ʾ�Ķ��ٶȴ��ں��ꡣһ����ֳ�Ļ�Ĥ��ʼ�ַ����ƻ��ؽ����ǣ��ؽھʹ��ڲ��������ƻ���Σ��֮�У������Ժ���Խ��͡�
c.���ʪ�ؽ��IJ�����
�����ٴ�״��Ԥ�⣬������ֱ�Ӷ�Ӧ�������Ļ�Ժ�������Խ�ߣ����Խ�
d.�ڹ�ȥ�����̳���2���RA����ʹ�ô�ͳ�ķ������ƣ�ֻ���ٲ��ֲ��˵IJ��������Ч���ơ����ԣ�Ŀǰ���ڷ�ʪ��ѧ�Һ��ٴ�ҽ����˵������RA����ս���ھ�������ؿ�ʼʵʩ���ƣ������̼����Ľ��̡���ˣ�������ʪ��ѧѧ��ġ����ʪ�ؽ�������ָ��2002�桷�н���RA����������г����Ĺؽ�ʹ��������ƣ�͡���Ĥ��ESR��CRP���ߣ���Ӧ���ڲ�����3���µ�ʱ����ʹ��DMARDҩ��ͬʱӦ�������Ƹ����õķ����������ɴ������������
��ˣ�������ʪ��ѧѧ��ġ����ʪ�ؽ�������ָ��2002�桷�н���RA����������г����Ĺؽ�ʹ��������ƣ�͡���Ĥ��ESR��CRP���ߣ���Ӧ���ڲ�����3���µ�ʱ����ʹ��DMARDs�����ڹؽڼ���Ӱ��ѧ֤�����ڳ����Ļ�Ĥ�ؽ���δ�����ƹ��IJ���Ӧ����ʹ��DMARDs��
������RA�Ƿ���Ҫ������ҩ�д���һЩ���ۣ���ѧ����Ϊ�е�����RAʹ�õ���ҩ�T�ɿ���֢״���������������ҩ����Ч��һ�������ӣ����������Ӹ����ã����е�ѧ����Ϊ����RA�����Ʒdz���Ҫ����һʱ�ڻ�Ĥ�Ļ���̶Ƚ�������Ԥ�������ҪӰ�죬��������������ҩ�Դﵽ�ؽڻ�Ĥ��֢����⡣1997��Boer�Ⱦ�֤��������RA������ʹ�üװ����ʡ���������ऺ������ɵ���̨����(��������ʼ��Ϊ60mg/d���ڼ�����Ѹ�ټ�����7.5mg/d�����ڵ�28��ʱͣ�ã��װ����ʼ���Ϊ7.5mg/d���ڵ�40��ͣ�á�)Ч��Ҫ���ڵ�����������ण����������ɺͼװ����ʶ�ͣ�ú��������ٴ�֢״������Ч����£�����������ҩ�飬4���Ժ�ؽ��ƻ��ij̶ȣ����Աȵ�����ҩ���ᡣMottonnenҲ����������RA�мװ����ʡ���������ऺ�HCQ����ʹ��Ч������DMARDs����ʹ�á�������Щ�ٴ�����Ľ����Ŀǰ�����ڶԴ�RA���˿�ʼ��ʹ���������ƣ����ڲ�����̨�������ǿ�����̨�����������ۣ�����Ҫ���и�������ٴ����顣������RAʹ�������Ƽ����ϼװ��������Ƶ�С��ģ�о����֣��������ٴ�֢״�Ŀ����ϣ������ڼ����ؽ��ƻ��Ľ�չ�ϣ�������ҩ��Ҫ���ڼװ����ʵ��á�����ȱ�ٴ��ģ���ٴ�����ͳ��ڹ۲죬�����Ŀǰ��û�еõ�ACR����ʽ�Ƽ���
B.����RA��ѡDMARDs�������Ѿ���ʶ������ʹ��DMARDs���Է�ֹ�ͼ���ؽ��ƻ��������ؽڵĹ��ܣ������ڹؽڷ����ƻ�ǰʹ��Ч�����á�����RA�������������ڽεõ���ϣ���������ʹ��DMARDs��ʱ����?������ʪ��ѧѧ���ڡ����ʪ�ؽ�������ָ��2002�桷��ָ��������һ���Ѿ�ȷ���RA���ߣ����ʹ��������NSAIDs��Ȼ���ڳ����Ĺؽ�ʹ�����صij�����ƣ�͡���Ի�Ĥ�ס�ESR��CRPˮƽ�������ߡ�����ѧ�����ʾ�ؽ��ƻ�����DMARDs��ʹ����Ӧ�Ϻ�3���£����κ�δ�������ƵIJ���������г����Ļ�Ĥ�ؽ��ƻ���Ӧ����ʹ��DMARDs�Է�ֹ������ؽڵĽ�һ���ƻ���
����ŷ�����ұȽϳ��õ�DMARDs�мװ����ʡ�
���������������ड��������ء�
����������infliximab��ʹ�ý��ٵ����������ʡ���ù��(D-��ù��)�����Ƽ�����ŵ���غͻ�����A����Щҩ���ѡ���ܺܶ����ص�Ӱ�죬���ڰ�ȫ������ͷ��õĿ��ǣ�ŷ�ķ�ʪ��ѧ�Ҵ������ѡ��
���������������ण��������ķ�ʪ��ѧ������ѡ�üװ����ʣ�����һ������ܻ��Ԥ��ܲ��õĻ��ߣ����Ƽ�ʹ�üװ����ʻ��������ơ�����ҩ��Ĵ����������35��
����DMARDs��ҩ֮����бȽϵ��ٴ����鲻�Ǻܶ࣬������о����֣������е�DMARDs�У�û����һ��ҩ���ڼװ�����(����Ч���������á������Ժͷ��õ�)���ʼװ�����Ŀǰ��DMARDs��ռ����Ҫ�ĵ�λ��������Ϊ��������ҩ����Чʱ�ıȽϱ���
C.DMARDs���������ƣ����ʹ�õ���DMARDs��������ؿ����ٴ�֢״���ֹ�����չ����������DMARDsҩ�������ʹ�á�������ҩ��3�������a.��ʼʱʹ�ü���DMARDs��ȡ�ò������⣬�������ȶ�����ȥһЩҩ������������ٵ�ҩ��ά�֣��������ν����̨����(step-down)��b.��ʼʱʹ��һ��DMARDs�����֢״���Ʋ����⣬��������������DMARDs��ֱ�����鱻����Ϊֹ����Ϊ��̨����(step-up)��c.һ��ʼ��ʹ�����ֻ�����DMARDsҩ�ﲢ����ʹ�ã�ֻ���м����ϵĵ���������ƽ�з���(parallel approach)������ʹ����һ�ַ���Ŀǰ������һЩ���ۣ�����ʹ�ú��ַ�����ǿ���Ķ���ҩ�������ʹ�ã�����ʹ�����ַ�������Ŀ�Ķ�������Ч�����Ӷ������ü��١����ڼװ�����������RA�е�������Խ�ԣ�Ŀǰ�����Ž�����Ϊ������ҩ�Ļ���(corner stone)��
����������Ҫ���ڲ��̽ϳ���������(ָ�Ѿ���������ʹ������DMARDs�������Ǽװ����ʺ���������ण���Ч������)RA���ߣ��о������װ����ʡ���������ऺ�HCQ��������ʹ�õ�Ч��Ҫ������3��ҩ�������ϣ����������ϵ�Ч����Ҫ���ڵ�ҩ���ã�����������ҩ�ĸ������뵥ҩʹ��û���������Tugwell��Ҳ���ּװ����ʺͻ�����A����Ч�����ڼװ����ʻ�����A����ʹ�ã����dz�����÷����и�Ѫѹ�ķ�����Ѫ����ˮƽ�����ߡ�������о����֣������Ƽ��ͼװ���������ʹ�ö�������RA�Ķ�����Ч�ܺã����Ҹ�����Ҳ�dz�С��������Ч���ڹ۲��С�������Ŀǰ������RA�Ƿ���Ҫ������ҩ�д���һЩ����(��36��37)��
������RA�Ĵ������̺�����ָ�ϣ�������ʪ��ѧѧ�ᡶ���ʪ�ؽ�������ָ��2002�������ʪ�ؽ��Ĵ���������ͼ44��ʾ��
�����ķ�ʪ��ѧ����1999���2000��ֱ�����һ��������������RA��������״���������һЩ��ʶ��Ϊ21���ͳ�RA�������ṩ��һ��ָ�ϡ���Щ��ʶ������
A.����RA�������Ŀ����������Ĥ�ͼ����Ļ�ԡ�
B.�����������ˣ����еIJ��˶�Ӧ��ʹ��DMARDs�������Ƽ�����Ϊ���ǵ��������˵����䡢��Ը��ҩ����Դ�ͷdz����ļ�����ԣ��������ǿ��ݲ���������ҩ���ơ�
C.������ʱ�����ܲ��̳��̺Ͳ������䣬Ӧʩ�����ƽ������Ƽ��Ĵ�ʩ��
D.����ʹ������Ч��DMARDs��
E.���������ձ�ʹ�õ�DMARDs�Ǽװ����ʣ���ͳ�ư����װ����ʻ������Чҩ������Ƽƻ���������ٴ������ж�85%��RA�������ʺϵġ�
F.DMARDsӦ�ñ��õ��㹻������������С����ʱ�Ѿ��ﵽ���������Ч�������Ѿ������ĸ����õ����ơ��Լװ�������˵�㹻����Ϊ����20mg/�ܣ����������Ϊ3g/d��
G.����Ӧ�þ��翪ʼ��ͨ����Ҫ����һ���κ���ܶ�RA���������������ʱ�ڵȴ�ʵ���ҵĽ�����ʱ���ڲ����κδ�������(��)�۲컼�߶Ե�1�ξ���ʱ�������Ƶķ�Ӧ���ǿ��еġ��������ֵȴ�Ӧ�ø���ʵ��������ţ��ڵ�1�ξ���ʱ������������ƿ�����ǡ���ġ�
H.��������Ļ�Բ��ܵõ���ֵĿ��ƣ���˵����ʱ������ʧ�ܡ�
I.һ����˵��DMARDs�㹻������ʱ��ֱ���ע����Ƽ�5���£���ù��6���£�
�����4���£�����DMARD�������Ƽ�3���¡�������ʱҩ����ȫ����������Ҫ��ʱ�������Ҫ��������ٴ�������ʱ����ӳ���ҩ�����Ч����ǿ����ȴ�������ǡ���ġ�
J.����������ؿ��Ʋ���ʱ��Ӧ�û��û���������DMARDs�������Ƽ���
K.DMARDs�������Ƽ���ʹ��Ҳ��һ�����ݡ�������߶Լװ����ʻ��������ص���Ч���ѣ����������DMARDsҲ�����кõ���Ч������������¿�����Ҫ���û����������Ƽ��������������DMARDs��������ʹ�üװ����� HCQ ���������������װ����� CsA�������ơ�
L.��������߶�DMARDs�������Ƽ����Ʋ�����ȫ��Ч�����ಡ��Ӧ��������Ч�����ƴ�ʩ���������Ļ�����DMARDs�����Ǻõ����Ʋ��ԡ�
M.�����ƹ����У����ݲ�������Ʒ�Ӧʹ�������Ƽ��������ʵ��ġ����ڽ�չ��RA��DMARDs������Чʱ����Ӧʹ�ÿ�ϸ���������ơ��������������ƿ��ٽ����ԡ������Լ�����
N.��ʹ��DMARDsʱӦ�ÿ��ǵ�Ԥ�����أ�������������ѧ�Ľ�չ��
0.���ý���(
��ŵ��)�Ͷ��Խϴ��DMARDs�Ѿ�����ʹ�ã�Ҳ���Ƽ�ʹ�á�
P.��Ƥ�ʼ����������ĸ����ã���ʹ����Ȼ�������ۣ����Ǻܶ��ʪ��ר������С����(10mg)����Ч����ȫ�ġ�
Q.����Ҫ��ʹ��NSAID��(��)����ʹ������������һ�ָ������ƶ���Щ�����Ǻ��ʵġ�
R.���е����Ʒ������뿼�ǵ����˵�ҽѧ����ᡢ�����;���״̬�����˵���Ը�dz���Ҫ��
S.ʹ��ҩ��ʱӦ�ø�֪�������ƽ������ĸ����á�
T.������ǰ���������Ƶ�Ч��ʱ����Ҫ�Բ����Խ���ר�ŵ���������������Ӧ����ACR�ĺ��ı�Ϊģʽ������Ҫ��������ʹ�����������ԡ����ܡ������ڷ�Ӧ��ؽڼ�����������
���������ƣ�
A.������һ���о�������RA�IJ������벡�˵Ľ����̶ȳɷ��ȣ����������������䡢���̡��ؽڼ��������ܲ�����ҩ�������͡����ܽ����̶���RAת��֮�����ϵ�����Ǻ���ȷ�����ǽ��������˽����ʪ�ؽ���Σ���ԡ�����Ѱ������Ͳ��õ����Ʒ�������������õ�Ԥ�������ڴ��ಡ�������С��ؽ������Ҵ�������(ASMP)֮���ֲ�����ʹ�̶ȼ��ͣ����Լ��ٿ������������ٻ��ѡ�������ѯ���Ի��ⲡ�˵�ѹ���������������ֿ�������֮��ʹ���߸е��Լ����ڻ������Ƽ����������뵽����֮�С�����Ŀǰ���ⷽ��Ĺ�������Ƿȱ���������ڲ��˺ܶࡢ���Թ˼����е�ҽʦ�Դ�Ҳ�������ӡ����ž�ҽ�����ĸ��ƺͲ��˽���ˮƽ����ߣ����˶��ⷽ���Ҫ��Ҳ����֮���ӡ�
B.�������ƣ���Ĥ�����ڽεĽ綨����Ҫ���������Ӧ�û���֪�������ȷʹ�ùؽڣ��Ա�����عؽڵ��ƻ��������Ʒ�������ԭ���Ǿ����ܱ����ڳ��غͷdz��عؽ�ʩ�ӹ��ȵ���������һ��Գ��عؽ���˵���DZ��ⲻ��г����ײ���Լ��ڳ���ʱ����Ĺ����������ظ����������Էdz��عؽ���˵�ؼ��DZ�����������ļ�����������ΪץȡС���ʱ����Ҫ���������Ի��л�Ի�Ĥ�IJ��˸��ʺ�ʹ�þ��нϴ��ܾ��Ĺ��ߣ�������ʹ��˫�֡���һ��������ע�������Ǿ����ܱ����ظ���������Ϊ�������Լ��������Թؽڵ�Ӱ�졣�о�������ǡ�����˶�������ǿ��������ճ��������������ƣ�͵ij̶ȣ����ƶԲ��������Ե���������������״̬�����ҿ���������ʹ�����ԡ�
C.��ʳ�Ʒ�������һֱ��Ѱ����ʳ�����ʪ�ؽ���֢״�IJ��������ػ�֮��Ĺ�ϵ������ͨ���������ߵ���ʳ��ȥ�Լ������������أ�������������ֹͣ��ҩ�������ⷽ����о��Ѿ������˺ܶ࣬����Ŀǰ����Щ���滹�������ۡ�
�����ͳ���֬���ᣬ��
������ҹӣ���͵ȣ��Լ�ijЩ��Ԫ�������ȣ���ʹRA���ߵ�֢״���⡣�����ܼ�����ʹ�����͵Ĺؽ���Ŀ�����ҿ��Լ��ٳ���ʱ�䣬��ǿ�������ӻ�ƣ�͵ȣ����������������ܸı䲡�̡�
��֪����ȱ������Ӱ�����߷�Ӧ��������ʳ���Ƶ�RA���˳������ؼ��ᣬ������Ϊ֬�����������ٵ�Ե�ʡ����ܼ���������߷�Ӧ�ܵ����ƣ�������RA֢״�Ļ��⡣����ǿ�����ǣ���������ֵ�֤��˵����ʳ���ƿ���ת��RA�IJ��̣����Ը�����ֻ�ܿ���������ʩ��ͬʱ��������ʳҲ��Ԥ��֢״�������ֶ�֮һ��
D.������ƣ����ʪ�ؽ����������Ʒ�Ϊ�����ࣺԤ�����������ؽ���(����)�������ڲ��̵IJ�ͬ�ν��в�ͬ��������
��Ҫǿ�����ǣ��ڶԲ��˿�ʼ����ʱ��Ӧ�������ҽ�����룬�ڲ��̵IJ�ͬ�ι�ͬ�ƶ���Ӧ�����Ƽƻ�����RA���˳������Կ��Ƶ���ʹ�����Χ�����ƻ�ؽڹ��ܵ�����ʱ�������Կ���������Ԥ�����ڲ�ȡԤ�������������ڸ��ƹؽڹ��ܡ�
F.�������ƣ����ʪ�ؽ�������һ�����Լ��������ҿ����漰ȫ��������١�ϵͳ�����ƱȽ����ѣ�����Ǩ�Ӳ����������������϶����������ϸ����ߴ���ʹ�࣬Ӱ�컼�ߵ�����������������ؿ���ͨ����-�ڷ���ϵͳֱ������������ϵͳ�������书�����ң������ʪ�Լ�����Ҳ����ͨ����֪����Ϊ������Ӱ�켲����֢״�仯������ת�飬Ӱ�����ƺ��������ڴ�ͳ��ҽѧģʽ�Ѿ�������-����-�����һ����ҽѧģʽת�䣬�������������ܵ����ӣ�Ҳ��Ϊ��ҩ�����ơ��������ƺͿ�������֮��һ����Ҫ�����Ʒ�ʽ��˹̹����ѧ��Kate Lorig����Ƶ�������������(self-help education management)����Ч�����ӻ��߹��ڷ�ʪ�Լ�����֪ʶ��������ʹ����һ��������������Լ�������֪��Ϊ�Ʒ�(cognition-behavior treatment��CBT)��Ҫ���ڻ�����ʹ���������ʪ�ؽ��ס��������������ٴ��ϳ���������һ���������ƣ���֤ʵ�Ի����ʪ�Լ������ߵ�֢״���������������ȷ��Ч����
(3)�������ʪ�ؽ������ƣ���������Ϊ�������Ʋ�����ɹؽڻ����Լ���������֢ʱ�����Ƶ��ص���ݼ����Ļ�������ͬ��
����RA��һ���ص㣬����ȼ������(burning-up)����Ҳ����˵����֢״�Ͽ������˵Ĺؽ����͡���ʹ���Լ��ᣬ�������������糿����ƣ���к�ƶѪ��Ȼ�������ء�ʵ���ϴ�ʱ��֢�Ժܻ�Ծ��Ӧ�ø�����������ơ����������治ͬ���ǣ����ڲ��˲��̺ܳ����������Ĺ�����Խϲ����Ҫ�ر�ע��������ҩ�︱���õ�ָ�ꡣ
������߲���ƽ�ȣ���ô���Ƶ��ص������μ���ؽڵĻ��Ρ���ʱ��Ҫ�������ֶ�������������������ơ��������ƿ���������ԭ��ͽ�����У�
�����κο����Ʒ������ȿ��ǿ�����ʹ��
����һ��Ŀ����Ӧ�����Ʒ���Ӧ�����ܼ�ಢ����ʵʩ��
�۶Ի��߽��г�ֵĽ���ʹ֮�������Ƶ�Ŀ�ģ�����ߵ������ԡ�
����Ϣ���ƶ����Լ�����֢����ͬʱҲ�ٽ��������������������Ϣ������ʵ����˶���ƽ�⡣
�ݹؽڱ���ԭ��A.�ؽ��ڼа�̶�����Ϣ��ʱ���������λ���Ա�����Σ�B.������������λ�任ʱע�������������ԡ��ؽڱ�������ȫ��ʡ����C.�ʱ�ڿ��ܵķ�Χ��Ӧʹ����ǿ׳�Ĺؽڣ�D.�ƻ���ʩ�ж���ʱӦ���ؽڵĹ��ú���ʹ�ü�����С��ͬʱӦע��ʡ����
���˶��Ʒ��кܶ�Ŀ�꣬ͨ��ͨ������Ķ���ֻ��һ��Ŀ�걻��ѵ���ɡ���ЩĿ�������A.���ֹ��ܣ�B.�ָ����ܣ�C.���������;�̬������D.�����˶�������E.��ǿ���õ����Ҹо���F.�ṩ��Ѫ�ܷ����ѵ����G.�ṩ�˶������֡�
��ʹ�üа�Ӧ����Ϊ�˻�����ʹ���ƹ��ܣ�������Ϊ�������������λ��ظ��Ѿ���������������ʱʹ�á�
������ƵĽ���һ���ǣ�A.������ʹ��B.�ָ��ؽ�����λ�ã�C.�ָ�������D.�ָ����ܡ�
���ʱ�ڵ�����������ؽ�����Ϊ�����ؽ������Ƕ��Ѿ������˹����ƻ��Ĺؽڶ��ԣ���Ҫ�йؽڹ̶����ؽڳ��������ܶ�ؽڵĹؽڹ̶��������ѶȽϴ����Ѽ�������������Щ�ؽڣ�����ؽں��м��ƹǹؽڵ��ں϶Խ����ʹ���ƹ��ܺ���Ч��Ŀǰ���ڽ��С����ڼ�����Ϻ�ճ�̼��ĸĽ����ؽڳ�����ʵ���Ѿ��ݱ�Ϊ�ؽ��û�����
(4)���������ʪ�ؽ������ƣ�������RA��������Խ�Ϊ���֣������������\���ķ�չ��Ŀǰ���Ƶ��ֶν���ǰ�Ѿ��ḻ�����ࡣ�������³��ֵ������Ƽ�����Ѫ��ϸ����ֲ�ȷ�����Ϊ������RA���ߴ���һ��ϣ����������������Щ��������ʮ�ֳ��졣�����������ţ����õ�δ��������RAһ���ᱻ������
��ѧ�߽����������RA(��Լװ�����Ч��������)�����ƿ��Բ������·���(��38)��
9.RA���Ƶķ�չ����
(1)�������ƣ�Ŀǰ��Ϊϸ��������RA�ķ���������������Ҫ�����ã�������IL-1��������������-���ȡ��������ڶ���ģ�ͻ�����RA�������϶����֣������۹ؽ�ǻ�ڿ��Լ���������IL-1����(sIL-1R)�Ϳ�����������������-������(s�����������Ӧ�-R)����Щ���ʿ�����ֹIL-1��������������-������Եİ�ϸ�������ϣ�������һ�ֱ����Ե����ʡ����ǣ��ɻ����Է���������Щ���ʺ������٣������Եֿ�IL-1�������������Ӧ���������һϵ�з�Ӧ��������û�����������Ĵ������ʣ��Ϳ��Լ����������RA�Ľ�չ���̣�������Щ��Դ�Ե����ʱ�������������RA��ҩ��������ĸ����ö�ҪС�öࡣ����������£���������Ӧ�˶�����
�������Ƶ�ԭ�����ǣ�����RA���������õĵ����ʵĻ�����뵼�������ϸ���ڣ�ʹ�䳤�ڸ�Ч����һ��ˮƽ����Щ�����ʣ��ﵽ���Ƶ�Ŀ�ġ�Ŀǰ������ķ����������ࣺһ���ǽ������ϸ����ȡ���������һ���Ļ�������ֳ������ٽ����������ڣ���һ�־���ֱ�ӽ�����һ����������������������ڣ������ڽ��������ϸ�������ڶ�RA���л������Ƶ�һ�������˵IJ��Ծ��ǽ����ؽ�����(anti-arthritis gene)ת�Ƶ����۹ؽڵĻ�Ĥ��ϸ����(synovial lining)�������ں����ⷽ����Ӧ�õ����岻ͬ�������⣬��ת¼�����鵼�Ļ���ת����һ���ɿ��ļ��������õĹؽ��ڿ��Դ�������6�ܵĹؽ��ڻ���������������֢�����������á����õĿ�ԭ�յ��Ĺؽ���ģ�͡�è�����ϸ�����յ��Ĺؽ���ģ�͡���
��ԭ��
��ĸ�����յ��Ĺؽ���ģ���У��Ը��ַ�ʽ������IL-l��������(IL-1Ra)�Ļ�������ԶԹؽڲ������ֱ������á�
�����ڣ��������뵽�ؽڵĻ�Ĥ��ϸ������ͨ���ٲ�����AAV(adenoassociated virus)��֬�������D
NA��ʹ����Щ���壬���������IL-1�����(sIL-1R��)�Ļ������õ�
��ԭ�յ��Ĺؽ���ģ������ʾ�������Ŀ��ؽ����ԡ�ʹ���ٲ����ֲ����벡��IL-10(vIL-10)����
��ԭ�յ��Ĺؽ���ģ����Ҳ��ʾ�˿��ؽ����ԡ���Ȥ���ǣ���ʵ�������ⷢ�֣�sIL-1R���vIL-10����ĵ��벻����ע��ؽڣ������ڷ�ע��ؽڶ������Ƽ����Ļ��ԡ�
���˵��뿹�����ߵ���ϸ�����ӵĻ����⣬���ܵ����������Ա�ɾ���Ļ������磬���������ռ�ø�����룬�������������Τ�Ϳ���ɱ����Ĥ�ںͻ�Ĥ��Χ��ϸ���������ø�����Τɱ�����������ټ�ø��������ϵ�ϸ����ʵ����ҩ���Ի�ģ�г����������㹻��Ŀ�����ڷֻ��Ļ�Ĥϸ�����Ա���Ч��ɱ����������֪���������͵ġ�����Ĥ�г����ȴ�ͳ�Ļ�Ĥ�г�����ʲô�ŵ㡣���ַ����Ѿ��о��˶��꣬���dz��ڵĽ�����DZȽϺ�����fas��λ(fas L)����ĵ���Ҳ���о���һ������������������£���ת���Ļ�Ĥϸ��ͨ��fas����ͬʱ����ѡ����ɱ���ؽ��������T�ܰ�ϸ������������˿��Ը���Ч�Ŀ��Ʋ��顣Kobayashi�ȷ���fas����������ṹ��(F
ADD)��fas�鵼�Ļ�Ĥϸ����������ؼ������á�ͨ���ٲ�����������RA��Ĥϸ����תȾF
ADD��������յ�F
ADD������ϵ��͵���������ֲ������RA��Ĥϸ����������������ȱ�ݲ�(SCID)С��Ĺؽ��ھֲ�ע��F
ADD�ٲ���(Ad-F
ADD)������ͨ���յ�����������Ĥϸ�����������ֵ���ֻ���ڻ�Ĥ��֯����Ӱ������ϸ����
�����ؽ�������Ƣϸ����ʵ������˳ɹ��Ľ���������ʵ��ϵͳ�У�����
��ԭ�յ��ؽ���С����Ƣϸ����������������SCIDС���С�ʹ�ñ���S������������
RI��ת���������Ӧ�1(TGF-��1)�����ʵ��ȡ���˽ϺõĽ����
��RA����ģ��ʵ���У�������s������������R��vIL-10���ٲ�������ϵͳ�Ե���Ҳ��ʾ�˸��ƹؽ������������ܼ����������ѭ���о��Ѿ���ⲻ��ת�������俹�ؽ���Ч�����Գ�������ʱ�䡣����������£�ֵ��ע����ǣ�Ϊ���������Ŀ��ؽ�����������Ҫע����ٲ�������������ӽ��ڲ������ظ���������
��һ�ַ����Ǽ�ע���뿹�ؽ�������D
NA������ͨ������;����������ˮƽ���ߣ����ǻ�����������ʱ��ϳ������������ͨ����ע����TGF-�µ�cD
NA���Լ�����������ϸ�����յ��Ĺؽ��IJ����ԡ����������ע�����IL-10��cD
NAҲ��������
��ԭ�յ��Ĺؽ��ס�
�Ѿ��ڶ���ģ����������Ŀ��ؽ��������У�IL-1Ra��s������������-R��TGF-��1��vIL-10��sIL-1R��FasL��IL-13��IL-4���ڽ�����RA��Ĥϸ������������ϸ����ֲ��SCIDС���ģ���з��֣���Ĥϸ��ʹ�����˱������ֻ��ƣ�һ���ǻ�Ĥϸ��ֱ����ʴ����һ���ǻ�Ĥϸ����������ϸ���鵼�������ܽ⡣ʹ�÷�ת¼������IL-1Ra��cD
NA�������У�������������ϸ���鵼�������ܽ⣬��Ӱ�컬Ĥ����ʴ������IL-10��vIL-10�����뽫���ƻ�Ĥϸ�������ǵ���ʴ����Ӱ������ϸ���鵼�������ܽ⡣
��1996�꣬FDA���˵�1���������Ƶ������о����μ��о��Ķ���Ϊ9������RA�ľ�����Ů�����Ƕ�����������MCP�ؽڵ�ȫ�ؽ��û���������1�����������ǹؽ��еõ����ԵĻ�Ĥ��֯��������ȡ������άϸ������������������Щϸ�����ֳ����飬һ�鱻��ת��IL-1Ra cD
NA����һ�鱣��ԭ�����ھ�����ȫ���Ժֱ���Щϸ��ע�䵽ԭ�Ȼ��ߵ�MCP�ؽ��ڣ�ÿ�����߶���2���ؽ�ע�䴦�����ij���άϸ��������2���ؽ�ע��û�б�ת��ij���άϸ����1�ܺ�ƻ��еĵ�2�������ֱ�ȡ���ؽ��ڵĻ�Ĥ��֯�����������������Ĥ��֯�гɹ��ؽ����˻���ת�ƺͱ���ڹؽ��ڻ���IJ����������ѧ���ԡ����������ʱ��̣ܶ��ٴ��ϲ�û�в����ؽ���֢״�ĸ��ơ�
����Ŀǰ���õ���ʵ������RA�Ļ����������Ź�����ǰ��������ʵ�鼼���Ľ������ڲ��õĽ������������ٴ���
(2)��Ѫ��ϸ����ֲ���ƣ�����RA��һ����������������ij�̶ֳ��ϣ������Ա��������ڶ����ܰ���ֳ�Լ��������Լ����ı�־�ǣ�ɥʧ�������ơ�ԭ������ͻ��Ϳ�¡��ֳ��������RA���ߵĻ�Ĥϸ���еij���ά��ϸ�������������������ֳ������������Ϊ�������ǵ��ƻ���ϸ�������������ƵĿ��ܻ�����ԭ�������ͻ�䡣��RA�������۹ؽڵĻ�Ĥϸ���п��Է���p53ԭ�������ͻ�䡣B�ܰ�ϸ��������Tϸ�������ƫ��(skewing)��ʾ����RA���۹ؽڻ�Ĥ����Bϸ����Tϸ���Ŀ�¡������RA�Ͷ��Լ���һ����Ҳ�ܴ������ص��²к���ʹ������Ԥ���������������ϵ�ԭ��������������ѪҺϵͳ������������Ѫ��ϸ����ֲ(hemopoietic stem cell transplantation��HSCT)��Ȼ�����������������RA��
�ڶ������ϰ���ƶѪ�Ļ���ʹ��������Ѫ��ϸ����ֲ(allo-HSCT)���ƺ��֣���Щ�ϲ�RA�IJ�����RA֢״Ҳ�õ��˻��⡣һ����8�������ϰ���ƶѪ�ϲ�RA�Ļ��ߣ���������ֲ�õ��˻��⣬��3���ֱ�����ֲ��58�졢75���93�����GVHD��������1����2���RA֢״������1�����ⳬ��2�꣬1�����ⳬ��6�꣬1�����ⳬ��8�꣬1��������ᣬȻ���黺�ⳬ��11�꣬��ֲ�ɹ��ߵ������ڶ���10�����ϡ�Allo-HIST�Ļ���ԭ���Ǹı�����Լ����Ļ������ԣ��ṩ���������ֲ���Բ�����ֲ���������ЧӦ(graft versus autoimmunity��GVA)����ˣ���������������Ȼ����RA�IJ���ʹ�ù������Ѫ��ϸ�������������Ը�ϸ�����Է�ֹ�����ķ������ɻ���ϸ���鵼��GVAЧӦ���������ڳ���Ĺ����ܰ�ϸ��������������Ӧ��ϸ�������������ں��յ��������ٴ�������ЧӦ�������������������������GVAЧӦ������ģ�allo-HSCT�������Ķ����ǹ���ϸ��������������֯�����߷�Ӧ������ֲ�������Ӧ(graft-versus-host disease��GVHD)����������Ѫ��ϸ����ֲ��ȣ�allo-HSCT���нϸߵķ�����(morbidity)�Ͳ�����(mortality)����Ҫ��GVHD�йء���һ���棬�����������ʹ�ñȽϰ�ȫ�ķǹ�������Ը�ϸ����ֲ(non-myeloablative stem cell transplant)����Σ�յĹ��������Ԥ����(myeloablative conditioning)������ν����������ֲ(mini-allografting)�����磬��Ԥ����ʱʹ�û���������fludarabine�ȡ��Ѿ�֤ʵ��ͨ���������ƶ����ǹ��������Ԥ����Ҳ���Գ�ֶ�Ѹ�ٵ���ɹ�����Ѫ��ϸ���ļ�(ingraftment)������������Ѫ��ϸ������Ӧ����������ͼ���������ֲ������صĶ��ԺͲ����ʡ���GVHD��Ȼ��Ӱ��allo-HSCT��ȫ�Ե���Ҫ�ϰ�����������ֲ����ܰ����(CD34 ����)������������GVHD��Σ���ԣ���ͬʱ��ֲʧ�������ӡ���ֲ�ɹ������Ԥ�����Ļ���ǿ�ȡ�����Ĺ����ϸ����Ŀ�ʹ�ʹ�ӵ�Tϸ����Ŀ��Ӱ�졣Ŀǰ��Ϊ��allo-HSCT����RA��˵��һ�ֿ�����(curative)�ķ�����������ȱ���dz�������Է����ʺͲ����ʽϸߡ���ô��Ƴ�һ�ַ������Խ������ʺͲ����ʼ��ٵ���С����Ҫ�����һ�����⡣
ALAN TYNDALLͳ�ƣ���2001��5��Ϊֹ��EBMT/EULAR���ݿ���ʹ����������Ѫ��ϸ����ֲ(auto-PBSCT)�������������Լ����Ĺ�350��������RA 43������43���У���ȥ1����Աʧ�ܣ��������������ֲ����ֲ��1���������õ���õ���39����ƽ�����ʱ��Ϊ11���¡�����13����ת��1�������ȶ���18����������ת��10���º�֢״������7��������auto-PBSCT�Ļ����У�һ��ʹ�û������� G-CSF��Ա����һ�����ʹ��G-CSF��Ա�������ڶ�Ա�ڼ䲡�����ᵽ�жȵĻ�����������ơ�����Ԥ����ʱ��ʹ�û�������200mg/kg����3�������˿�������(ATG)������2��ʹ��
������(busulfan) ����������1��ʹ��fludarabine ATG����������������
������ ���������飬�����IJ����д�ʹ�õ���DMARDs(�װ����ʡ�CsA����������)���ܵõ����õķ�Ӧ��������ֲǰ����Ч�������ܴﵽ��һ��˵�������߶�auto-PBSCT�ij��������ԽϺã���ֲ����Բ����ʽϵ͡���ֲ��֢״���̾Ϳ��Ի��⣬���߹ؽ�ʹ��ʧ�����Ŧ�ۺ���ͷ���ճ�����������ܿ�ָ��������������⣬���ʪ�����ʧ��ESR�ָ����������ʪ������ʧ�������о��������ƺ�֢״������������(�ﵽACR50��70)������ȫ���ⲻ�Ǻܳ�����������һ�����ϵĻ�����2���ڸ�������ֲ��֢״�����ʱ���ƺ���Ԥ������ǿ���й�ϵ���Ա����鷢�֣�ʹ�û������� 100mg/kg�Ļ��߷�Ӧ����ʱ����1��2���£���ʹ�û������� 200mg/kg�߷�Ӧʱ�䳤��18��20���¡�����ʾʹ�ø�ǿ��Ԥ�����������ܴ�����ֲ�����ʱ��Ļ��⣬����ֲ����Բ�����Ҳ���ܻ���֮���ӡ�������Щ�����Ļ��ߣ�ʹ����ֲǰЧ��Ƿ�ѵ�DMARDs����ܻ��֢״�Ŀ��ƣ����ҿ������ýϳ�ʱ�䡣���������auto-PBSCT����һ�������ķ����������ԶԲ��̲������ߵ������ã����ҿ��Գ����ϳ���ʱ�䡣
ѡ��ʲô���IJ��˽���HSCT��û���ϸ�Ĺ涨���ӷ�ʪ���ĽǶ�������������IJ���Ӧ�þ������漸���ص㣺������չ�����صIJ�̬���������ڶԴ�ͳ��ҩ��������Ч��Ԥ�Ƶ���Ч���۴��ڲ������ڣ�û�г��ֲ����������������֤�ݱ������κ��Ѿ����ڵĹؽ���֯�ƻ�Ϊ�����ԡ�����RA���ٴ����̺���Ԥ�ƣ��Ծ���IJ��˶��ԣ��ڲ�������ȷ������Ԥ��dz����ѡ�����ķ������ۺ��ٴ��������ʵ���ұ����������Ԥ���Ļ��ߡ�������֪���Ǿ���DR��1���ͱ����Ļ����������ǹؽ��ƻ�����ҩ�����Ƶķ�ӦҲ��Խϲ�����ַ�����δӦ�����ٴ���Ŀǰһ���������ѵľ����ǣ�����ϣ������ֲ���û���Ļ�������Щ���ڲ������ڵģ������ڽ���HSCT�����ȶ�������Щ���̽�չѸ�ٺͲ������ϣ����С�Ļ��ߡ���ͬHSCT���ƶ�����������������һ���������ߵ�ѡ���������Щ���������Ҵ�ͳ���Ʒ���ʧ�ܵIJ������ϣ�����ͬ��Ҳ�����Ʒ�Ӧ���Ѷ��Ҹ����þ���ΪHSCT����RA�д��������Σ�Ŀǰ����ѡ��ı�Ҳֻ�Ǹ��Ҿ���̸֮������Ҫ�����Ĺ���ʹ֮��������(��39)��
10.��ҽ����
(1)��֤���Σ������ٴ��ϴ��·�Ϊ��ںͻ����ڡ���ڶ��Լ��Է��������Ի����������ʽ���֡���λ�ڱ���֢״������аʵΪ���������ڼ����ȶ�״̬����Ծ�ֹ�Ρ���λ����ٴ�������Ϊ��������а�������Է����������ƺ�ת�뻺���ڣ���������ȶ�����ؽ��ѱ��Σ���ʹ���ף����Ȳ������ԡ��ٴ��г��������뻺�⽻����֣�����������أ�������ʵ���������ȴ��ӣ�����֤��ҩ�������ѡ�
���ݱ��������ʵ����ʵ���ӵIJ����ص㣬���ڡ�������аʵΪ������аʱ�ֱ��������ɢ����������ʪ��������Ѫ�ȷ�������аʵ���鲢�������Ա걾��ˣ�������а���ֱ�ѡ�õ���������������Ѫ����Ƣ��θ�ȷ���
�����飺
A.��Ѫ����
��֢���������ݣ��ؽڱ��Σ�����ή�����ǽڷ��ۣ���Ӳ���ؽڹ���4���������м����������
���������ϥ����������ѣ�Ρ��ļ¡����̡�ָ���ף���ϸ������̦�����൭�������൭�졣
�η��������������Ѫ��
��ҩ��ʮȫ�����϶���������Ӽ���
����15g������10g��ɣ����30g����ܴ10g������10g��ϸ��5g������10g����ҩ10g����ܺ10g���ػ�10g������15g��ţϥ15g������15g������15g������10g�����3g���ʲ�5g��
����������ʮȫ����������Ѫ�Է����������ܴ���������ʪֹ��ʹ�����Զ��١�ţϥ��ɣ�������ܲ�������׳��Ѫ����֮Դ���ֿ�׳����Գ���ԣ�ϸ����ɢ�纮��ͨ�����硣��ҩ���ù���������Ѫ��������а֮����
�Ӽ���ƫ��Ѫ���ߣ��ʸɶ�����ʧ�߶��Σ����������ȣ�ȧ�죬��
�������֮��ƫ�����ߣ����۰ף����ף�η��ϲ�£����㲻�£���
�ҹ�����֮���������Ӱ��ӡ����ǣ����Ƥ�����ؽ���ʹ���ߣ�����ʯ�Ҷ����ȧ�ݡ����������̶��١����ȡ���ȸ����ҩ��ѡ��Ӧ�á����ڲ����վã��Dz�ľ֮Ʒ������Ч������Ѫ������֮�������ߡ������ߡ����ߵ���A���������อ֮�ط�Ҫҩ������������֮��ҩ���Կ�����ѡ�á�
B.�������飺
��֢���ؽ���ʹ���ڷ�������֮�ؽھ��β������ֲ�������ȵ����Ⱥ��ף���ʹ����ҹ�����ԣ��������Թؽھֲ�֢״��ͬʱ��ͷ��Ŀѣ�������ʸɣ��ķ����������ȣ�ҹ�²�������ϥ��������ϸ�������졣���ͼ���RA�����ڡ�
�η���������������Ѫ��Ѫ������ǡ����ؽڡ�
�ػ�20g�������10g��ɽ����10g�����彺10g(�Ȼ�)��¹�ǽ�10g(�Ȼ�)����˿��30g����ţϥ15g������15g��ɣ����30g������10g��
���������еػơ�����ӡ�ɽ���ǡ����彺�����������DZ��������˿�ӡ�¹�ǽ�������Ѫ����ţϥ��ɣ��������������׳����������Ѫ��Ѫ�������̲�����������衢ǿ׳���֮Ч��
�Ӽ��������̽ϳ���������������ʹ��ֹ�ߣ���Ю�����磬��������30g��
����20g������10g��Ю��ʪ�ߣ����ֹؽ���ʹ�����ţ��ӷ���15g����ܴ15g��������10g��Юʪ������̦���壬�ӳ�����20g��������15g��ľ��10g��������ʪ�ȣ�ͨ��ֹʹ�������������ߣ������ػ�30g����Ů����10g��������15g��
C.�������飺
��֢���ؽ���ʹ�����ͣ�����ҹ�أ����첻������ϥ���������������ʹ��η��ϲů�����㲻�£���ɫ�۰ף��Ժ����ڵ����ʣ�ë���������ף����ɻ����䣬���渡֫�ף���С��Ƶ��������������Ů���¾��������٣����ʵ����ۣ���̦����������������
�η����²����������ʪ��ɢ��ͨ�硣
��ҩ���������Ӽ���
����9g������12g������15g��ϸ��3g����20g��ɽ����12g��ţϥ15g�����6g����ܺ12g������12g������30g������20g��ʯ����12g����9g���ջ�9g������9g������5g��
���������и��Ӵ������ȣ�����ɢ���Ʊ�Ϊ��ҩ�����硢���ϸ���������ɢ����ʪ��ɽ���ǡ�ţϥ�����������������Ϊ��ҩ����ܺ�������Ѫͨ�磬���Ρ��������Dz���������ʯ���ѷ���������ʪͨ�ϣ��ջ�����ͷĿ���������ͨ�磬��Ϊ��ҩ���������·�ɢ��ɢ��ͨ��Ϊʹҩ��
�Ӽ����������ӵ��Ρ������IJݣ���̵ʪ�����ü����ǡ����ӡ����ʣ�����Ѫʹ������桢�����㡢��ûҩ�������������ء�ʯ���ȡ�
D.Ƣ�����飺
��֢���ǽڽ�Ӳ�����첻�����ؽ����䣬η��ϲů�����㲻�£���ϥ�������ڵ����ʣ����渡֫�ף��ɲ�ͣ�С��Ƶ�������ϡ�磬������������Ů�Ӵ�����ϡ���൭�֣���̦����������������
�η����²�Ƣ����ͨ���ñԡ�
��ҩ������ͨ������
����18g������12g���츽��12g�����5g(��ĩ)������15g�����15g��С����10g������15g������12g���gݲ��15g�����2�����˸ʲ�6g��
�������������츽�ӡ�������������Ρ��������������顢�����Ѫ��Ѫ��С���㡢����¾�ͨ�磬����gݲ������ʪ������������ʪ���ʲݵ�����ҩ��ȫ�������²�Ƣ����ͨ���ñ�֮����
��аʵ��
A.�纮ʪ�ԣ�
��֢���ؽھ�ʹ���������죬����ǿֱ�м���ʱ��ʱ�أ��������أ����Ȼ��⣬ÿ����������ء���̦���ף����ҽ���妻���
�η��������ֹʹ����ʪͨ�ԡ�
��ҩ����ͷ�����������Ӽ���
������������Ʒ���������ɢ���бԣ���ͷ�ѷ�ɢ�����¾�ֹʹ����������������ҩ��Ѫ�ԣ��ʲݺ���ҩ����ӷ��ۣ�����Ѫ�������ֹʹ���ֿ�����ͷ����֮�������ʡ�������ʪͨ�ԣ����֡��ʲ�ֹ�μ���ʹ����ܺ���������Ѫ����ͷΪ�������ȵĶ�ҩ����ʼ����ҪС����ҩ������ʱ��������Ӵ�����尾ʱ��Ҫ�����Է��ж���
�Ӽ����ؽ��״�ʪʢ�ߣ������ɢ�������ߣ��ü����ʡ��컨����ɽ�ף���ϴ�
�������ڷ���
B.��ʪ�ȱԣ�
��֢�����ڱ������Ի�ڡ��ؽ���ʹ���ֲ����ȷ��죬��淢�ȣ�������磬�ڿʣ�С��̳࣬��졢̦���ƣ��������������
�η���������ʪ�����ͨ�硣
��ҩ�����ӹ�֦�����á�
��ʯ��15��30g(�ȼ�)��֪ĸ���ưء���֦��������10g������15g�������ǡ��ʲݡ�Ǽ������6g����ͩƤ����Ѫ�ٸ�12g��
C.���ȱԣ�
��֢���ؽں��ף�������ʹ�����ɴ�����������ת�࣬Ƥ�º�ߣ����Ⱥ�ս���ķ����ڿʣ��ѻơ����ɣ���̦�ƣ����һ�������֤��ΪRA���Է����ڱ��֡�
�η������Ƚⶾ����Ѫ����Ѫͨ�ԡ�
��ҩ�������°�����ζ��
�������������Ρ����ء������������ʲݡ�
ë������������������Ƚⶾ����Ѫֹʹ֮�������顢���֡�ţϥ�л�Ѫ����֮����������ҩ�����ʪ�����������нϺõ�Ч�����ټ��������ʡ����ٲݳ�ʪ���ؽ���������ֹʹ���ָ��ؽڻ֮����
D.���ȴ���֤��
��֢������ڱ������������ȶ��ڹ��ɽΣ��ؽ���ʹ��ؽ�������ʹ�����ʵ��죬��̦����ƣ���������
�η�������ɢ����ͨ�����硣
��ҩ����֦��ҩ֪ĸ���Ӽ���
��֦����ơ��Ƹ��Ӹ�6g������֡����������硢֪ĸ�����϶���12g��ȫЫ4.5g�������㡢��ûҩ����ľ��10g��
��̵����
A.̵�����
��֢���ؽ���ʹ�ұ��Σ��ʱʹ���������ޣ������ʹ��ʹ�����ƣ�Ƥ��ʧȥ���ԣ���֮��Ӳ��������������ɫ��ڣ�����Ƥ�½�ڣ���֫�����飬�������ף����ʰ���������ߡ����㣬��̦���ף�����ɬ��
�η�����Ѫ��������̵���͡�
����10g����ܴ10g������10g���컨10g���㸽10g������10g������֬10g��ûҩ10g��Ǽ��15g����ܺ10g��ţϥ30g���ʲ�5g���ư���10g����10g��
�Ӽ������Ѫ���ס��������ߣ��������°���(Ԫ�Ρ������������顢�ʲ�)�����Ƚⶾ����Ѫ������������ר��ʹ��������㡢�Ӻ������ر�档���������ߣ���Ϊ�ܰͻ�����������ݭ������
ָ������������ˮ�Ρ���������
B.��Ѫ���飬̵�����
��֢�����ڱ������ڹؽڽ�Ӳ���νΡ��ؽ���ʹ�����ͱ��Σ����������ɫ�۰ף��ļ����̣���ƣ���룬���ʵ��죬��̦�ף�����ϸ�ҽ���
�η���������Ѫ����̵������ͨ�����硣
��ҩ��������ʹ���Ӽ���
���顢���������Ρ��������ɸ����10g�����Ρ����ߡ���к�����ߡ�
������12g��Ǽ�
���������顢�����6g����֦���ʲݸ�4.5g��
C.��������̵�����
��֢�����ڱ������ڣ��ر��dz���ʹ�ü�����ҩ��Ļ��ߣ��ؽ���ʹ�����Σ��������ݣ����첻������ϥ�������ؽھֲ����ȣ�ͷ�ζ�����ʧ�ߵ��������ʺ죬��̦����ϸ����
�η����̲�������������Ѫ���ѷ�ͨ�硣
��ҩ����ζ�����Ӽ���
��ζ�ӡ��Ƹ��顢���ơ�������6g������졢ɽ���⡢��ء������١�����Ƣ����ë������12g��ţϥ�����θ�10g�����ߡ��䷿��4.5g��
�Ӽ�����аƫʤ�ļ���ܴ�������ɣ����÷��磻��аƫʢ��ϸ������ƣ�ʪаƫʢ�ӷ�������ɳ�����Ƥ����Ѫ��������ڡ����Σ���аƫ�ؼ���ʯ�ࡢ�����ߡ�
��ҽ֤����һ����̬�Ĺ��̣�һ��֤�Ϳ��Գ��ֲ��̵IJ�ͬ�ڣ���Ȼ�������鼰�������������к��ڣ����ڼ��Է���ʱ�ֿ����ȶ���ʪΪͻ�����֣�����ʵ��У���ˣ�������֤�ͣ�����һ�ɲ��䣬����һ��֤���ڲ�ͬʱ�ڿ��Լ���������֢����Ѫ��̵�裬�����ٴ���֤ʩ��ʱӦ���ݵ�ʱ���������֤��ҩ��
(2)�ۺ����ƣ�
�ڵ��鷽��
A.������90g��ˮ�������3��ͣ3�졣�ιؽں�����ʹ����Ѫ���������ϡ�⣬�������á�
B.���ȸ�250g��ϴ�����飬����0.75kg���ݰ��º�ÿ��20ml��2��/d��
C.15%��������ÿ��10��15ml��3��/d���������������ߣ���ȥƤ������ҩ20g��ˮ��2h������ڷ���
D.�����ҩ�����������500��600g��ţϥ60��90g���ʲ�60��90g����������60g������10�����Ƚ�������ȥ�ǣ�����ҩ�����Ļ�6��6ҹ�������ױ�ڣ������ڼ��ɡ�ÿ���緹������1ֻ����10��Ϊ1���Ƴ̡��Ƴ̼��7�죬���߷�3��4���Ƴ̣����߷���9���Ƴ̡�
������Ʒ���
A.���룺��֤ȡѨ���б�ȡ���ᡢ���š�Ѫ����ʹ��ȡ���ᡢ��Ԫ���ű�ȡƢ�ᡢ����Ȫ���������������ȱ�ȡ�������ء��Ϲȡ����ء��ֲ�ȡѨ���粿ȡ���ǡ����s�����ء���أ��ⲿȡ���ء������������ء��Ϲȣ��Ų�ȡ�������ȱߡ����s��ί�С����С�����Ȫ��ϥ��ȡ���𡢶��ǡ�ϥ�ۡ���������Ȫ��������ײ�ȡ���ӡ��������պ������ء����档������ƽ��ƽк������̵���������30min��1��2��1�Ρ����ʵ����õ�Ƶ�������10min��
B.�ķ���ȡ����Ѩ(����ֲ�)���������ǡ����ء��Ϲȡ����С�����������������ǡ������������ء����ᡢ������������ÿ��ѡ4��6Ѩ��ʩ�����º;ģ�ÿѨʩ��10��20min��1��2��/d��
C.��Ѫ��������ʹ��λ��������ѭ�У��ھֲ�ȡ1��2������Ѩ�Ͳ���ֲ���Χ��������������Ѩ��ɢ�̷�Ѫ��������ֲ���Χ����Χ�̷�Ѫ������÷������ߵ��(ߵ�̷�Χ�Դ��ڻ��)��Ƥ����Ѫ�����������̷�Ѫ�����ιޡ��ؽ���������������ʹ���߹�������1�Σ�5��Ϊ1���Ƴ̡�
D.Ƥ���룺����Ѩ(ѹʹ��)�����۹ؽ���Χ���й�Ѩλ�����ش̷��������䲿λȡѨʩ�Σ���ϥ�ؽ���ʹ����ѡȡ������θ������̫��Ƣ��ߵ���Ժ����ص�ߵ�����𡢶��ǡ�����Ȫ��ϥ���غͰ���Ѩ��������һ��ѭ��ߵ���ؾ���ѭ�У���֫��Զ������ˣ����ɽ�����Զ��ߵ�����Ƥ���Ͽɳ��ֺ;�������һ�µĺ���(Ƥ��С��Ѫ��)�������ص�Ѩλߵ���ص�ߵ�����۹ؽ���Χ��Ѩλ������ѨΪ��ʹ���ػ����еIJ�λ��ÿ��ߵ��1�Ρ��Ƴ��벡�̾����йء�
E.���룺��ȡ����ؽھֲ���Ѩλ�Ͱ���ѨΪ�������ɸ��ݾ����֤��ѭ��ȡѨ�����������ֲ������̶ֹ�Ѩλ��˳�ֳ��룬���ٴ���Ƥ�£��ټ�ѹ���뵽�������Ƚ��е�����������ɽ⡢���룬ͬʱ��湳���й��ɵ�ǰ�����˶�����ǣ������ճ��������֯��Ҳ���Ӳ��������Χ��ǣ�������Բ�����ÿ��������2��3�μ��ɣ����ֲ��������ȸС��еȵ�����ʱ���룬��������ѹ�ȷ�ֹ��Ѫ������1�Σ�10��Ϊ1���Ƴ̡�һ����������3���Ƴ��ԺͿ��յ�����Ч����
F.ͷ�룺ȡ�����1/3�����ǰб������б��(�Բ���Ӧ��λ)�����д�����С�������к���������1/3����ǰ���̣����ǰб������б��(�Բ���Ӧ��λ)���ش������̣����д����������´̡�������ʱ��������������������������������������������֫�����ࡣÿ������3��5min�����15min������1�Σ�����2��4h��1��/d��7��10��Ϊ1���Ƴ̡��ٴ������硢ʪ�������ߣ��ɲ������ƴ��ķ��밴Ħ����ͷƤ��Ա�����һ����Ч����RA�ļ��Ի��Ӧ�ʵ������˶���������̫�����ڼ��ң��ڻ����ڼ�ƽʱ�����ڼ��˼��֫����������֫��Ļָ���������RA���ɸ�������1�Σ����ɼ��þķ�����������Ƴ̡�
���⣬���ж��롢��Ѫ��ˮ�뵶�����ߡ�������Ʒ���
�������Ʒ��������Ժ�Ӫͨ�硢�����ؽ�Ϊԭ���ڹ���ǿֱ�������ͨ�磬��ѪֹʹΪԭ��
A.��֫����a.�������ƣ�ҽ��վ��һ�࣬һ�Ųȵ��ϣ�����֫���ڴ����ϣ���
�����ֱ��ڡ����ʩ�Σ������粿������������ͬʱ�ʵ���ϸ��ؽڵı������b.�����ƣ��Ӽ粿���������������÷����ص��ڼ硢�⡢����ϰ�����ǡ����ꡢ���s�����ء�����������Ϲȡ����ء����ꡣc.�������ƣ�ҽ������ǰ�ࡣ������������ָ��ָ��ؽڣ�ͬʱ����ʶȵ�ҡ����Ȼ����ҡ�硢��ؽڣ�����֫4��5�Ρ�
B.��֫����a.���߸���λ��ҽ��վ���ԡ���
��ʩ���β���������С�Ⱥ�ࡣ�š�ϥ���ؽں������ص����ƣ�ͬʱ����ź��졢��չ��ϥ�ؽڵ������������Ȼ���������s��ί�С���ɽ��b.��������λ��ҽ��վ���ԣ����÷�ʩ�ڴ���ǰ��������࣬������С����࣬������Ȫ��������Ѩ���µ��ײ���ͬʱ����Źؽڵ���չ�������������c.�����ơ���ϥ�ؽ���Χ��
�����ƣ�ͬʱ��ϰ���ϥ�ۡ�d.�����ơ����ؽ���Χ���㱳��
�����ƣ�ͬʱ����ؽ����켰�ڡ��ⷭ�������ҡ��ֺ��ҡ�ؽڡ�Ȼ����ί�У���С�Ⱥ�����µ�����4��5�Ρ�������֫���Ӵ��ȵ�С�ȡ�������֫����֫��������صĹؽڣ����ɼ��ò������ȷ������Ч��һ��������
��������ͳ�Ʒ���ɰԡ������ɰ��ʪ�ࡢ���������ҩ��������ȡ�
(3)���Ʒ���ʵʩ��ĿǰRA������������ҩ�����ҩ����ڲ�ͬ���������Ч�����ң�����ҩ������ƻ����ͬ���ʶ�һ�������RA���ߣ�������������ҩ���ơ���ҽ���й�����������������������ν��̨��ʽ��������������ʹҩ��������Ч����һ�Ӹı䲡��Ŀ���ʪҩ������Ƽ�����ù������Ч�ټ�ϸ����ҩ����������Ƥ�ʼ��ء����ַ�ʽ�����ȱ����ʹ��������ʹҩ������Ч�ߣ������ѱ��ƻ������øı䲡��ҩ�������ɵ��ƻ������ָ�����һ��Ϊ��̨��ʽ���������϶���ҩ���Ժ��ֱ�ͣ�ã�������һ���ָ�������С��ҩ��ά�֡�����Щ�����������������ۣ�ĿǰҲ��û��������ģʽ��
������ʪ��ѧ������Ȩ������־���ؽ������ʪ�����Ϸ�����2002�����������ʪ�ؽ�������ָ�ϣ�ָ����ѭ֤ҽѧ֤ʵ�����ⲡ��Ŀ���ʪҩ�ܸ��Ʋ��鲢�ӻ��ǹؽ��ƻ�(��Ӱ��ѧ֤ʵ)������κ�ȷ��Ϊ���ʪ�ؽ��Ļ��ߣ�������н����Թؽ���ʹ�����Գ�����ƣ�͡���Ի�Ĥ�ס�Ѫ����C-��Ӧ����ˮƽ��������Ӱ��ѧ֤ʵ�йǹؽ��ƻ�������ʹ�÷��������ҩ�Ƿ��ܳ�ֻ���֢״����Ӧ��ȷ���3����֮��Ӧ��ʼӦ�û��ⲡ��Ŀ���ʪҩ���ơ����õİ���
���������������ड��װ����ʡ����������Լ�����������������
����������infliximab������ʹ�õ����������ʡ���ù�������Ρ���ŵ�����Լ������ء��µ�����ָ���Ƽ����ⲡ��Ŀ���ʪҩ�������ƣ������Ǽװ����ʼ���������़�
��������������������е����������Լ������Ƽ�����������������������ǰ�������á��ڷ�С������Ƥ�ʼ���(С��10mg/d�����Ч����������ҩ��)���Լ��ֲ�ע����Ƥ�ʼ��أ����ڲ��������ʪ�ؽ�������֢״�dz���Ч���½����о�֤�ݱ�����С������Ƥ�ʼ����ܼ����ؽ��ƻ��Ľ��ȣ������Ƥ�ʼ��ؾ��л��ⲡ���DZ�ܡ�Ȼ����ȫ��ʹ��С������Ƥ�ʼ��ص�ͬʱ������ʱ��Ȩ���丱���á�������Ƥ�ʼ������ƵĻ���Ӧ�����(1500mg/d��������ʳ���Ƽ�)��ά����D(400��800U/d)���ƣ�Ӧ����Ƥ�ʼ������ƿ�ʼʱ���衣���⣬���������ƹ�ϸ��ҩ�������Ƕ��������Ƽ���������ֹ�Ƕ�ʧ�����ھ�����Ů��ͬʱ����Ƽ���������ơ�������ʹ�����ܣ��ؽڻ��Χ�����Լ���ؽڽṹ�ƻ����µĹ��������Կ����������ơ����ʪ�ؽ���������ư����ܼ�ѹ������Ĥ�г���ֺ(ָ)ժ�������ؽڳ������Լ��ؽ��ںϵȡ�
�����ҹ�������ɿ�������ҩ���ϵķ���������������ҽ���ƵĻ����ϣ��ٸ�����ҽ��֤���ۺ����ƣ������ʵ��ķ�������������ǿ��Ч�����ٸ����õ�Ч�����ȶ��ڲ��ˣ�������ҽ��֤ʩ������ʹ�øı䲡�����ҩ���������ҽҩ��֤���ơ�
��ս�Ը߶ȿ��ǣ��������ʪ�ؽ��ף����봦���á��αꡱ�롰�α����Ĺ�ϵ�����αꡱ��ֹʹ�����α��������ڻ������߹��ܡ������������ʹ�Ľ�����������࣬������ЧѸ�٣�����������ʹ���ܽϺõĽ��������ֹʹҩ��ͷ��������ʪ�ؽ���ֻ����ʱ������ʹ֢״����ͣ������ʹ֢״���֣�������ʹ��ֹʹҩ�������忹��ҩ�����صȣ�������θ�������ˡ��������ˡ���Ѫ�������Ƶȸ����ã���Щ��������ʱ��ԭ�������أ�����Ӱ�����彡�������ԣ���������ʹ�ܹ����ܵ�����£�Ӧ����������ֹʹ�����������߹��ܵĵ�����Ŀǰ�����û���ҵ�һ��ҩ������ڽ϶�ʱ����ʹ���ҵĻ������߹��ָܻ�������״̬����������ʪ�ؽ��������鵤��ҩ�����ݡ����ǣ��ڳ��ڵ��ٴ�ʵ�������ڵ��о��У������Ѿ������˲����ܶԻ�������߹��ܷ������ô̼����õ�ҩ�������(������Щҩ������ض���ÿ������˵���Ǻ㶨�ġ���һ��)����ʹ���ҵ����߹����ָ���������ӽ���������ƣ�����ҽҩ��֤���Ρ���ġ����õľ���״̬��������г�Ļ��������˵��˶���ʳ��ȡ����е���ҽҩ��֤���ν�Ϊ��Ҫ���Ѿ��������ѧ�߽��ܣ����γ��˹�ʶ����Ϊ������Ч��ȷ�У����Ҹ�����С�������á�������Ҫǿ�����㣺һ����ҽҩ�����֤���Σ���������һ��һҩ�����������ʪ���ˣ�������ҩ�Ѽ��ѳԣ����ʺ��ִ��˳��ڷ��ã��������ֱ���ϳ��ڷ�ҩ�����ԣ����������Ϊ�ִ����õļ��͡�ʵ��֤���������ԡ��α���Ϊ���桰�αꡱ�ķ���������ҽ��ϣ��ۺ����ƣ��������ʪ�ؽ���Ԥ���DZȽϺõġ�
10.����
(1)�������⣺��ʹ�����ͣ��ؽڱ��Σ�Ƥ�������������ʣ�������뵡��
(2)����Ŀ�꣺ֹʹ�����Ს��ʹ�ࣻ��֫�а��֧�߹̶����Է�ֹ�����ؽڻ��κͲ�������λ����ǿӪ���������ֿ���������������������������뿵������ǿ���ܶ��������ֹؽڻ���ܡ�
(3)������ʩ��
����Ϣ��Ӫ��������������ϵ���Ϣ��RA�������Ƶ�һ���֡���������Ҫ����Ϣ�����Ӳ����������ȫ����ؽھ����ַ�ʱ��Ҫ��ȫ�Դ���Ϣ���������ɶԿ���֢�������óе������Ĺؽ���Ϣ���������IJ��ˣ���ÿ��ϳ�������2��4h����Ϣʱ�伴�ɡ���������ʳ���䣬�Լ����������������á�Ӧ���ݲ��˵����������Լ��������ص㣬�����ʺ��ڲ��˵���ʳ������������ʳ����ʳ�˸����Ӫ�����ߺ�ά���ء��ơ����������ʵ�ʳ�Ӧ�����������־��Ⲣ����Ӫ���������䡢���塢����֮�
������������������ԱӦʹ���˺�������˽�ò��IJ��鼰���̣����������ں��������ܷ�Χ�ڼ���������ͬʱҲӦ������ؽں���ʹ��Ԥ���ؽڱ��εķ����̸����˺ͼ�����ʹ�����ʵ���ʹ������ֹʹ�����а塢�������Ƶȿ��Ʋ��顣�Բ���һʱ���ܿ��ơ��������ꡢ�������С���Ҫ���ġ���ο�IJ��ˣ�Ӧ˵���������з�����������������ֻ֮�м�ʱ���ƣ�����ʹ������Կ��ơ����߱������õ����������ƾ��л������壬�������������״̬������ơ�
������������ڼ�����Ӱ�죬�����ߴ������㣬��Ҫ������ָ����ÿ������£���ʱ���ɺ�Һ���ڻ�������ִ�����������ϴ�Ż�ϴ�裬��ʹѪ��ͨ������֫�幦��ɥʧ�Դ������ߣ�Ҫ��ֹѹ�������������ع����ϰ��ߣ�������ʳ��ӵĻ�������ֹ���͡����۵ķ���������ͻȻ���ƶ����ء���ʹ����ʱ������Ħ�ؽ����Եļ��⣬�Լ��ἡ�⾷�ζ�����ؽ���ʹ��
(4)�ʵ�������������Ԥ�����η�����
�ٲ��˵����ƣ�A.�Դ���Ϣʱ����Ҫ����ͷ���ڲ���ϥ�£����Ҳ�Ӧ�ò��˳�ʱ��ά����̧��ͷ����ϥ�������ƣ���Ԥ�����˷���������ϥ���Źؽڵ������������������ʱ��Ӧ������ƽ�ɣ��������ַ��ؽ���չ�����ƣ�ͨ���������µ�һС��ͷ��ʹϥ��ƽֱ���ֱ۵�����Ӧ�����������ϣ��������»����µ�һС��ͷ���۵���ë������ά����չ�������Բ��ˣ���Ҫʱ���Է���ɰ����Ԥ���Źؽ��ⷭ��B.Ӧ�����������ƣ�ÿ������Ӧ��2��3�θ��ԣ�ÿ��15��30min���Է��Źؽڷ���������������C.��ʱҲ�������üа��֧�߹̶����ַ��Ĺؽڣ�һ�����ʹ��ʹ���ᣬ��һ����Ҳ����Ԥ������ٻ��η�����D.����վ��ʱҲӦά��ֱͦ���ơ�
�ڻ���˶������������������еġ��˶��Ʒ�����
(5)����Ӧ��ҩ���ĿǰΪֹ����û���κ�һ��ҩ���������RA���������ڼ䣬ҽ���Ὺ�����˸��ֲ�ͬ��ҩ�Ӧ���ò����˽⣬��������ܺ�ҽʦ��ͬ������Щҩ��Բ���������Ч�ġ�
(6)����ȵ�Ӧ�ã��������ڹؽڿ�ʹ�ؽ���ʹ����Ӳ�����͵�֢״���ᣬҲ����ʹ������ɡ��������˶�֮ǰ�����ȣ�Ҳ����ʹ�˶�ʩ��������������Ч���ȵ�ʹ��ͨ���ڼ����ڹ����ʩ�С����õ����Ʒ����кܶ࣬���磺���õ��ȵ桢��ˮ����ʯ��ԡ�ͺ����ߵȿɹ������ȣ������ȷ���ԡ����ԡ�Լ�����ԡ�ȣ����ṩʪ�ȡ��ڲ��ֲ��˵Ĺؽ���ʹ���������������û��⣬�ڼ�����Ҳ����ʹ�á��۲���ʹ���Ȼ��䣬��ӦС�ģ�����Ƥ�������ˡ�
(7)������ѵ�����������չˣ���Э������ѧϰ����Ч���ճ����ʽ������������������ڿ����ø��ֲ�ͬ�������չ����ߣ���Э������ά������ȵĶ����ԣ�����ʹ����������ֵ�ʳ�ߡ����������Ӻ�Ь�Ρ�������κ���Ͱ�߶ȵȣ���ʹ���������н�ʳ����ͷ����Ь�ʹ�С��ȡ�������ƣ����һ����֢״�����˶Ի�����������ϵͣ���˶��ڲ��˵������չ˻����ʱ��Ӧ�мƻ���ʹ�������ӣ���Ӧ�������ƣ�С�
(8)��Ժָ����RA��һ�����Ե�ȫ���������Լ��������̳��������������ʶԳ�Ժ�ؼ������IJ���Ӧ���ó�Ժָ�����������̹������ٸ�뻼�߶��ڸ��ָ�ȾӦ������Ԥ�������ơ���ע���������ʪ����ð����ˮ������ʪ�¡������ڳ�ʪ������Ļ�������Ϣ��Ԥ���з纮�����ز��顣�ļ�������Ӿ����������ϯ���յ��ȣ������շ��ؽ��ķ���������������ʳ�������䡢���塢����֮Ʒ������ҽ�����й��ܶ������˶�Ҫ�ʵ�����������
�ɶ����п�Ȫԡ���Իָ��ؽڹ��ܡ�����ҽ����ҩ�������ͣҩ����ҩ�������������������︴�顣
11.����
(1)Ŀ����ԭ����������ҪĿ���ǻ�����ʹ���������ף����ֺ��Ƽ������ؽڹ��ܣ�Ԥ�����������μ�������������������
Ϊ������Ȼָ����߹��ܣ��ﵽ���ܵĿ��������Ʊ�������Ʒ�������һ����ע��ȫ��Ӫ����ҩ����������ƣ���һ����ע���ֹ�ͽ������Σ���ǿ���ܶ�����������������ƺ��ٽ��и��ƹ��ܵ����ƣ��������������Ƽƻ�����ͬ���ڲ��ò�ͬ���Ƽ�������ʩ�����Ի�������������й����̣�������������ģ�ȡ�����ǵĺ���������������Ч����
(2)������
��ҩ�����ƣ��������ơ����֡�
��������ƺ���λ��������ʹ�������������¹ؽ�ǿֱ�����Ҫע�Ᵽ��������ƺ���λ���Դ�����Ӳ�崲����ͷ�˵ͻ��ã�����λʱ��֫ȡ����λ�����ȱ�������λ����λʱ����ƽ�忿���Σ�����ֱͦ�����α��ϣ�������ƽ���ڵ��档
�۶���ƽ�⣺�������˶����ȶ���ɲ���Ҫ�����ģ�������ʹ���ֲ�����ȫ��ֹ�����¼���ή���ؽ����������������Դ���Ϣ�������˳���3�ܡ��Դ��ڼ侭���任��λ��ÿ��ȡ����λ1��2h��ʹ�������֫���ܵõ���չ����������������ķι��ܡ��ؽھֲ����üа��������ƶ���
(3)�˶��Ʒ���
��ˮ���˶��Ʒ���ʹ�������ø����ڲ�����״̬�½��в���ѵ��������ˮ�������ɶ�������������ˮ�б任�˶������ٶȣ��ɸı��˶���ʽ��ˮ���˶�һ�������ü��ؽ����˷�����
�ڹؽڻ��ѵ�������������ɷ�ֹ���������Ρ�Ԥ����ή�������ֻ��߹���״̬���ճ��������ܡ�A.�����ڻ��ߵ���ؽ�Ӧ�ý�����������֧�̶ܹ�����ʱ��жװ�߽��������������Ҫ��ֹ���εļ��ء�B.���Եȳ���ϰ��������ϰ������ѵ��������ʹ��Χ�ڽ��С�C.ÿ���ؽڵĻӦ�ﵽ���ޣ�ÿ��ѵ��ʱҪ�ﵽ�ؽ�ȫ��Χ�˶���ÿ������1�Σ�����Ӧ������ʹ�Ӿ硣D.һ����ÿ��1��2h���ж�ʱ�����ϰ(5min�����)Ϊ�ˣ�Ч����һ�㳣��ϳ�ʱ����ϰ���á�E.�˶��Ʒ�ǰӦ�������ƣ�����ˮԡ�����������ơ�F.���볤�����ġ�ѭ������ϰ������ȡ��Ч����G.����ǽ̻Ỽ��һ������ɻ��ڱ��˰�������ɵļ�ͥ���Ƽƻ������ڸ��鲢����Ҫ���ġ�
(4)�������ƣ�
�������Ʒ��������ÿ���ʹ�����������Σ���������֯��չ�Լ�����ëϸѪ��ͨ�ԡ������ڡ��з��Ȳ���ʹ�á����������¡�A.ȫ�����ȣ���ʪ����������Ȫ�Ʒ�������ԡ��ɰԡ�����Ƶȣ���Ȫԡ�����ܻ���ӭ���Ʒ���B.�ֲ������Ʒ������ȴ�����ԡ�����ơ������ߡ���Ƶ���Ʒ�(Ŀǰ�౻������)����ȫ��Ӱ���С��C.�������ף��Ի��߽�������ʱ�������¶ȿɴ�40�棬ÿ��30min��2��/d���ɼ�����ʹ��
��ˮ�Ʒ������ÿ�Ȫԡ����ˮԡ������ԡ�ȡ����Ի�ڲ��˼������߲�����ȫ��ˮ�ơ�
�۵���Ƶ���ƣ��羭Ƥ���̼���(TENs)���䶯���Ʒ������ŵ��Ʒ���������Ƶ���ҵ��Ʒ����кܺõ���ʹ���ã�������ŵ��Ʒ���ʹЧ����ѡ�
���⻯�ɵ��ɳ��������ƣ�֢״�������м��ᣬ�ɽ������ʪ��ԣ������⻯�ɵ��ɶԸ���Ķ��Է�Ӧ��
�����Ʒ������ڼ�����֢�ڣ�����ʹ���ٽ�ѪҺѭ�����������������ס��ӿ�ֲ��³´�л������
��ԭ��ά���ԣ������ڼ�����������ܶ��������ܸ��ƹؽڹ��ܵ����ã�����Щ���߲�Ը���ܴ����Ʒ���
����ҵ���Ƽ��ճ���������ѵ�����ؽڵ���չ�������˶���ÿ�������2��3�Ρ���������һ�������Ȧ��������ָ�ؽڹ��ܣ�������ת����ת��������ؽڹ��ܣ���̤���г�������ϥ�ؽڹ��ܣ���Բľ��̤�շ��һ��������ؽڹ��ܵȵȡ�ÿ�λǰ�ֲ�Ӧ�����ȷ�����������ơ���������ˮ�Ƶȣ�ÿ�λ��Ҫ�ӻ�����ʹ�����̶ܳ������������Ӧ�����ӣ�ѭ������֮�Ժ㡣
���ճ��������������ϲ�Ļ��ߣ������価������ճ�����ѵ�������ʳ��ȡ���ˮ����ˮ����ϴ��šë�����������ºͿ��ӡ���ۡ����س��롢�ֱ����ҡ�����ˮ��ͷ����վ���ƶ����¶ס����С�����¥�ݡ�����ԡ�ص�ѵ����Ϊ�˴ﵽ������������ʱ��Ҫ��װijЩ�����þߵĽṹ���������һЩ�Զ��þߣ���������������������ҵ�Ʒ������ƻ��߹����⣬�������������Ӧ�������Ƕ����Ľ��е�һ���ۺ�ѵ����
��������ͳ�Ʒ�������Ʒ��������Ʒ����ڱ�����ȸ��ص�����½����ʶ���ٺ���������˶ν���̫��ȭ�ȡ�
������а塢�������ȿ�������������֫��Զ�˹ؽڱ��Σ�����ָ�ؽڳ߲�ƫλ��ָ��ؽڵĶ쾱���εȡ���֫�ؽڵ��ⷭ��������Ρ����ø���Ԥ�����ε�֧��(��߷��ӱ�����ʯ��е�)��ǿ������ؽ��켡�������Կ�����֧�ߡ��а塢���ȡ����εȵ�Ӧ���ܼ���ؽڻ��η�չ��������ʹ�����ף���ֹ���ڹؽڲ��ȶ�����һ������ͨ���а���������ָ�ؽڼ�ָ��ؽڡ��̶��а峣���ڼ����ڻ�������Ӧ����ж�����ؽڻ��
�ڼ����ڣ��̶��а�ÿ
�����24h����Բ����Ļ�����Ϊ��Ҫ���������ֹѹ���γɡ���������ƺ���Ӧ���̼а�̶�ʱ�䡣�����ʪ�����ַ��������������ľ�Ȧ��ͷ�̶����м�λ����˯�ߺͻʱ(���Ͻ֡��˳���)��Ϊ��Ҫ�����ؽں��㲿������ʱ���ɲ��ý���Ь�Ա����㣬�������´����
Ϊ�����´������Ӧ�ù��Ȼ������������Ḻ�غı������ߡ���Щ�豸�ɱ���ϰ���Ը����������ˣ�����������֫���۹ؽڵĶ��⸺�ء���ˣ����Ȼ���������Ӧװ�а��֣��Լ��ٶ��֡������粿�ĸ��ء���Щ��ʩҪ��ҽʦ���ݻ���ʵ�������������
������������Ҫʹ��������սʤ���������������ģ��������õ������;���״̬������������ƣ��ﵽ������Ŀ�ġ�
����������������������ѡ���ʵ�ָ���£��Կ��Ʋ��䣬�������Σ����ƹ�������Ҫ���á����õ������л�Ĥ�г������ؽ����������ؽ��ɽ������ع������ؽ��ں������ؽڳ��������˹��ؽ��û����ȡ�



 ���в�ѧ
���в�ѧ
 ����
����
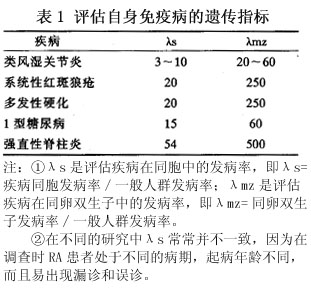
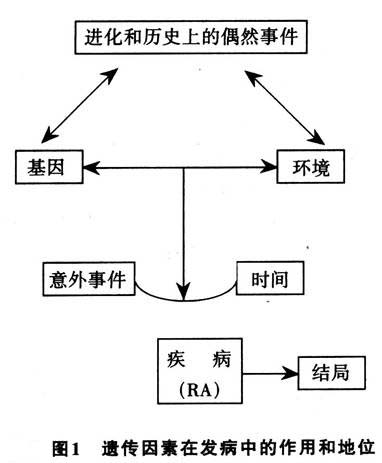
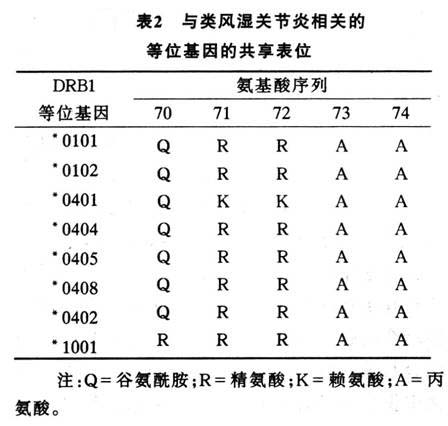

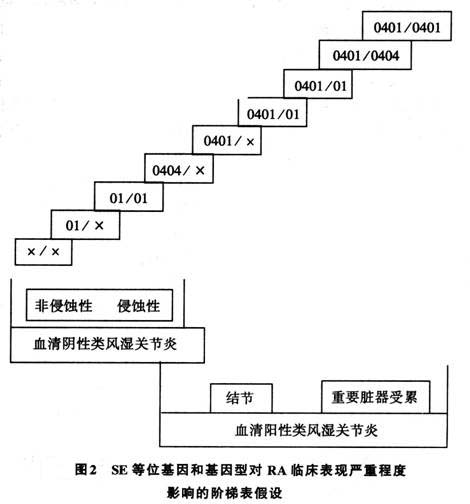



 ��������
��������

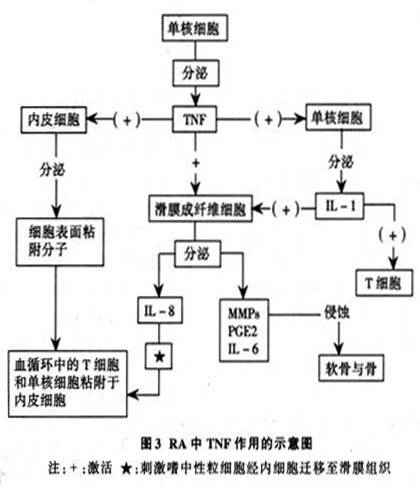
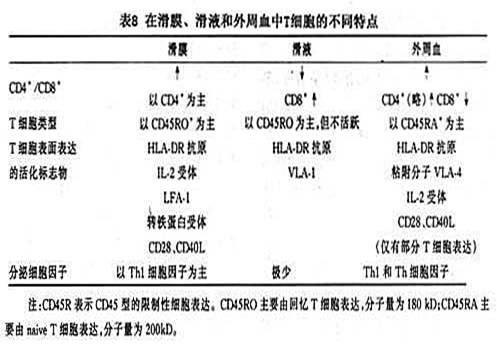




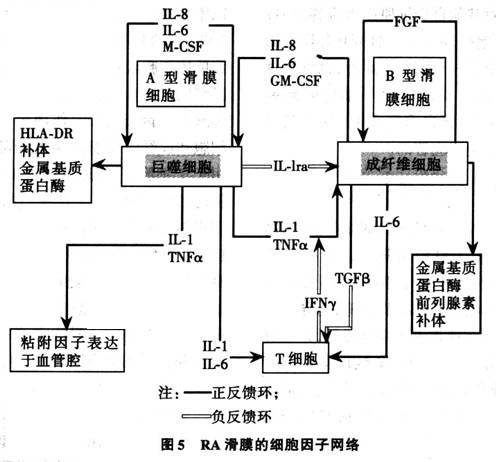




 �ٴ�����
�ٴ�����
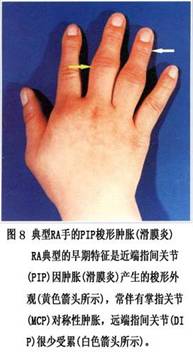
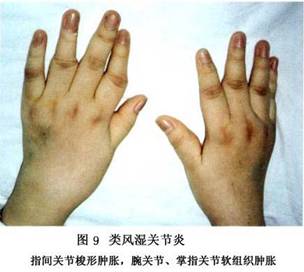
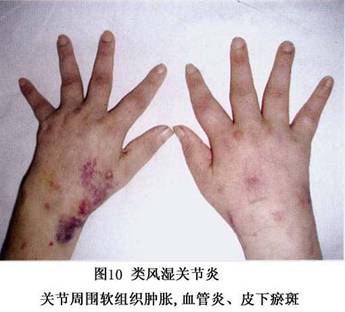
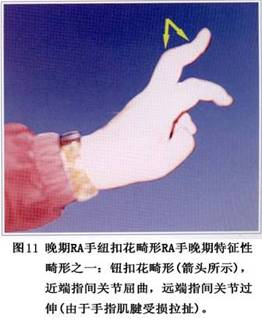
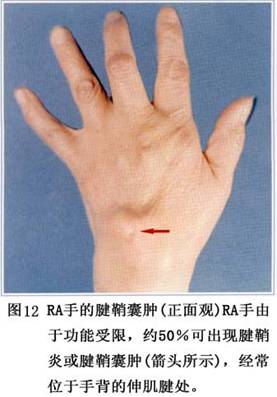
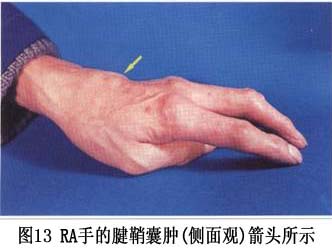
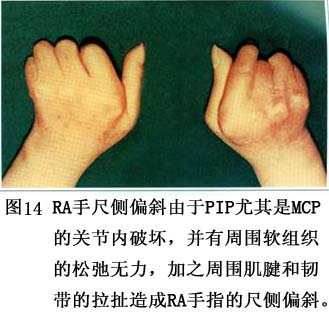
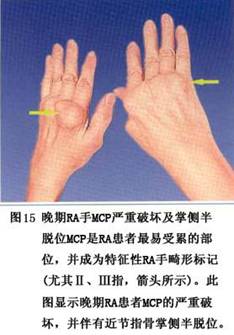
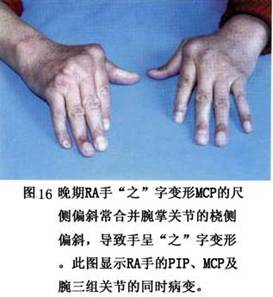

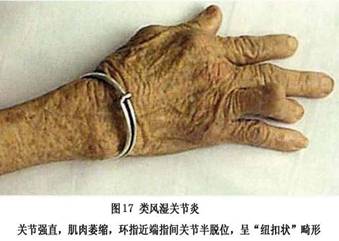
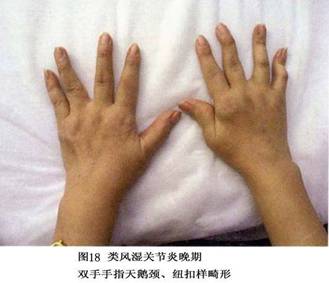
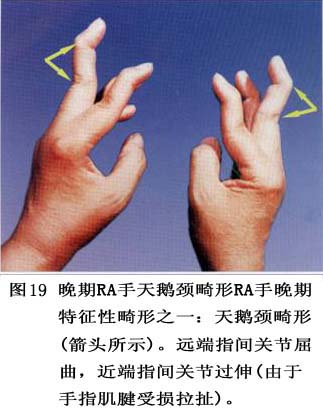
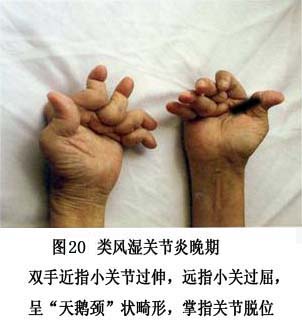
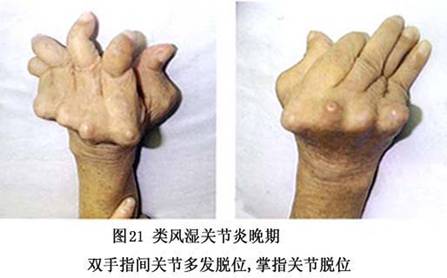
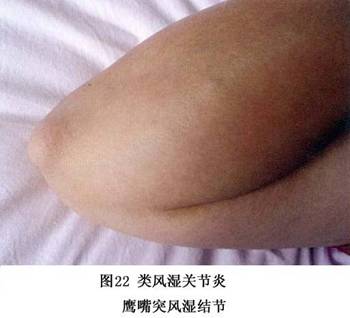
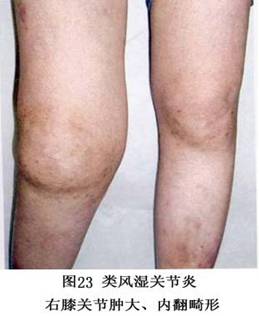
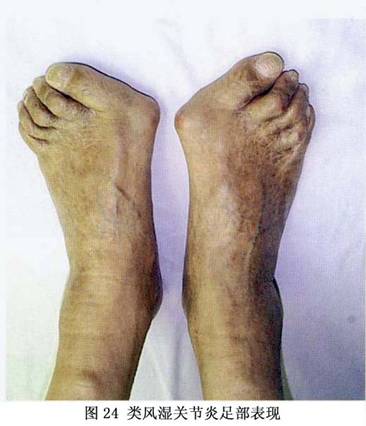

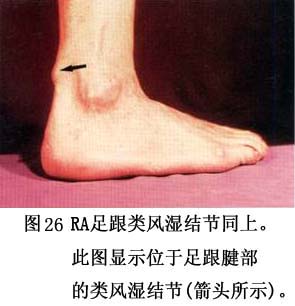

 ����֢
����֢
 ʵ���Ҽ��
ʵ���Ҽ��
 �����������
�����������
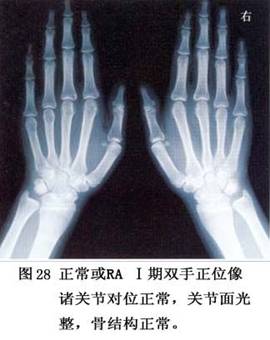
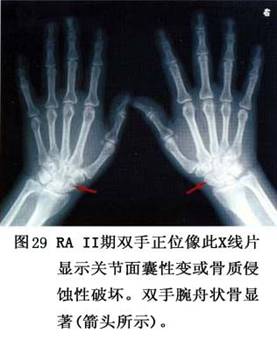
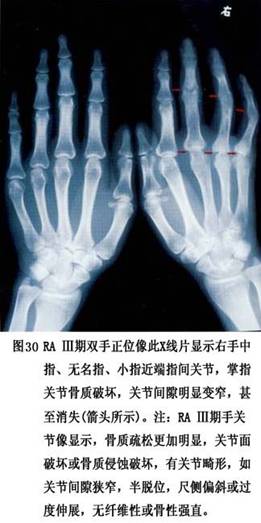
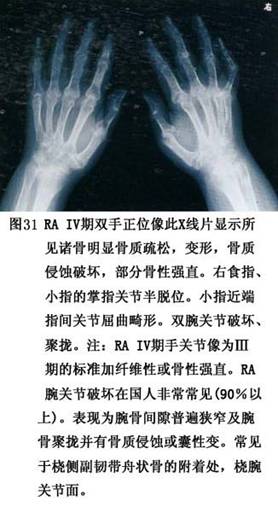
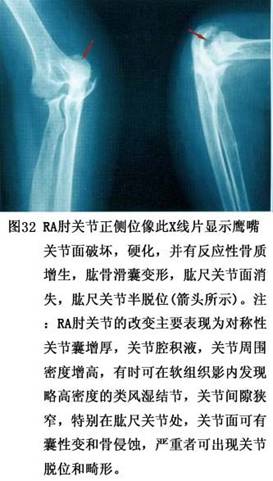
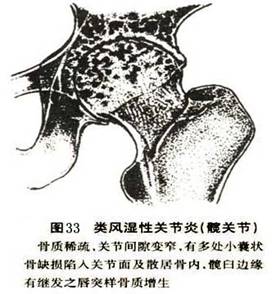
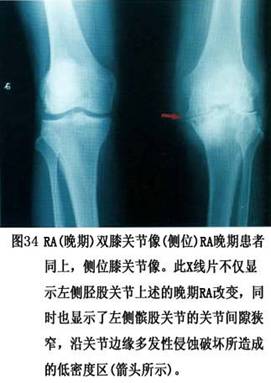
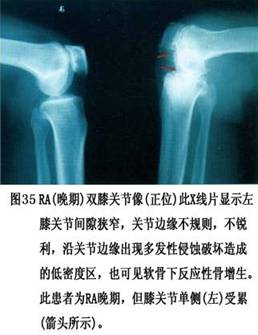
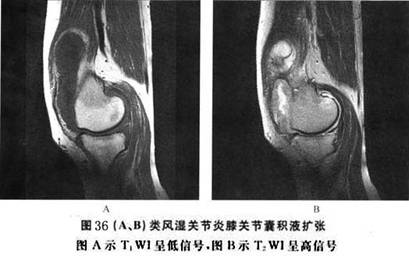
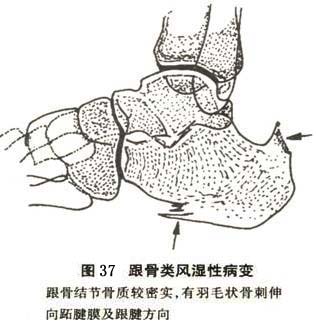
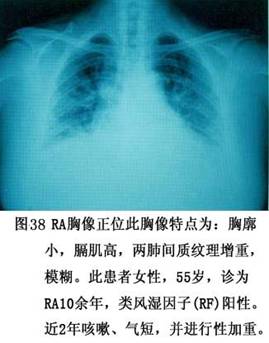
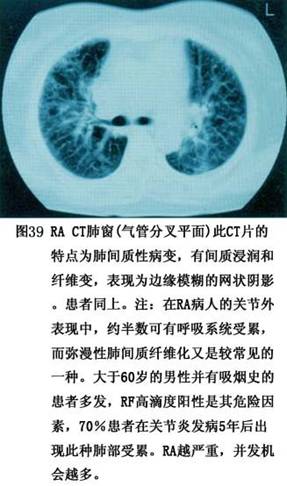
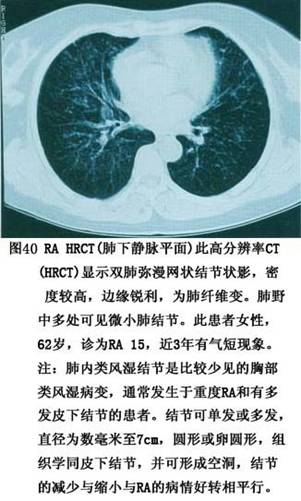
 ���
���
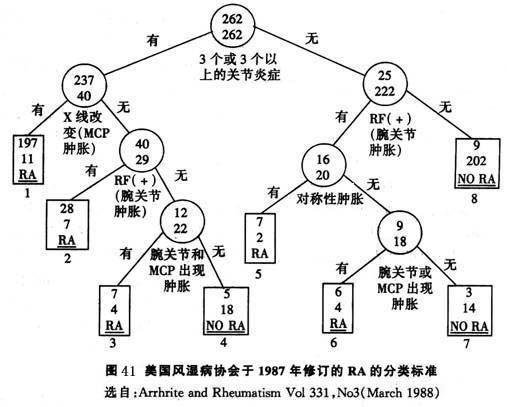
 �������
�������

 ����
����
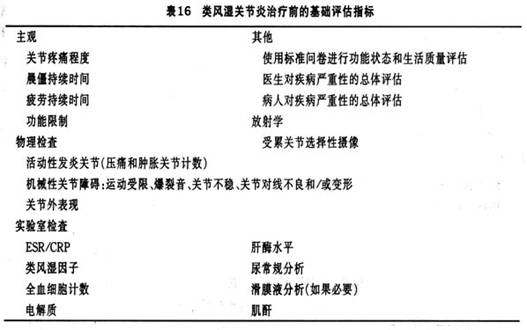



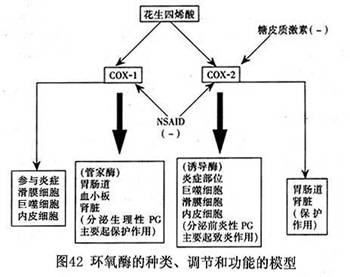
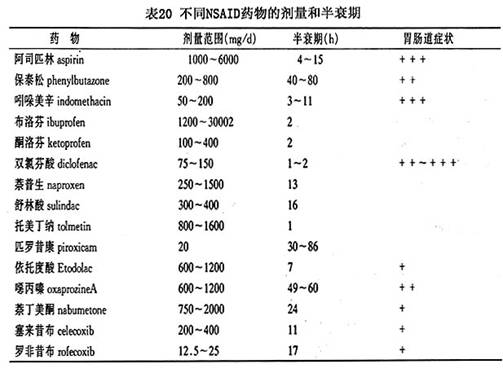

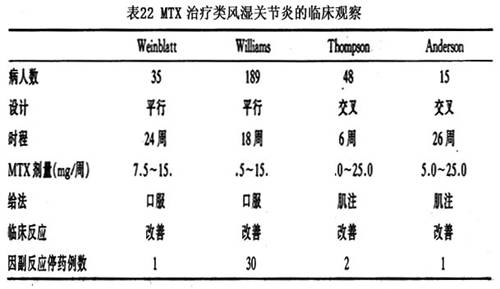













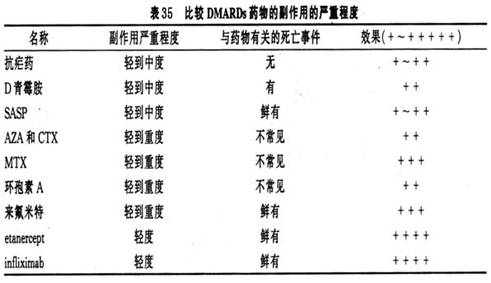
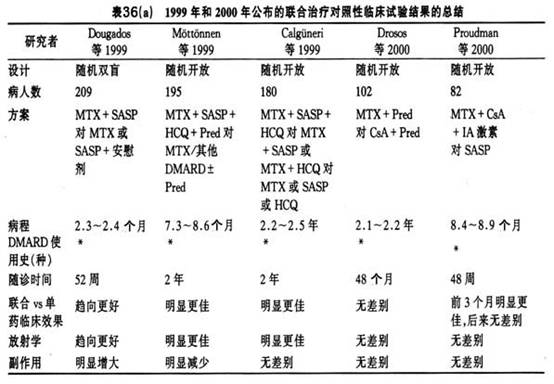

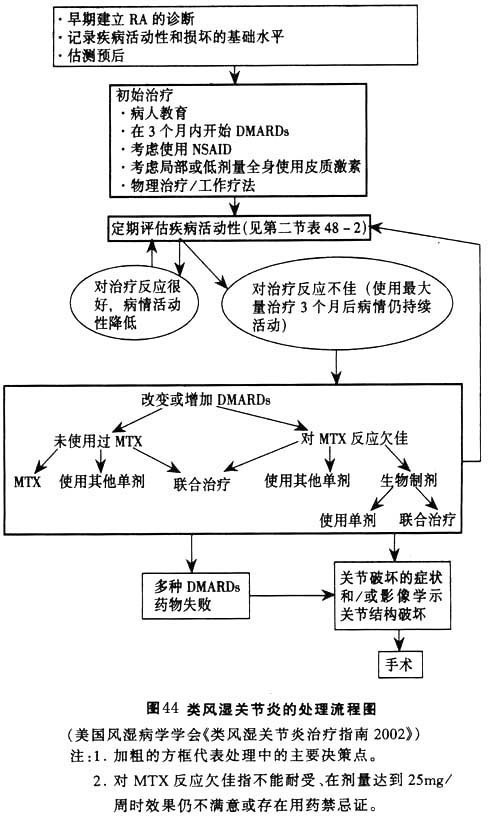
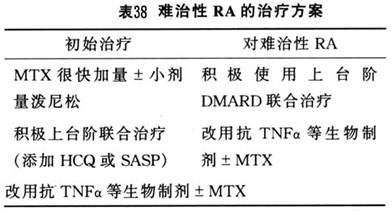

 Ԥ��
Ԥ��
 Ԥ��
Ԥ��
